人教版(2019)選擇性必修1《1.2 反應熱的計算》2020年同步練習卷(4)
發(fā)布:2024/12/18 6:30:2
-
1.已知下列熱化學方程式:
①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H1=-26.7kJ?mol-1
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=-50.75kJ?mol-1
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H3=-36.5kJ?mol-1
則反應FeO(s)+CO(g)═Fe(s)+CO2(g)的焓變?yōu)椋ā 。?/h2>A.+7.28 kJ?mol-1 B.-7.28 kJ?mol-1 C.+43.68 kJ?mol-1 D.-43.68 kJ?mol-1 組卷:261引用:15難度:0.9 -
2.下列變化過程需要吸收能量的是( )
A.氫氣球發(fā)生爆炸 B.向污染的河水中投放生石灰 C. 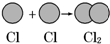
D. 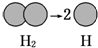 組卷:29引用:4難度:0.9
組卷:29引用:4難度:0.9 -
3.下列說法正確的是( )
A.反應熱是1 mol物質參加反應時的能量變化 B.當反應放熱時△H>0,反應吸熱時△H<0 C.任何條件下,化學反應的焓變都等于化學反應的反應熱 D.在一定條件下,某一化學反應是吸熱反應還是放熱反應,由生成物與反應物的焓的差值來決定 組卷:77引用:7難度:0.5 -
4.下列各組熱化學方程式中,化學反應的△H前者大于后者的是( )
①C(s)+O2(g)═CO2(g)△H1 C(s)+O2(g)═CO(g)△H212
②S(s)+O2(g)═SO2(g)△H3 S(g)+O2(g)═SO2(g)△H4
③H2(g)+O2(g)═H2O(l)△H5 2H2(g)+O2(g)═2H2O(l)△H612
④CaCO3(s)═CaO(s)+CO2(g)△H7 CaO(s)+H2O(l)═Ca(OH)2(s)△H8.A.① B.④ C.②③④ D.①②③ 組卷:811引用:181難度:0.7 -
5.下列說法正確的是( )
A.酸和堿發(fā)生中和反應生成H2O時所放出的熱量稱為中和熱 B.物質完全燃燒生成氧化物時所放出的熱量叫做該物質的燃燒熱 C.反應物所具有的總能量大于生成物所具有的總能量時,△H<0 D.反應物所具有的總能量小于生成物所具有的總能量時,△H<0 組卷:20引用:2難度:0.8 -
6.已知:N2(g)+3H2(g)?2 NH3(g)△H=-92.4 kJ?mol-1.一定條件下,現(xiàn)有容積相同且恒容的密閉容器甲與乙:①向甲中通入1 mol N2和3 mol H2,達到平衡時放出熱量Q1 kJ;②向乙中通入0.5 mol N2和1.5 mol H2,達到平衡時放出熱量Q2 kJ.則下列關系式正確的是( )
A.Q1=2Q2=92.4 B.92.4=Q1<2Q2 C.92.4>Q1>2Q2 D.Q1=2Q2<92.4 組卷:106引用:3難度:0.7 -
 7.已知:
7.已知:
①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H1=-905.5kJ?molˉ1
②N2(g)+O2(g)?2NO(g)△H2
一定條件下,NO可以與NH3反應轉化為無害的物質,反應如下:
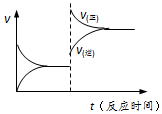
③4NH3(g)+4NO(g)+O2(g)?4N2(g)+6H2O(g)△H3=-1625.5 kJ?molˉ1下列說法正確的是( )A.反應①使用催化劑,△H1減小 B.反應②生成物總能量低于反應物總能量 C.反應③一定能自發(fā)進行 D.反應③達到平衡后升高溫度,v(正)、v(逆)的變化如圖所示 組卷:143引用:5難度:0.7
-
22.發(fā)射衛(wèi)星時可用肼(N2H4)作燃料,二氧化氮作氧化劑,兩者反應生成氮氣和氣態(tài)水。
(1)肼(N2H4)中氮元素化合價為,氮氣的電子式為。
(2)肼和二氧化氮反應的化學方程式為。
(3)已知拆開1mol H-H鍵,1mol O-H(g)鍵,1mol O=O鍵分別需要的能量是436kJ、463kJ、496kJ,則O2與H2反應生成2mol H2O(g)所釋放的熱量為kJ
(4)已知N2H4(g)-空氣燃料電池,電解質溶液為KOH溶液,若負極產(chǎn)生了一種無毒氣體N2,則負極的電極反應式為;若導線中轉移電子2mol,則標況下正極消耗的O2為L。組卷:7引用:1難度:0.5 -
23.某實驗小組同學進行如下實驗,以檢驗化學反應中的能量變化.請回答下列問題:

(1)實驗中發(fā)現(xiàn),反應后①中的溫度,②中的溫度.(填“升高”或“降低”)
(2)上述反應過程中的能量變化可用圖2表示的是。(填“①”或“②”)
(3)實驗①中測得產(chǎn)生氣體的速率與時間的關系如圖3所示,則t2-t3反應速率逐漸減小的主要原因是.
(4)寫出①中發(fā)生反應的離子方程式:.組卷:10引用:2難度:0.5


