魯科版(2019)必修第二冊《2.3.2 化學反應的限度》2020年同步練習卷(1)
發布:2024/4/20 14:35:0
-
1.可逆反應達化學平衡時,下列說法不正確的是( )
A.正反應速率等于逆反應速率 B.不再繼續反應 C.混合物的各成分的百分含量不變 D.同時存在反應物和生成物 組卷:7引用:1難度:0.7 -
2.可逆反應2SO2+O2?2SO3達到平衡的標志是( )
①消耗2mol SO2的同時生成2mol SO3
②SO2、O2與SO3的物質的量之比為2:1:2
③反應混合物中,SO3的質量分數不再改變.A.①② B.①③ C.只有③ D.只有① 組卷:71引用:30難度:0.7 -
 3.過程中以B的濃度改變表示的反應速率v正、v逆與時間t的關系如圖所示,則圖中陰影部分的面積表示為( )
3.過程中以B的濃度改變表示的反應速率v正、v逆與時間t的關系如圖所示,則圖中陰影部分的面積表示為( )A.c(B)減少 B.n(B)減少 C.c(B)增加 D.c(B)增加 組卷:14引用:2難度:0.7 -
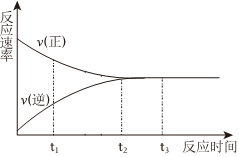 4.一定條件下的某可逆反應,其正反應速率v(正)和逆反應速率v(逆)隨反應時間t的變化如圖所示.下列判斷不正確的是( )
4.一定條件下的某可逆反應,其正反應速率v(正)和逆反應速率v(逆)隨反應時間t的變化如圖所示.下列判斷不正確的是( )A.t1時刻,v(正)>v(逆) B.t2時刻,v(正)=v(逆) C.t2時刻,反應達到最大限度 D.t3時刻,反應停止 組卷:40引用:8難度:0.7 -
 5.右圖是可逆反應N2(g)+3H2(g)═2NH3(g) 在反應過程中的反應速率(v)與時間(t)的關系曲線,下列敘述不正確的是( )
5.右圖是可逆反應N2(g)+3H2(g)═2NH3(g) 在反應過程中的反應速率(v)與時間(t)的關系曲線,下列敘述不正確的是( )A.t1時,v正>v逆 B.t2時,反應到達限度 C.t2-t3,反應停止 D.t2-t3,各物質的濃度不再發生變化 組卷:46引用:3難度:0.9
-
 15.一定溫度下,某恒容密閉容器中含有NO2、N2O4兩種氣體,反應開始至達到平衡狀態過程中,兩種物質的濃度隨時間的變化如圖所示。
15.一定溫度下,某恒容密閉容器中含有NO2、N2O4兩種氣體,反應開始至達到平衡狀態過程中,兩種物質的濃度隨時間的變化如圖所示。
(1)表示NO2濃度變化的曲線是(填“x”或“y”),寫出相應的化學方程式:。
(2)從反應開始至達到平衡的過程中,用N2O4表示的反應速率v(N2O4)=。a、b兩點對應狀態中,x代表的物質的反應速率相對大小為v(a)v(b)。
(3)若平衡后改變溫度,容器中氣體的平均摩爾質量變大,則反應向生成(填“NO2”或“N2O4”)的方向進行。組卷:6引用:2難度:0.7 -
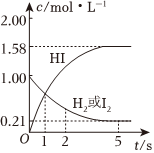 16.某溫度時,向某VL的密閉容器中充入3mol H2(g)和3mol I2(g),發生反應H2(g)+I2(g)?2HI(g),測得各物質的物質的量濃度與時間變化的關系如圖所示。請回答下列問題:
16.某溫度時,向某VL的密閉容器中充入3mol H2(g)和3mol I2(g),發生反應H2(g)+I2(g)?2HI(g),測得各物質的物質的量濃度與時間變化的關系如圖所示。請回答下列問題:
(1)V=L。
(2)該反應達到最大限度的時間是s,該段時間內的平均反應速率v(HI)=mol?L-1?s-1。
(3)當反應達到平衡狀態時,n(HI)=。
(4)判斷反應達平衡的依據是(填序號)。
①H2消耗的速率和I2消耗的速率相等
②H2、I2、HI的濃度比為1:1:2
③H2、I2、HI的濃度都不再發生變化
④該條件下正、逆反應速率都為零
⑤混合氣體的平均相對分子質量不再發生變化
⑥氣體的顏色不再發生變化組卷:9引用:2難度:0.7


