2021-2022學年遼寧省營口第二高級中學高二(上)第一次月考化學試卷
發布:2024/11/18 11:0:1
一、單選題
-
1.醋酸溶液中存在電離平衡 CH3COOH?CH3COO-+H+,下列敘述不正確的是( )
A.升高溫度,平衡正向移動,醋酸的電離常數Ka增大 B.CH3COOH溶液加少量的CH3COONa固體,平衡逆向移動 C.室溫下,欲使0.1 mol/L醋酸溶液的電離度α增大,可加入少量冰醋酸 D.0.10 mol/L的CH3COOH 溶液加水稀釋,溶液中c(CH3COOH)/c(CH3COO-)減小 組卷:48引用:5難度:0.7 -
2.25℃時,下列事實不能說明HF是弱酸的是( )
A.0.1mol?L-1的氫氟酸溶液pH>1 B.升溫,氫氟酸溶液的酸性明顯增強 C.氫氟酸溶液中含有HF分子 D.稀氫氟酸溶液的導電能力弱 組卷:83引用:4難度:0.8 -
3.下列說法正確的是( )
A.將AgCl放入水中不能導電,故AgCl不是電解質 B.CO2溶于水得到的溶液能導電,所以CO2是電解質 C.金屬能導電,所以金屬是電解質 D.固態的NaCl不導電,熔融態的NaCl能導電,NaCl是電解質 組卷:745引用:27難度:0.9 -
4.稀氨水中存在著下列平衡:NH3?H2O?NH4++OH-,若要使平衡向逆反應方向移動,同時使c(OH-)增大,應加入的物質或采取的措施是( )
①NH4Cl;②硫酸;③NaOH固體;④水;⑤加熱;⑥少量MgSO4固體。A.①②③⑤ B.③ C.③④⑥ D.③⑤ 組卷:86引用:5難度:0.7 -
5.由表格中電離常數可以判斷下列反應可以發生的是( )
弱酸 HClO H2CO3 電離平衡常數(25℃) K=3.0×10-8 K1=4.5×10-7
K2=4.7×10-11A.NaClO+NaHCO3═HClO+Na2CO3 B.NaClO+CO2+H2O═HClO+NaHCO3 C.2NaClO+CO2+H2O═2HClO+Na2CO3 D.2HClO+Na2CO3═2NaClO+CO2+H2O 組卷:20引用:4難度:0.6 -
6.25℃時,相同物質的量濃度的下列溶液:①NaCl ②NaOH ③H2SO4其中水的電離程度按由大到小順序排列的一組是( )
A.③>②>① B.②>③>① C.①>②>③ D.③>①>② 組卷:178引用:8難度:0.9
二、填空題
-
19.25℃時,有關物質的電離平衡常數如下:
(1)電解質由強至弱的順序為化學式 CH3COOH H2CO3 H2SO3 電離平衡常數 K=1.8×10-5 K1=4.3×10-7
K2=5.6×10-11K1=1.5×10-2
K2=1.02×10-7(用化學式表示,下同).
(2)常溫下,0.02mol?L-1的CH3COOH溶液的電離度約為,體積為10mL pH=2的醋酸溶液與亞硫酸溶液分別加蒸餾水稀釋至1000mL,稀釋后溶液的pH,前者后者(填“>”、“<”或“=”).
(3)下列離子CH3COO-、CO32-、HSO3-、SO32-、在溶液中結合H+的能力由大到小的關系為.組卷:7引用:4難度:0.5 -
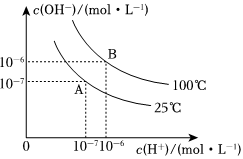 20.在水的電離平衡中,c(H+)和c(OH-)的關系如圖所示:
20.在水的電離平衡中,c(H+)和c(OH-)的關系如圖所示:
(1)A點水的離子積常數為1×10-14,B點水的離子積常數為。造成水的離子積常數變化的原因是。
(2)100℃時,若向水中滴加鹽酸,(填“能”或“不能”)使體系處于B點狀態,原因是。
(3)100℃時,若鹽酸中c(H+)=5×10-4mol?L-1,則由水電離產生的c(H+)=。
(4)25℃時,若pH=a的100體積某強酸溶液與pH=b的1體積某強堿溶液混合后溶液呈中性,則混合之前該a+b=組卷:48引用:1難度:0.7


