2022年山東省青島十九中自主招生化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題(共7小題,每題3分,共30分)
-
1.近年來,我國科技發展日新月異,國力的日益強大印證了科技興則民族興、科技強則民族強的道理。2022年北京冬奧會完美落幕,請利用你學過的化學知識完成1-4題:
下列變化中屬于化學變化的是( )A.速滑館“冰絲帶”用二氧化碳做制冷劑制冰 B.蘇格蘭人用花崗巖制成冰壺 C.天宮課堂中王亞平老師用酚酞和純堿溶液做出五環中的紅環 D.開幕式上冰立方雕刻成的奧運五環徐徐升起 組卷:29引用:0難度:0.80 -
2.近年來,我國科技發展日新月異,國力的日益強大印證了科技興則民族興、科技強則民族強的道理。2022年北京冬奧會完美落幕,請利用你學過的化學知識完成1-4題:
下列關于冬奧會的化學知識描述正確的是( )A.化學與材料 B.化學與健康 ①滑雪頭盔中使用的玻璃纖維屬于有機合成材料
②制作滑雪板的玻璃鋼屬于復合材料①餐廳食譜中的糖醋里脊富含糖類、維生素和蛋白質
②奧運村的直飲水為軟水,在生活中我們可以采用煮沸的方式將硬水轉化為軟水C.化學與環境 D.化學與能源 ①冬奧比賽體現綠色低碳理念,其中低碳就是指降低二氧化碳的排放
②冬奧場館防疫消毒,使用的消毒液濃度越高效果越好①光伏發電將太陽能轉化為電能
②火炬“飛揚”利用氫氣為燃料,實現污染零排放A.A B.B C.C D.D 組卷:42引用:0難度:0.80 -
3.近年來,我國科技發展日新月異,國力的日益強大印證了科技興則民族興、科技強則民族強的道理。2022年北京冬奧會完美落幕,請利用你學過的化學知識完成1-4題:
 冬奧會完美落幕,冰雪五環驚艷世界。在復習時同學們驚奇的發現,“五環”能形象的呈現常見物質間的關系,如圖所示,甲、乙分別是氧氣、氧化鐵、稀鹽酸、氫氧化鈣四種物質中的一種,“五環”中相交兩環的物質間能夠發生化學反應。下列說法錯誤的是( )
冬奧會完美落幕,冰雪五環驚艷世界。在復習時同學們驚奇的發現,“五環”能形象的呈現常見物質間的關系,如圖所示,甲、乙分別是氧氣、氧化鐵、稀鹽酸、氫氧化鈣四種物質中的一種,“五環”中相交兩環的物質間能夠發生化學反應。下列說法錯誤的是( )A.甲與碳的反應有可能生成有毒物質 B.甲與鐵的反應很劇烈,火星四射,放熱 C.鐵與乙反應得到淺綠色溶液 D.圖中反應只涉及兩種基本反應類型 組卷:37引用:0難度:0.70 -
4.近年來,我國科技發展日新月異,國力的日益強大印證了科技興則民族興、科技強則民族強的道理。2022年北京冬奧會完美落幕,請利用你學過的化學知識完成1-4題:
碲化鎘發電玻璃成為綠色和科技辦奧交匯的創新點。如圖是碲的原子結構示意圖,有關信息正確的是( )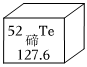
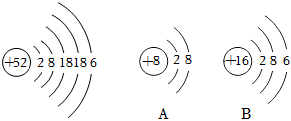
A.碲的中子數為52 B.碲可以形成碲酸H6TeO6,其中碲的化合價為+6 C.碲的化學性質與A和B相似 D.碲位于周期表中的第六周期 組卷:30引用:0難度:0.80 -
5.工業上綜合利用鋁土礦(主要成分為Al2O3,還含有Fe2O3、FeO、SiO2)的部分工藝流程如圖。實驗室模擬上述流程中,不需要使用的裝置是( )
鋁土礦濾渣稀硫酸過濾硅酸鈉氫氧化鈉固體灼燒A. 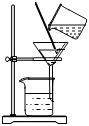
B. 
C. 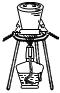
D. 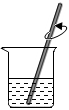 組卷:36引用:1難度:0.5
組卷:36引用:1難度:0.5
三、解答題(共5小題,滿分45分)
-
19.我國高鐵創造的中國速度令世界矚目,到2050年,我國將全面建成更高水平的現代化鐵路強國。高鐵建設中金屬鐵的應用極為廣泛,某興趣小組的同學對鐵及其化合物開展了一系列探究。
【探究一】生活中的鐵
(1)高鐵鐵軌建設多使用鐵合金而不用純鐵,是因為鐵合金比純鐵(填“軟”或“硬”)。
(2)鐵粉放在食品包裝袋中用途廣泛,被稱為“雙吸劑”這是因為:。
【探究二】鐵的回收利用
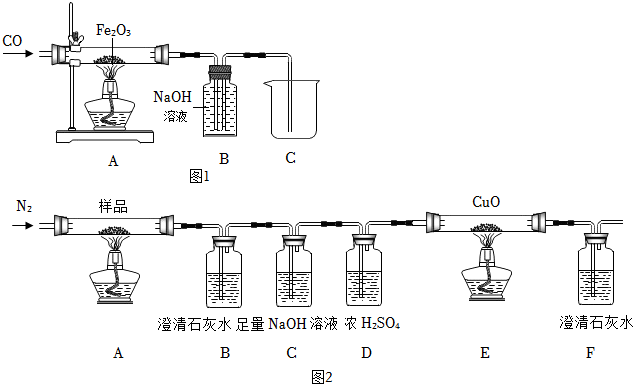
該興趣小組的同學回收使用過的“雙吸劑”粉末,利用圖1所示實驗裝置模擬工業煉鐵。
(1)連接好裝置后應先,再添加藥品完成實驗。
(2)如果實驗成功,裝置A中發生反應的化學方程式為,玻璃管內反應的實驗現象是。
(3)裝置B的作用是(填字母)。
A.吸收CO2
B.檢驗CO2
C.收集CO
【探究三】鐵的化合物
三草酸合鐵酸鉀K3[Fe(C2O4)3]是制作含鐵催化劑的主要原料,該興趣小組探究無水三草酸合鐵酸鉀K3[Fe(C2O4)3]樣品受熱分解的產物,并對所得氣體產物和固體產物進行驗證,按圖2裝置進行實驗(夾持儀器已略去,假設每步所需藥品均足量)
(1)實驗開始時緩緩通入氮氣一段時間后,應先加熱反應管(填“A”或“E”)。
(2)待反應完全后,停止實驗的先后順序為。(選填下列序號)
①停止通入氮氣
②熄滅A處酒精燈
③熄滅E處酒精燈
(3)足量NaOH溶液的作用是。
(4)能證明分解產物中有CO氣體生成的實驗現象是。
(5)該小組為探究反應后所得固體中鐵元素的存在形式,取A中充分反應后所得固體于試管中,加入足量蒸餾水,過濾、洗滌、干燥得到7.2g黑色粉末(經分析固體中僅含鐵、氧兩種元素),將7.2g該黑色粉末與100g溶質質量分數為7.3%的稀鹽酸恰好完全反應生成氯化亞鐵,求出黑色粉末中鐵原子與氧原子的個數比。組卷:144引用:1難度:0.4 -
20.MgSO4?7H2O在工農業生產中均有廣泛用途,現以菱鎂礦石(主要成分是MgCO3,含少量MnCO3、SiO2)制取MgSO4?7H2O晶體,實驗流程如圖:
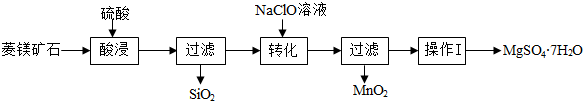
(1)“酸浸”時,為了提高浸取率,除了攪拌、提高硫酸濃度外,還可采取的措施有(寫出一種即可)。此時,MnCO3發生反應的化學方程式是。
(2)“轉化”時主要反應是NaClO+MnSO4+H2O═MnO2↓+NaCl+H2SO4,氯元素反應前后化合價變化情況是(填“升高”或“降低”)。
(3)硫酸鎂溶液在不同溫度下進行濃縮結晶,可得到不同的晶體:
①“操作Ⅰ”的具體操作過程是:在48℃左右蒸發濃縮濾液至表面有晶膜、溫度/℃ -3.9~1.8 1.8~48.1 48.1~67.5 67.5~200 析出晶體 MgSO4?12H2O MgSO4?7H2O MgSO4?6H2O MgSO4?H2O等 、過濾、洗滌、低溫干燥。
②“操作Ⅰ”所得濾液中能分離出一種可循環使用的物質,該物質是(填化學式)。
(4)已知:MgSO4?7H2O中鎂元素質量分數為9.76%,采用熱分析法測定所得MgSO4?7H2O樣品中鎂元素質量分數:
①未加熱前,測得樣品中鎂元素質量分數略大于9.76%,可能的原因是。
②高于900℃后,測得剩余固體中鎂元素質量分數大于20%,可能的原因是。
(5)若用100t菱鎂礦石可制得246tMgSO4?7H2O產品,忽略反應過程中鎂元素損失,則該菱鎂礦石中MgCO3的質量分數為。組卷:172引用:1難度:0.3


