2023年江蘇省南通市如皋市中考化學一模試卷
發(fā)布:2024/6/9 8:0:9
一、選擇題(每小題2分,共20分)
-
1.下列常見食物富含糖類的是( )
A.青菜 B.面條 C.雞蛋 D.黃瓜 組卷:14引用:1難度:0.5 -
2.人類的生存離不開氧氣。下列有關氧氣的說法正確的是( )
A.硫在氧氣中燃燒生成三氧化硫 B.保持氧氣化學性質的最小粒子是氧原子 C.魚類能在水中生存,說明氧氣易溶于水 D.實驗室常用加熱KMnO4的方法制取氧氣 組卷:38引用:1難度:0.7 -
3.用鋅粒與稀硫酸反應制取并收集氫氣的部分操作如下,其中不正確的是( )
A. 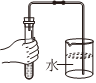
檢查氣密性B. 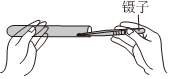
加入鋅粒C. 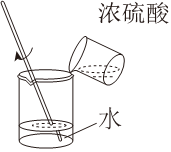
稀釋濃硫酸D. 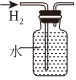
收集氫氣組卷:33引用:1難度:0.7 -
4.下列有關物質的性質與用途具有對應關系的是( )
A.氮氣難溶于水,可用作保護氣 B.濃硫酸具有吸水性,可用作干燥劑 C.金剛石無色透明,可用于制作鉆頭 D.熟石灰微溶于水,可用于改良酸性土壤 組卷:21引用:1難度:0.7
二、非選擇題
-
14.氫氧化鈉是重要的化工原料。某興趣小組對氫氧化鈉進行了如下探究:
Ⅰ.氫氧化鈉的制備
用氯化鈉溶液制備氫氧化鈉的部分流程如下:
(1)在實驗室中進行操作①時,常采取的措施有(任寫一種)。
(2)操作②發(fā)生反應的化學方程式為。
(3)取少量通過上述流程制得的氫氧化鈉樣品于燒杯中,向其中加入足量稀硝酸,再滴入硝酸銀溶液,有白色沉淀生成,說明樣品中含有。
Ⅱ.氫氧化鈉的性質
(4)某小組將酚酞溶液滴入NaOH溶液中,溶液變?yōu)榧t色,一段時間后紅色消失。
【提出問題】滴有酚酞的NaOH溶液由紅色褪為無色的原因是什么?
【猜想與假設】
甲同學:酚酞與O2發(fā)生了反應;
乙同學:NaOH溶液與空氣中的CO2發(fā)生了反應;
丙同學:與NaOH溶液濃度大小有關。
【設計與實驗】三位同學為驗證各自的猜想,設計并進行了如下實驗。
①甲同學取少量實驗中的NaOH溶液于試管中,加熱煮沸,冷卻后滴入酚酞溶液,并迅速向試管中滴入植物油,植物油的作用是。
②乙同學進行如圖所示實驗,試管中溶液的紅色褪去,他認為自己的猜想正確。丁同學認為該現(xiàn)象不能佐證乙同學的猜想,理由是。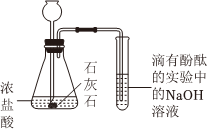
③丙同學取質量分數(shù)為30%和0.5%的NaOH溶液各2mL分別置于1、2號試管中,滴入數(shù)滴酚酞溶液,觀察到1號試管中紅色很快褪去,2號試管中;由此判斷自己的猜想正確。
Ⅲ.氫氧化鈉的用途
(5)某“管道疏通劑”的成分為氫氧化鈉固體、鋁粉、硝酸鈉。其工作原理是鋁和氫氧化鈉遇水反應(原理為2Al+2NaOH+2H2O=2NaAlO2+3H2↑)放出大量的熱,能加快氫氧化鈉對毛發(fā)等淤積物的腐蝕;產生的氣體能增加管道內的氣壓,利于疏通。
①使用該疏通劑時要防止明火,原因是該疏通劑與水反應產生的在空氣中遇到明火可能會引起爆炸。
②檢驗發(fā)現(xiàn),該疏通劑與水反應前后硝酸鈉的質量和化學性質均未改變。由此,同學們猜測:硝酸鈉可能是鋁粉和氫氧化鈉溶液反應的催化劑。請設計實驗判斷此猜想是否正確,簡述實驗過程(包括操作、現(xiàn)象和結論):。(實驗中必須使用的試劑:鋁粉、氫氧化鈉溶液、硝酸鈉粉末)組卷:84引用:2難度:0.5 -
15.某學習小組對某胃藥“碳酸氫鈉片”(標簽如圖)進行了如下探究:

步驟1:取2片胃藥,研碎后放入錐形瓶中,加水完全溶解得到150g溶液;
步驟2:以質量分數(shù)為36.5%的濃鹽酸和蒸餾水為原料,配制100g質量分數(shù)為0.365%的稀鹽酸作為模擬胃酸;
步驟3:取步驟1所得溶液30g于錐形瓶中,再將步驟2所得模擬胃酸逐滴加入瓶內,用磁力攪拌器充分攪拌,測得實驗過程中溶液的pH變化情況如圖-2所示。
(1)NaHCO3溶液顯(填“酸性”“堿性”或“中性”)。
(2)步驟2中所需蒸餾水的體積為mL。
(3)步驟3中,胃藥中其它成分不參加反應。請通過計算判斷該胃藥中碳酸氫鈉的含量是否與標簽相符。組卷:61引用:2難度:0.3


