2022-2023學年江蘇省無錫市江陰市九年級(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括20小題,每小題只有1個選項符合題意。每小題2分,共40分)
-
1.“共建清潔美麗世界”,我們在行動。下列做法不符合這一主題的是( )
A.拒絕使用一次性餐具 B.超市購物自備購物袋 C.生活污水處理后排放 D.大量施用農藥和化肥 組卷:49引用:7難度:0.7 -
2.2022年第24屆冬季奧林匹克運動會在中國成功舉辦,此次盛會向世界展示了中國力量。下列涉及化學變化的是( )
A.點燃“飛揚”火炬 B.硅膠漿料在模具中冷卻成型 C.用絨線手工編織頒獎花束 D.裁剪布料制成“瑞雪祥云”服飾 組卷:282引用:22難度:0.7 -
3.地殼中含量最多的元素是( )
A.Fe B.Al C.Si D.O 組卷:853引用:280難度:0.9 -
4.將下列四種家庭常用的調味品分別放入水中,不能形成溶液的是( )
A.食用油 B.食鹽 C.味精 D.蔗糖 組卷:69引用:15難度:0.9 -
5.“讓中國人的飯碗牢牢端在自己手中”,化肥起到非常重要的作用,下列化肥中屬于磷肥的是( )
A.K2CO3 B.K2SO4 C.Ca(H2PO4)2 D.CO(NH2)2 組卷:13引用:1難度:0.8 -
6.小明同學在實驗時,做了下列記錄,有關實驗現象描述正確的是( )
A.NH4NO3固體溶于水,溶液的溫度升高 B.打開盛有濃鹽酸試劑瓶的瓶塞,瓶口出現大量白煙 C.鐵絲在氧氣中劇烈燃燒,火星四射,生成四氧化三鐵 D.氫氧化鈉溶液中加入硫酸銅溶液,產生藍色沉淀 組卷:46引用:2難度:0.5 -
7.下列有關物質的性質與用途對應關系正確的是( )
A.碳酸氫銨受熱易分解,可用作氮肥 B.CO2能與水反應,可用于滅火 C.純堿具有堿性,可用于治療胃酸過多 D.石墨有導電性,可作干電池的電極 組卷:21引用:1難度:0.7 -
8.如圖所示的有關化學實驗操作正確的是( )
A. 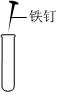
向試管中加入鐵釘B. 
配制溶液C. 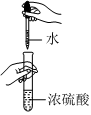
稀釋濃硫酸D. 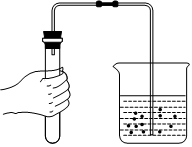
檢查裝置氣密性組卷:50引用:2難度:0.7 -
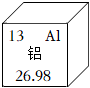 9.硬鋁常用于制造火箭、飛機的外殼,鋁元素的相關信息如圖所示,下列說法正確的是( )
9.硬鋁常用于制造火箭、飛機的外殼,鋁元素的相關信息如圖所示,下列說法正確的是( )A.鋁元素的相對原子質量為13 B.Al2O3中Al為+2價 C.硬鋁的強度和硬度比鋁的大 D.鋁是非金屬元素 組卷:4引用:1難度:0.6
二、化學是改變現有世界,給予我們美好生活的科學。完成21~23題。
-
27.目前,鐵是使用最廣泛的金屬,同學們對生活中的鐵制品展開了項目化學習的探究。
任務一:尋找生活中廢舊鐵制品的一些處理方法。
(1)方法1:丟棄。結合圖,生銹的廢舊鐵制包裝盒屬于(填寫序號)。
(2)方法2:除銹翻新。除鐵銹常用加入稀鹽酸的方法,但是如果稀鹽酸過量還會腐蝕金屬鐵,寫出鐵與稀鹽酸反應的化學方程式,反應的現象是。
任務二:實驗探究鐵生銹的條件及影響因素
實驗1:如圖所示進行實驗1,一段時間后觀察到C中鐵釘生銹,AB中鐵釘無明顯變化。
實驗2:為進一步探究影響鐵生銹速率的因素,小組同學設計如圖所示實驗2,利用傳感器監測該過程中氧氣濃度的變化來判斷鐵生銹的情況。實驗記錄如表: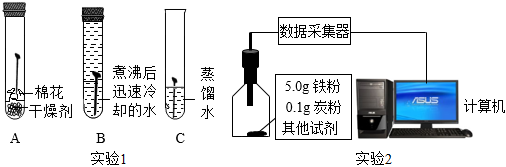
【解釋與結論】序號 其他試劑 初始時氧氣濃度/% 200s時氧氣濃度/% 水/滴 食鹽質量/g 稀醋酸/滴 ① 0 0 0 20.8 20.8 ② 10 0 0 20.8 15.2 ③ 10 0 5 20.8 12.7 ④ 10 1.0 0 20.8 8.0
(3)由實驗1能得出“與水接觸是鐵生銹的條件之一”的結論,依據的現象是。
(4)實驗2的①中200s時氧氣濃度沒有發生變化的原因是。
(5)由實驗2得出“食鹽能加速鐵生銹”的結論,依據的實驗是(填序號)。
(6)實驗2中,設計②③的目的是。
任務三:了解防止鐵生銹的方法
【實踐積累】
(7)同學們通過實際觀察、查閱資料,了解了自行車常用的防銹方法。請選擇你知道的自行車構件(支架、鏈條、輪圈、車把等),說明其防銹方法:(至少寫兩種方法)。組卷:68引用:1難度:0.5 -
28.市場上常見的蘇打水有蘇打氣泡水和無氣蘇打水兩種。它們的主要成分中都含有碳酸氫鈉,俗稱小蘇打。小明同學對碳酸氫鈉產生了興趣,于是對其性質進行了探究。
【查閱資料】①碳酸氫鈉的溶解度如表。
②碳酸氫鈉固體在潮濕的空氣中久置或受熱(50℃以上)就分解生成Na2CO3、H2O和CO2。溫度 10℃ 20℃ 30℃ 40℃ 溶解度 8.1g 9.6g 11.1g 12.7g
③碳酸氫鈉在270℃左右就能完全分解而碳酸鈉受熱不分解。
④很多濃酸稀釋過程中都伴隨著放熱過程。
探究1:NaHCO3溶液與鹽酸反應的熱效應
室溫下(20℃),邊攪拌邊向盛有0.5gNaHCO3固體的燒杯中加入10mL水。溶解后測得溫度為18.5℃;恢復至室溫后,向燒杯中加入過量10mL質量分數為20%的鹽酸(20℃),攪拌測溫,測得溫度為20.8℃。
(1)實驗中配制的NaHCO3溶液(填“是”或“不是”)飽和溶液。
(2)由上述實驗可知:NaHCO3固體溶于水(填“放熱”或“吸熱”)。有同學認為由上述實驗得出NaHCO3溶液與鹽酸反應放熱的結論并不可靠,理由是。
探究2:久置的NaHCO3樣品中NaHCO3含量的測定
在下列裝置B中放入久置于潮濕空氣中的(假設只有NaHCO3和Na2CO3)樣品(各裝置中氣體吸收劑足量)。
【實驗步驟】
①;
②稱取樣品20g,加到裝置B中;
③稱量裝置B、D的質量(含藥品);
④連接裝置;
⑤加熱;
⑥停止加熱繼續通入空氣;
⑦再次稱量裝置B、D的質量(含藥品)。
【數據記錄】
【問題討論】裝置B 裝置D 實驗前物質的質量/g 200.0 120.0 實驗后物質的質量/g 196.9 122.2
(3)請完善【實驗步驟】①。
(4)A裝置的作用是。
(5)寫出裝置A中可能發生的化學反應方程式:。
【數據分析】
(6)選擇表中合適的數據計算樣品中NaHCO3的質量分數。(寫出計算過程)
【拓展應用】
(7)固體Na2CO3中混有少量NaHCO3,可通過的方法除去。組卷:24引用:1難度:0.4


