2018-2019學年四川省成都市龍泉中學高三(上)入學化學試卷
發布:2025/1/3 3:0:2
一、選擇題
-
1.下列說法不正確的是( )
A.石英是制造光導纖維的原料,也是常用的半導體材料 B.氧化鋁是冶煉金屬鋁的原料,也是較好的耐火材料 C.天然氨基酸能溶于強堿或強酸溶液,是兩性化合物 D.船舶外殼裝上鋅塊,是犧牲陽極的陰極保護法進行防腐 組卷:29引用:3難度:0.9 -
2.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.標準狀況下,4.48L Cl2溶于水所得氯水中含氯的微粒總數為0.4NA B.5.6g乙烯和環丁烷(C4H8)的混合氣體中含的碳原子數為0.4NA C.常溫下,pH=2的鹽酸溶液中含有的H+數目為0.02NA D.常溫下,1L 0.5mol/L的FeCl3溶液中,所含Fe3+數為0.5NA 組卷:106引用:2難度:0.9 -
3.有機物X的蒸氣相對氫氣的密度為51,X中氧元素的質量分數為31.7%,則能在堿性溶液中發生反應的X的同分異構體有(不考慮立體異構)( )
A.15種 B.14種 C.13種 D.12種 組卷:83引用:15難度:0.7
二、非選擇題
-
10.過氧化鈣(CaO2)是一種白色晶體,無臭無味,能潮解,難溶于水,可與水緩慢反應;不溶于醇類、乙醚等,易與酸反應,常用作殺菌劑、防腐劑等。通常利用CaCl2在堿性條件下與H2O2反應制得。某化學興趣小組在實驗室制備CaO2的實驗方案和裝置示意圖(圖一)如下:
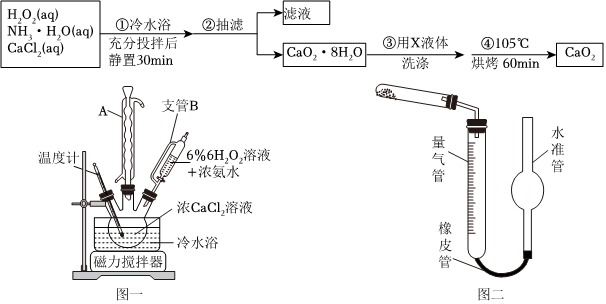
請回答下列問題:
(1)三頸燒瓶中發生的主要反應的化學方程式為:;
(2)儀器A的名稱,三頸燒瓶右口連接的是恒壓分液漏斗,其支管B的作用是;
(3)步驟③中洗滌CaO2?8H2O的液體X的最佳選擇是(填寫正確答案的序號,下同)
A.無水乙醇B.濃鹽酸C.水D.CaCl2溶液
(4)過氧化鈣可用于長途運輸魚苗,這利用了過氧化鈣以下哪些性質;
A.可緩慢供氧B.能吸收魚苗呼出的CO2氣體C.能潮解D.可抑菌
(5)已知CaO2在350℃時能迅速分解,生成CaO和O2.該小組采用如圖二所示的裝置測定剛才制備的產品中CaO2的純度(設雜質不分解產生氣體),準確稱取1.000g樣品,置于試管中加熱使其完全分解,收集到67.20mL(已換算為標準狀況)氣體,則產品中過氧化鈣的質量分數為(保留4位有效數字);組卷:6引用:1難度:0.5 -
11.堿式碳酸銅[Cu2(OH)2CO3]是一種用途廣泛的化工原料。工業上可用電子工業中刻蝕線路板的酸性廢液(主要成分有FeCl3、CuCl2、FeCl2)制備,其制備過程如圖:
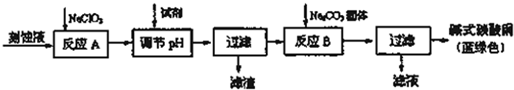
查閱資料知,通過調節溶液的酸堿性可使Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
(1)氯酸鈉的作用是物質 Cu(OH)2 Fe(OH)2 Fe(OH)3 開始沉淀pH 6.0 7.5 1,4 沉淀完全pH 13 14 3.7 ;
(2)調節溶液A的pH范圍為,可以選擇的試劑是。(填序號)。
a.氨水 b.硫酸銅 c.氫氧化銅 d.碳酸銅
(3)反應B的溫度要控制在60℃左右,且保持恒溫,可采用的加熱方法是。
(4)已知濾液中含有碳酸氫鈉,寫出生成堿式碳酸銅的離子方程式:。
(5)過濾得到的產品洗滌時,如何判斷產品已經洗凈。組卷:19引用:8難度:0.5


