2021-2022學(xué)年安徽省江淮十校高三(上)第一次聯(lián)考化學(xué)試卷
發(fā)布:2024/11/5 16:0:2
一、選擇題(本大題共16小題,每小題3分,共48分。每小題只有一項符合題目要求。)
-
1.我國力爭在2030年前碳達峰,2060年前實現(xiàn)碳中和。化學(xué)在致力“碳達峰、碳中和”方面發(fā)揮著巨大作用。下列措施不利于實現(xiàn)上述目標(biāo)的是( )
A.燃油汽車使用尾氣催化轉(zhuǎn)化裝置 B.汽油中添加乙醇 C.“禁塑令”頒布有利于減少CO2排放 D.加強新能源汽車推廣使用 組卷:12引用:3難度:0.6 -
2.化學(xué)與生活、生產(chǎn)、科技密切相關(guān)。下列說法正確的是( )
A.新冠病毒使用雙氧水與醫(yī)用酒精混合消毒,其消毒效果更佳 B.嫦娥五號登月采集的樣本中含有3He,3He與3H互為同位素 C.“凡酸壞之酒,皆可蒸燒”中涉及蒸餾操作 D.古代的鎏金工藝?yán)昧穗娊庠?/label> 組卷:19引用:1難度:0.6 -
3.《中國詩詞大會》以“賞中華詩詞、尋文化基因、品生活之美”,不僅弘揚了中國傳統(tǒng)文化,還蘊含著許多化學(xué)知識。下列詩詞分析不正確的是( )
A.“嫘祖栽桑蠶吐絲,抽絲織作繡神奇”中的“絲”不耐酸堿 B.“煮豆燃豆莢,豆在釜中泣”中的能量變化主要是化學(xué)能轉(zhuǎn)化為熱能 C.“愿滴無聲入水驚,如煙裊裊幻形生”中的“墨滴”具有膠體的性質(zhì) D.“獨憶飛絮鵝毛下,非復(fù)青絲馬尾垂”中的飛絮、鵝毛主要成分都是蛋白質(zhì) 組卷:4引用:1難度:0.7 -
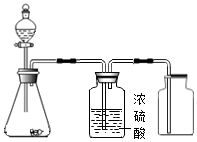 4.在實驗室采用如圖裝置制備氣體(不考慮尾氣處理),不合理的是( )
4.在實驗室采用如圖裝置制備氣體(不考慮尾氣處理),不合理的是( )A.NO B.SO2 C.O2 D.Cl2 組卷:6引用:2難度:0.8 -
5.用NA表示阿伏加德羅常數(shù)的值,下列說法中正確的是( )
A.12.0g熔融的NaHSO4中含有的陽離子數(shù)為0.2NA B.常溫常壓下,1.7g甲基(-14CH3)中所含的中子數(shù)為0.9NA C.7.8g苯中含有的碳碳雙鍵數(shù)目為0.3NA D.常溫常壓下,92g的NO2和N2O4混合氣體含有的原子數(shù)為6NA 組卷:7引用:1難度:0.7 -
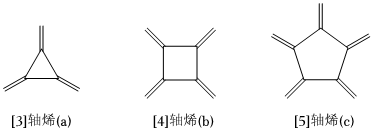 6.軸烯(Radialene)是獨特的環(huán)狀烯烴,環(huán)上每個碳原子都接有一個雙鍵,含n元環(huán)的軸烯可以表示為[n]軸烯,如下圖是三種簡單的軸烯。下列有關(guān)說法正確的是( )
6.軸烯(Radialene)是獨特的環(huán)狀烯烴,環(huán)上每個碳原子都接有一個雙鍵,含n元環(huán)的軸烯可以表示為[n]軸烯,如下圖是三種簡單的軸烯。下列有關(guān)說法正確的是( )A.軸烯的通式可表示為CnHn B.a(chǎn)分子中所有原子都在同一個平面上 C.b與苯互為同系物 D.c能使酸性KMnO4溶液褪色,發(fā)生加成反應(yīng) 組卷:13引用:1難度:0.7 -
7.用下列實驗裝置能達到相關(guān)實驗?zāi)康牡氖牵ā 。?br />
A B C D 實驗裝置 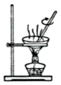
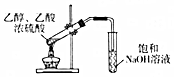
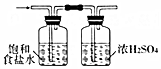
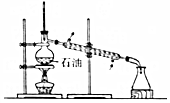
實驗?zāi)康?/td> 由CuSO4溶液制取膽礬 制備乙酸乙酯 除去CO2氣體中混有的HCl雜質(zhì) 石油分餾制備汽油 A.A B.B C.C D.D 組卷:6引用:1難度:0.5
二、填空題(本大題有5小題,共52分)
-
20.鉬酸鈉晶體(Na2MoO4?2H2O)是一種金屬腐蝕抑制劑。如圖是利用鉬精礦(主要成分是MaS2,含少量PbS等)為原料生產(chǎn)鉬酸鈉晶體的工藝流程圖。
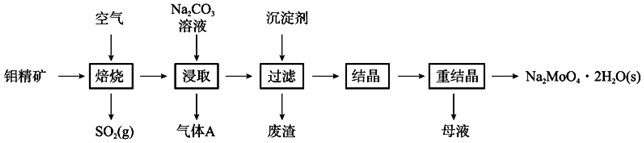
(1)Na2MoO4?2H2O中鉬元素的化合價是。
(2)“浸取”時得到的氣體A的電子式為;MoO3與Na2CO3發(fā)生反應(yīng)的離子方程式為。
(3)向濾液中加入沉淀劑Ba(OH)2固體以除去。若濾液中c(CO2-3)=0.40mol?L-1,c(MoO2-4)=0.10mol?L-1,當(dāng)BaMoO4開始沉淀時CO2-3的去除率是CO2-3%[已知:Ksp(BaCO3)=1×10-9,Ksp(BaMoO4)=4.0×10-8]。
(4)鉬酸鈉和月桂酰肌氨酸的混合液常作為碳素鋼的緩蝕劑。常溫下,碳素鋼在三種不同介質(zhì)中的腐蝕速率實驗結(jié)果如圖所示: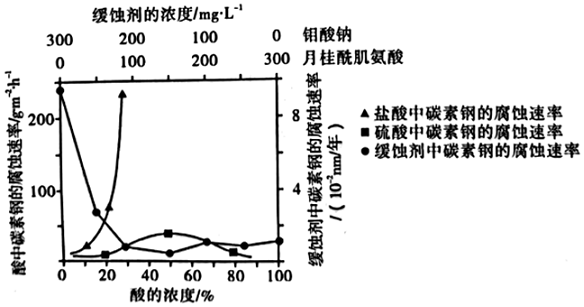
①要使碳素鋼的緩蝕效果最優(yōu),鉬酸鈉和月桂酰肌氨酸的濃度比應(yīng)為。
②碳鋼在鹽酸中的腐蝕速率比硫酸快得多,其原因可能是;硫酸濃度大于50%,碳鋼的腐蝕速率下降,原因可能是。組卷:4引用:1難度:0.5 -
21.2021年6月17日我國自主研發(fā)的神舟十二號飛船進入太空,改進型火箭推進劑之一為無色氣體N2O4。已知NO2和N2O4的結(jié)構(gòu)式分別是
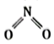 和
和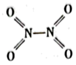 。實驗測得N-N鍵的鍵能為167KJ?mol-1,NO2中氮氧鍵的鍵能為466KJ?mol-1,N2O4中氮氧鍵的鍵能為438.5KJ?mol-1。
。實驗測得N-N鍵的鍵能為167KJ?mol-1,NO2中氮氧鍵的鍵能為466KJ?mol-1,N2O4中氮氧鍵的鍵能為438.5KJ?mol-1。
(1)寫出N2O4轉(zhuǎn)化為NO2的熱化學(xué)方程式。
(2)在100℃時,將0.40mol的NO2氣體充入2L的密閉容器中,每隔一定時間就對該容器內(nèi)的物質(zhì)進行分析,得到下表所示數(shù)據(jù)。
平衡常數(shù)K可用反應(yīng)體系中氣體物質(zhì)分壓表示(即Kp),表達式中用平衡分壓代替平衡濃度,分壓=總壓×物質(zhì)的量分?jǐn)?shù)[例如:p(NO2)=p總×x(NO2)]。設(shè)反應(yīng)開始時體系壓強為P0,反應(yīng)N2O4?2NO2,平衡時各組分壓強關(guān)系表達的平衡常數(shù)Kp=時間/s 0 20 40 60 80 n(NO2/mol) 0.40 n1 0.26 n3 n4 n(N2O4/mol) 0.00 0.05 n2 0.08 0.08 ,則Kp=[p(NO2)]2p(N2O4);20~40s內(nèi),NO2的平均反應(yīng)速率為mol?L-1?h-1。
(3)反應(yīng)N2O4(g)?2NO2(g),一定條件下N2O4與NO2的消耗速率與自身壓強間存在:v(N2O4)=k1-p(N2O4),v(NO2)=k2-[p(NO2)]2。其中k1、k2是與反應(yīng)及溫度有關(guān)的常數(shù)。一定溫度下,k1、k2與平衡常數(shù)Kp的關(guān)系是k2=。
(4)將一定量的NO2充入注射器中后封口,如圖是在拉伸或壓縮注射器的過程中氣體透光率隨時間的變化(氣體顏色越深,透光率越小)。下列說法正確的是。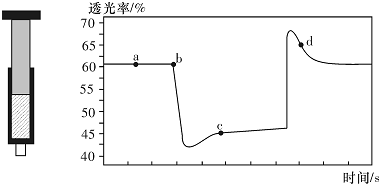
A.d點:v(正)>v(逆)
B.b點的操作是壓縮注射器
C.c點與a點相比,c(NO2)增大,c(N2O4)減小
D.若不忽略體系溫度變化,且沒有能量損失,則b、c兩點的平衡常數(shù)Kb>Kc組卷:5引用:1難度:0.6


