2023年四川省成都市青羊區中考化學二模試卷
發布:2024/4/20 14:35:0
一、(本題包括15個小題,每小題3分,共45分。每小題只有一個選項符合題意。)
-
1.四川省三星堆遺址出土了大量精美青銅器,青銅是金屬冶鑄史上最早出現的合金,與純銅相比,其強度高、熔點低、鑄造性好、耐磨、耐腐蝕。其中屬于青銅的化學性質的是( )
A.強度高 B.熔點低 C.耐磨 D.耐腐蝕 組卷:211引用:3難度:0.7 -
2.讓“綠色大運”成為成都大運會閃亮的底色。下列行為不符合該理念的是( )
A.倡導綠色出行,大力發展公共交通 B.倡導低碳辦公,盡量使用自然光源 C.倡導清潔能源,禁止使用化石燃料 D.倡導垃圾分類,綜合利用生活資源 組卷:34引用:3難度:0.7 -
3.化學與人體健康息息相關。下列說法正確的是( )
A.合理添加食品添加劑,可改善食品的品質 B.為增強身體免疫力,只吃肉類不吃蔬菜 C.奶茶具有良好口感,可取代水長期飲用 D.霉變大米含有黃曲霉素,煮熟仍可食用 組卷:55引用:4難度:0.7 -
4.合理使用化肥有利于提高農作物產量。下列化肥中,從外觀即可與其他化肥相區別的是( )
A.氯化銨 B.硫酸鉀 C.尿素 D.磷礦粉 組卷:116引用:3難度:0.9 -
5.分類法在日常生活和科學研究中具有廣泛的運用。下列物質中,屬于氧化物的是( )
A.Fe3O4 B.O2 C.K2MnO4 D.H2SO4 組卷:29引用:4難度:0.8 -
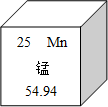 6.北京大學生命科學學院蔣爭凡教授研究組發現,錳離子是細胞內天然免疫激活劑和警報素。在元素周期表中錳元素的某些信息如圖所示,下列有關錳的說法不正確的是( )
6.北京大學生命科學學院蔣爭凡教授研究組發現,錳離子是細胞內天然免疫激活劑和警報素。在元素周期表中錳元素的某些信息如圖所示,下列有關錳的說法不正確的是( )A.屬于金屬元素 B.原子核內有25個質子 C.中子數為25 D.相對原子質量為54.94 組卷:64引用:2難度:0.9
四、(本題包含2個小題,共23分)
-
19.Ⅰ.某太陽能技術研究所利用太陽能聚光器獲得高能量太陽能,設計了熱化學循環反應兩步制取H2,其流程如圖所示。
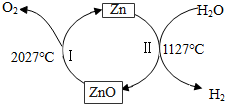
(1)反應Ⅰ的基本反應類型為反應。
(2)反應Ⅱ中涉及到化合價改變的元素有。
Ⅱ.從海水中提取鎂、制“堿”,都體現了人類改造物質的智慧。結合以下流程圖(部分操作和條件已略去),回答相關問題: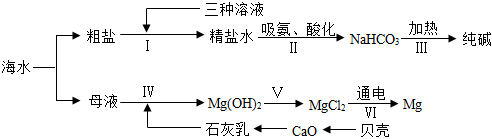
【查閱資料】常溫下,幾種物質在水中的溶解度(單位:g)
(3)粗鹽中含有氯化鎂、硫酸鈉、氯化鈣等可溶性雜質,通過步驟Ⅰ加入三種溶液充分反應后過濾,再加入適量稀鹽酸進行除雜。步驟Ⅰ加入下列三種溶液的先后順序為NaCl NH4Cl NaHCO3 36.0 37.2 9.6 (填字母序號)。
a.稍過量的Na2CO3溶液
b.稍過量的BaCl2溶液
c.稍過量的NaOH溶液
(4)母液中有MgCl2,卻經歷了步驟Ⅳ、Ⅴ的轉化過程,其目的是。
(5)步驟Ⅱ的反應方程式為NH3+NaCl+H2O+CO2=NaHCO3↓+NH4Cl,該過程有NaHCO3晶體析出,而沒有氯化鈉和氯化銨析出的原因是,該過程得到的副產品屬于肥;
(6)步驟Ⅴ反應的化學方程式為,基本反應類型是反應;
(7)由CaO制得石灰乳的化學方程式為,步驟Ⅳ用石灰乳而不用石灰水的原因是。組卷:90引用:2難度:0.5
五、(本題只有1個小題,共13分)
-
20.過氧化鈣(CaO2)一種緩釋型增氧劑,可用于魚塘增氧、農作物栽培、污水處理等方面。
【查閱資料】過氧化鈣在與水反應緩慢釋氧時,另一種生成物可吸收CO2;
Ⅰ.過氧化鈣性質的研究
(1)取少量過氧化鈣放入試管中,加足量水,產生氣泡,將帶火星的木條伸進試管中,觀察到帶火星的木條復燃,說明有生成;
(2)對實驗(1)所得渾濁液,進行如下探究:取少量渾濁液于圖1的瓶中,先開啟二氧化碳傳感器測裝置內二氧化碳的體積分數,然后用注射器注入足量稀鹽酸。觀察到白色渾濁消失,二氧化碳含量隨時間的變化如圖2所示。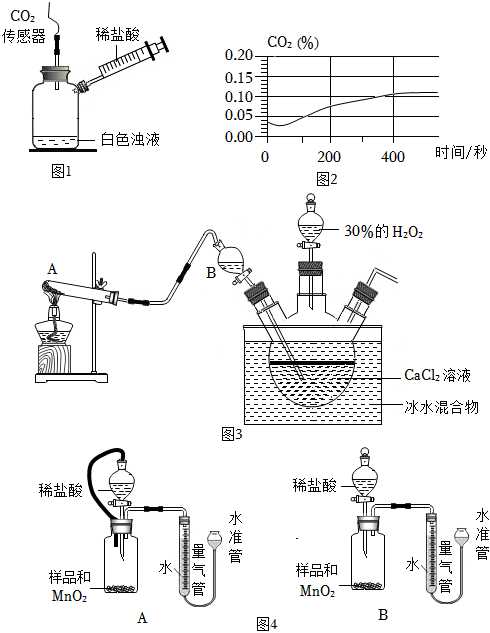
依據實驗現象及曲線,分析二氧化碳含量變化的原因(用化學方程式表示);
(3)檢查圖1裝置氣密性的方法為。
Ⅱ.制備過氧化鈣
【查閱資料】①過氧化氫受熱易分解;②氨氣極易溶于水,并與水反應,形成氨水。
以氨氣、雙氧水、氯化鈣為原料,可制得CaO2?8H2O沉淀,反應裝置如圖3所示:
(4)圖3裝置A加熱熟石灰和硫酸銨制得氨氣,氨氣溶于水形成氨水,通過分液漏斗注入三頸燒瓶。相比直接向三頸燒瓶溶液中通入氨氣,利用分液漏斗注入氨水的優點是。
(5)制取CaO2?8H2O的化學方程式為CaCl2+H2O2+2NH3?H2O+6H2O=CaO2?8H2O+2Y,則Y的化學式為;該反應溫度不能過高的原因是:①防止氨水揮發,②。
Ⅲ.測定過氧化鈣樣品純度
【查閱資料】1.過氧化鈣易與酸反應:2CaO2+4HCl=2CaCl2+2H2O+O2↑;
2.過氧化鈣樣品中其他雜質不與鹽酸反應生成氣體。
該小組取樣品2.0g,設計如圖4所示裝置,通過測定O2體積,計算樣品中CaO2的質量分數。
(6)相同條件下,(填“裝置A”或“裝置B”)能使測定結果更準確;原因是。
(7)具體實驗步驟如下:
a.連接裝置并檢查氣密性;
b.稱量樣品的質量2.0g;
c.裝藥品,調節量氣裝置兩邊液面相平,讀取量氣管刻度為10mL;
d.向廣口瓶內加入稀鹽酸,充分反應;
e.冷卻至室溫;
f.再次調節量氣裝置兩邊液面相平,讀取量氣管刻度為234mL。
步驟f中將量氣裝置兩邊液面調平的原因是。
(8)實驗狀況下,每32gO2體積為22.4L,依據實驗計算得到樣品中過氧化鈣含量為;若其他操作均正確,下列因素可使測定結果偏小的是(填序號)。
a.廣口瓶中殘留少量O2
b.烘干時溫度過高,生成了部分CaO
c.稀鹽酸的用量不足
d.步驟f中沒有調節量氣裝置兩邊液面相平,直接讀數
【反思】
(9)結合以上探究可知,保存過氧化鈣的注意事項是。組卷:121引用:2難度:0.4


