2020-2021學年黑龍江省大慶中學高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、單選題(每題3分,共54分,每小題只有一個正確選項)
-
1.如表中對SO2性質的相關實驗現象的描述或所做的解釋錯誤的是( )
選項 實驗現象 解釋 A 酸性KMnO4溶液褪色 SO2具有還原性 B Na2S溶液變渾濁 SO2與Na2S溶液反應產生了S單質 C BaCl2溶液變渾濁 SO2與BaCl2溶液反應產生了BaSO3沉淀 D 品紅溶液褪色 SO2具有漂白性 A.A B.B C.C D.D 組卷:9引用:1難度:0.7 -
2.下列敘述正確的是( )
A.濃硫酸是一種干燥劑,不能用來干燥SO2氣體 B.在蔗糖中加入濃硫酸后攪拌,蔗糖變黑、體積膨脹、并放出有刺激性氣味的氣體,只體現了濃硫酸的脫水性 C.硫酸與鐵反應時,生成物與反應條件、酸的濃度、反應物的用量等有關 D.把足量銅粉投入含2molH2SO4的濃硫酸中,反應后得到標準狀況下氣體體積為22.4L 組卷:2引用:1難度:0.8 -
3.下列離子方程式中,正確的是( )
A.NH4Cl溶液與濃NaOH溶液共熱:NH4++OH- NH3↑+H2O加熱B.銅與稀硝酸的反應:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O C.用NaOH溶液吸收過量SO2:SO2+2OH-=SO32-+H2O D.向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O 組卷:6引用:1難度:0.7 -
4.下列關于氨及其化合物的說法不正確的是( )
A.NH3極易溶于水 B.常溫下,濃硝酸不能用鐵制容器盛裝 C.N2的化學性質穩定,可用作保護氣 D.NO、NO2均為大氣污染物 組卷:3引用:1難度:0.7 -
5.隨著科學技術的發展,無機非金屬材料突破了傳統硅酸鹽體系的界限,一系列新型無機非金屬材料相繼問世。下列有關硅及其化合物的說法中不正確的是( )
A.高溫結構陶瓷具有耐高溫、耐腐蝕、抗氧化等優良性能 B.二氧化硅常用于制作光導纖維 C.水泥、玻璃、水晶飾物都是硅酸鹽制品 D.硅晶片是生產芯片的基礎材料 組卷:9引用:2難度:0.6 -
6.原電池構成是有條件的,關于如圖所示裝置的敘述,錯誤的是( )
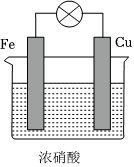
A.Cu是負極,其質量逐漸減小 B.H+向鐵電極移動 C.Cu片上有紅棕色氣體產生 D.Fe電極上發生還原反應 組卷:29引用:3難度:0.7 -
7.電池是人類生產和生活中的重要能量來源,各式各樣的電池的發明是化學對人類的一項重要貢獻。下列有關電池的敘述中正確的是( )
A.鋅錳干電池是一次電池,工作一段時間后正極碳棒變細 B.氫氧燃料電池工作時氫氣在正極被氧化 C.燃料電池可將熱能直接轉化為電能,故能量轉化率高 D.鉛酸蓄電池是充電電池,充電時是使放電時的氧化還原反應逆向進行 組卷:3引用:2難度:0.7
二、非選擇題(共46分)
-
22.如表是研究性學習小組研究影響過氧化氫(H2O2)分解速率的因素時采集的一組數據:用10mL H2O2溶液制取150mL氧氣所需的時間(單位:s)
請回答下列問題:
濃 度
反應條件30% H2O2 15% H2O2 10% H2O2 5% H2O2 無催化劑、不加熱 幾乎不反應 幾乎不反應 幾乎不反應 幾乎不反應 無催化劑、加 熱 360 480 540 720 MnO2催化劑、加熱 10 25 60 120
(1)該研究小組在設計方案時,考慮了濃度、、等反應條件對過氧化氫分解速率的影響.
(2)從上述影響過氧化氫分解速率的三個因素說明這些因素對分解速率有何影響?;;.組卷:38引用:6難度:0.5 -
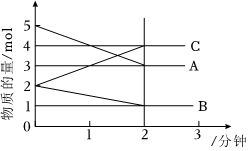 23.某反應在體積為5L的恒溫恒容密閉容器中進行,各物質的量隨時間的變化情況如圖所示(已知A、B、C均為氣體,A氣體有顏色)。
23.某反應在體積為5L的恒溫恒容密閉容器中進行,各物質的量隨時間的變化情況如圖所示(已知A、B、C均為氣體,A氣體有顏色)。
(1)該反應的化學方程式為。
(2)反應開始至2分鐘時,B的平均反應速率為。
(3)能說明該反應已達到平衡狀態的是。
A.容器內氣體的顏色保持不變
B.容器內氣體密度不變
C.v逆(A)=v正(C)
D.各組分的物質的量相等
E.混合氣體的平均相對分子質量不再改變的狀態
(4)由圖求得平衡時A的轉化率為。
(5)平衡時體系內的壓強是初始時倍。組卷:4引用:2難度:0.6


