2020-2021學年遼寧省實驗中學等五校協作體高一(下)期末化學試卷
發布:2024/12/22 16:0:2
一、選擇題(每題只有一個正確選項,每小題3分,共45分)
-
1.5月15日,天問一號著陸巡視器在火星著陸,中國首次火星探測任務取得圓滿成功。下列說法不正確的是( )
A.長征五號遙四運載火箭燃料使用的液氫是高能清潔燃料 B.“祝融號”火星車使用的太陽能電池板可以將化學能轉化為電能 C.巡航器用到碳纖維復合材料,主要利用其質輕、強度大和耐高溫性能 D.火星表面呈紅色,主要是由于火星土壤中含有Fe2O3 組卷:15引用:2難度:0.8 -
2.化學與生產、生活、科技等密切相關。下列說法正確的是( )
A.蔗糖、淀粉、纖維素在人體內水解最終產物都是葡萄糖,是人類重要的營養物質 B.水果罐頭中添加的維生素C主要用作營養強化劑 C.綠色化學的核心是應用化學原理和技術手段,減少或消除產品在生產和應用中涉及到的有害化學物質 D.冶煉鋁:鋁土礦 NaAlO2過量NaOH(aq)無水AlCl3過量HCl(aq)Al電解組卷:23引用:2難度:0.9 -
3.化學用語是表示物質組成、結構和變化規律的一種具有國際性、科學性和規范性的書面語言,下列化學用語表達正確的是( )
A.1-丁烯的鍵線式 
B.羧基的結構式-COOH C.羥基的電子式 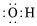
D.乙酸的球棍模型 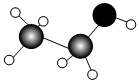 組卷:24引用:2難度:0.7
組卷:24引用:2難度:0.7 -
4.設NA為阿伏加德羅常數的數值。下列說法正確的是( )
A.2.8gFe與足量稀硝酸反應,轉移的電子數為0.1NA B.等質量(17g)的-OH和OHˉ所含的電子數均為9NA C.32g硫粉在氧氣中充分燃燒得到NA個SO3分子 D.28g乙烯所含共用電子對數目為6NA 組卷:22引用:2難度:0.9 -
5.已知可逆反應2A(s)+3B(g)?C(g)+2D(g)為放熱反應,下列有關敘述正確的是( )
①增加A的用量,v(正)增大。
②增大C的濃度,v(逆)增大,v(正)減小。
③體積縮小一倍,v(正)、v(逆)都增大。
④2molA和3molB的總能量大于1molC和2molD的總能量。
⑤若單位時間內消耗2molA同時生成1molC,說明反應已達平衡。A.③④ B.①② C.①④ D.④⑤ 組卷:34引用:2難度:0.6 -
6.下列敘述不正確的是( )
A.油脂在酸性或堿性條件下均可以水解 B.等質量的物質完全燃燒耗氧量:甲烷>乙烷>乙烯>苯 C.沸點:己烷>戊烷>2-甲基丁烷>丁烷>乙醇 D.甲醛HCHO、乙酸和丙醛組成的混合物中,氧元素的質量分數是37%,則碳元素的質量分數為54% 組卷:24引用:2難度:0.7
二、填空題
-
18.研究小組設計如圖1實驗(夾持裝置已略去)分別探究NO與銅粉、Na2O2 的反應
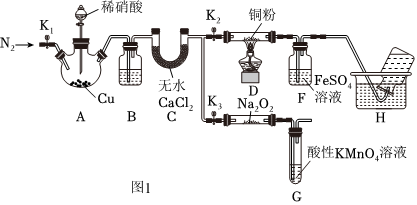
已知:①NO與Na2O2可發生反應:2NO+Na2O2═2NaNO2
②NO能被酸性高錳酸鉀溶液氧化為NO-3
③溶液中存在平衡FeSO4+NO?Fe(NO)SO4(棕色)
Ⅰ.關閉K3,打開K2,探究NO與銅粉的反應并檢驗NO。
(1)反應開始前,打開K1,通入一段時間N2,其目的是。
(2)裝置B中盛放的試劑為水,其作用是。
(3)裝置F中的實驗現象為。裝置H中收集的氣體為(填化學式)。
Ⅱ.關閉K2,打開K3,探究NO與Na2O2的反應并制備NaNO2.
(1)裝置G的作用是。
(2)若省略裝置C,則進入裝置G中的氣體除N2、NO外,可能還有(填化學式)。
Ⅲ.細菌可以促使鐵、氮兩種元素進行氧化還原反應,并耦合兩種元素的循環。耦合循環中的部分轉化如圖2所示。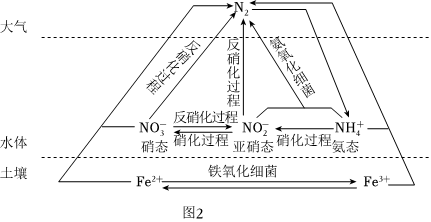
(1)圖所示氮循環中,屬于氮的固定的有(填字母序號)。
a.N2轉化為氨態氮
b.硝化過程
c.反硝化過程
(2)土壤中的鐵循環可用于水體脫氮(脫氮是指將氮元素從水體中除去),結合圖中的轉化,土壤中的鐵循環脫除水體中氨態氮和硝態氮的原理用離子方程式表示如下:6Fe3++2═6Fe2++N2↑+8H+和NH+4。組卷:26引用:1難度:0.6 -
 19.(1)亞硝酰氯(CINO)是有機合成中常用試劑。
19.(1)亞硝酰氯(CINO)是有機合成中常用試劑。
已知2NO(g)+Cl2(g)?2ClNO(g)為放熱反應,恒溫恒容條件下,將6molNO與3molCl2發生反應,下列可判斷反應達平衡狀態的是(填序號字母)
A.混合氣體的平均相對分子質量不變
B.混合氣體密度保持不變
C.NO和Cl2的物質的量之比保持不變
D.混合氣體體積保持不變
E.混合氣體顏色不再改變
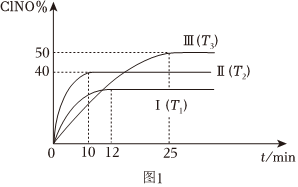
(2)在一恒容的體積為10L的密閉容器中充入3molNO和2molCl2,在不同溫度下發生反應2NO(g)+Cl2(g)?2ClNO(g),ClNO的百分含量隨時間的變化如圖1所示。已知:T1>T2>T3
①與實驗Ⅰ相比,實驗Ⅱ除溫度不同外,還改變的條件是;
②實驗Ⅱ反應至10min達到平衡,此時Cl2的轉化率為。(保留1位小數)
③實驗Ⅲ反應至25min達到平衡,用NO物質的濃度變化表示的反應速率為。
(3)常溫下,將除去表面氧化膜的Al、Cu片插入濃HNO3中組成原電池(如圖2),測得原電池的電流強度(I)隨時間(t)的變化如圖3所示,已知0~t1時,原電池的負極是Al片,反應過程中有紅棕色氣體產生。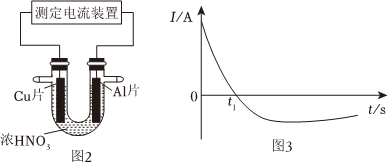
①0~t1時,正極的電極反應式為;溶液中的H+向電極移動(填寫Cu或Al)。
②t1時,原電池中電流方向發生改變是因為。組卷:28引用:1難度:0.5


