2020-2021學年江蘇省無錫市新吳區九年級(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括15小題,每小題1分,共15分。每小題只有一個選項符合題意。)
-
1.“碧水千河揚長帆,藍天白云飄紙鳶”。無錫人民正在積極建設“碧水藍天”的生態城市,下列措施中不合理的是( )
A.限制化學工業發展,關停所有化工企業,消除污染源頭 B.積極推廣太陽能、風能等新能源,減少化石燃料的使用 C.加強城市生活污水脫氮除磷處理,遏制水體的富營養化 D.禁止露天焚燒秸稈,推廣秸稈沼氣、發電、制酒精技術 組卷:8引用:2難度:0.7 -
2.合成材料的應用與發展,大大方便了人類的生活。下列屬于合成材料的是( )
A.鋁合金 B.玻璃鋼 C.桑蠶絲 D.聚乙烯 組卷:36引用:1難度:0.7 -
3.生產、生活中的下列變化,屬于物理變化的是( )
A.鋼鐵生銹 B.糧食釀酒 C.酒精揮發 D.木炭燃燒 組卷:20引用:3難度:0.8 -
4.下列物質能溶于水形成溶液的是( )
A.泥土 B.食鹽 C.香油 D.硫酸鋇 組卷:33引用:1難度:0.8 -
5.下列圖示中屬于節水標志的是( )
A. 
B. 
C. 
D.  組卷:14引用:2難度:0.9
組卷:14引用:2難度:0.9 -
6.《本草綱目》中“黃連”條目下記載:“吐血不止,取黃連一兩,搗碎,加鼓二十粒,水煎去渣,溫服。”該過程中沒有涉及的操作是( )
A.加熱 B.稱量 C.過濾 D.蒸發結晶 組卷:356引用:25難度:0.5
二、解答題(共5小題,滿分35分)
-
19.二氧化氯(ClO2)是一種高效、安全的消毒劑。工業上可采用氯酸鈉(NaClO3)為原料制備,如圖是工業生產中一種以食鹽水為原料制備二氧化氯的工藝原理。
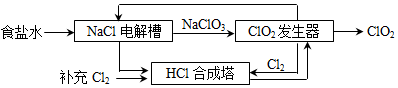
(1)NaCl電解槽:食鹽水在通電的條件下生成氫氧化鈉、氫氣和氯氣,寫出該反應的化學方程式;在加熱條件下,生成的氫氧化鈉再和氯氣反應生成NaCl、NaClO3和H2O。
(2)合成塔中發生的反應的基本類型是。
(3)二氧化氯發生器中的反應為:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2X,X為。
(4)該流程中可循環使用的物質除水以外還有。
(5)下列有關二氧化氯的說法,正確的是。
A.二氧化氯屬于氧化物
B.二氧化氯可用于飲用水的消毒殺菌
C.二氧化氯中氯元素的化合價是該流程中氯元素的最高化合價組卷:40引用:1難度:0.5 -
20.過氧化鈣(CaO2)是一種溫和的氧化劑,無毒,不污染環境。常溫下為白色固體,極易與水和二氧化碳反應。
Ⅰ.過氧化鈣的制備
(一)某實驗小組利用氧氣和鈣發生化合反應制備過氧化鈣,擬用圖1裝置進行。已知鈣是一種很活潑的金屬,常溫下極易和水反應生成氫氧化鈣和氫氣。你認為圖中裝置B的作用是。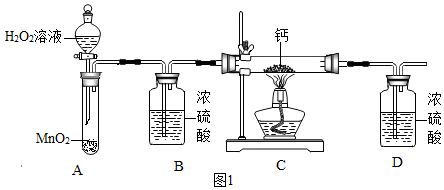
實驗步驟如下:
①檢查裝置的氣密性后,裝入藥品;
②打開分液漏斗活塞,通入一段時間氣體,加熱藥品;
③反應結束后,先熄滅酒精燈,待反應管冷卻至室溫后,停止通入氣體;
④拆除裝置,取出產物。
實驗步驟③的操作目的是。
(二)利用反應CaCl2+H2O2+2NH3+8H2O═CaO2?8H2O↓+2NH4Cl,在堿性環境下也可以制取CaO2?8H2O的裝置如圖2: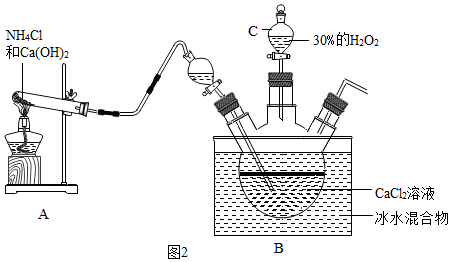
(1)反應結束后,經(填操作名稱)、洗滌、低溫烘干可獲得CaO2?8H2O。
(2)裝置A試管中反應的化學方程式為;裝置B中用冰水浴控制溫度,其可能的原因是。
Ⅱ.過氧化鈣的應用
(三)為解決魚池中氧氣不足的問題,通常向水中撒一些過氧化鈣(CaO2)。過氧化鈣與水反應的化學方程式為2CaO2+2H2O═2Ca(OH)2+O2↑。
(1)某興趣小組同學稱取7.2g過氧化鈣加入到足量的水中,計算生成氧氣的質量是多少?
(2)小組同學另取少量過氧化鈣固體于一定量的水中,一段時間后,燒杯中存在白色濁液。
【猜想】甲同學認為:白色濁液中含有CaCO3。
【實驗一】為了驗證甲同學的猜想,進行如下實驗。
取少量白色濁液于試管中,滴加稀鹽酸,白色渾濁物消失,沒有觀察到有氣泡產生。
【實驗二】為了進一步驗證甲同學的猜想,進行如圖的實驗。
【解釋與結論】實驗裝置圖 實驗操作 實驗現象 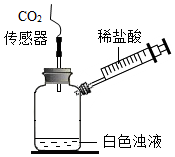
將注射器內稀鹽酸推入瓶中,并用二氧化碳傳感器測得裝置內二氧化碳的體積分數 Ⅰ.白色渾濁消失,沒有觀察到有氣泡產生
Ⅱ.檢測到二氧化碳含量隨時間的變化如圖所示
①甲同學提出白色濁液中含有CaCO3的理由是。
②由實驗二得出的結論是,相關反應的化學方程式為。組卷:68引用:1難度:0.7


