2021-2022學年吉林省長春外國語學校高二(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共16小題,每小題3分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.以下現象與原子核外電子的躍遷有關的是( )
①節日焰火
②棱鏡分光
③激光
④LED燈光
⑤凹透鏡聚光
⑥鋼鐵生銹A.①③④ B.③⑥ C.①③④⑤ D.①②③⑤⑥ 組卷:49引用:1難度:0.7 -
2.下列關于原子結構與元素周期表的說法正確的是( )
A.電負性最大的元素位于周期表的左下角 B.原子核外可能有兩個電子的運動狀態是相同的 C.2s軌道在空間呈啞鈴形 D.某基態原子的價電子排布式為4s24p1,該元素位于周期表第四周期IIIA族 組卷:79引用:1難度:0.7 -
3.根據下列五種元素的電離能數據(單位:kJ?mol-1),判斷下列說法不正確的是( )
元素代號 I1 I2 I3 I4 Q 2080 4000 6100 9400 R 500 4600 6900 9500 S 740 1500 7700 10500 T 580 1800 2700 11600 U 420 3100 4400 5900 A.元素的電負性最大的可能是Q元素 B.原子的價電子排布為ns2np1的可能是T元素 C.U元素可能在元素周期表的s區 D.R和S均可能與U在同一主族 組卷:66引用:6難度:0.7 -
4.下列說法中正確的是( )
A.1個氮氣分子中含有1個σ鍵和2個π鍵 B.N-O鍵的鍵長比C-O鍵的鍵長長 C.乙烯中碳碳雙鍵的鍵能是乙烷中碳碳單鍵的鍵能的2倍 D.NH4+中4個N-H鍵的鍵能不同 組卷:82引用:1難度:0.8 -
5.下列說法中正確的是( )
A.NCl3分子呈三角錐形,這是氮原子采取sp2雜化的結果 B.sp3雜化軌道是由任意的1個s軌道和3個p軌道混合形成的4個sp3雜化軌道 C.中心原子采取sp3雜化的分子,其空間結構可能是四面體形或三角錐形或V形 D.AB3型的分子空間結構必為平面三角形 組卷:113引用:5難度:0.6 -
6.下列“類比”結果不正確的是( )
A.CO2與Ca(ClO)2溶液反應得到HClO,則SO2與Ca(ClO)2溶液反應也得到HClO B.CO2的分子構型為直線形,則CS2的分子構型也為直線形 C.H2O2受熱分解生成H2O和O2,則H2S2受熱分解生成H2S和S D.AgCl溶解度大于AgI,則CuCl溶解度大于CuI 組卷:10引用:1難度:0.6
二、綜合填空題
-
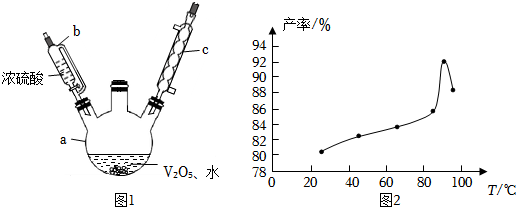
19.硫酸氧礬(VOSO4)對高血糖、高血癥等具有一定的治療作用。制備VOSO4的實驗流程及實驗裝置如圖1(夾持及加熱裝置已省略)。
V2O5+H2SO4(VO2)2SO4溶液(橙紅色)加熱VOSO4溶液(藍黑色)加草酸(H2C2O4)VOSO4晶體(純藍色)操作a
回答下列問題;
(1)儀器a的名稱為,在該儀器中發生反應生成(VO2)2SO4的化學方程式為。
(2)常溫條件下,V2O5是一種黃色固體粉末,微溶于水,溶于強酸(如硫酸,常溫下其溶解反應方程式為V2O5+4H2SO4+4H2O═V2O5?4SO3?8H2O,該反應屬于(填“氧化還原反應”或“非氧化還原反應”),在較適宜的溫度下,可減小濃硫酸的需要量,如圖2為反應溫度與產物產率間的關系,則最適宜的加熱方式為(填“直接加熱”或“水浴加熱”)。
(3)加入草酸前,反應液需充分冷卻并加適量蒸餾水稀釋的目的是;反應液由橙紅色變為藍黑色的反應的離子方程式為。組卷:4引用:1難度:0.6 -
20.氮元素是生命體核酸與蛋白質必不可少的組成元素,氮及其化合物在國民經濟中占有重要地位。

(1)氨催化氧化制得硝酸的同時,排放的氮氧化物也是環境的主要污染物之一。
已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ?mol-1
C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
2C(s)+O2(g)═2CO(g)△H3=-221kJ?mol-1
則反應2CO(g)+2NO(g)═N2(g)+2CO2(g)△H4=。
(2)在容積均為2L的三個恒容密閉容器中分別通入1molCO和1molNO,發生反應2CO(g)+2NO(g)═N2(g)+2CO2(g),a、b、c三組實驗的反應溫度分別記為Ta、Tb、Tc。恒溫恒容條件下反應各體系壓強的變化曲線如圖1所示。
①三組實驗對應溫度的大小關系是(用Ta、Tb、Tc表示),0~20min內,實驗b中v(CO2)=mol?L-1?min-1。
②實驗a條件下,反應的平衡常數K=L?mol-1。
(3)工業用鉑絲網作催化劑,溫度控制在780~840℃,將NH3轉化為NO,反應方程式為4NH3(g)+5O2(g)?4NO(g)+6H2O(g)。回答下列問題:
①NH3催化氧化速率v=k?ca(NH3)?cb(O2),k為常數。當氧氣濃度為1.0mg?L-1時,c(NH3)與速率的關系如表所示,則a=。
②其他反應條件相同時,測得不同溫度下相同時間內NH3的轉化率如圖2所示。則A點對應的反應速率v(正)c(NH3)×102/mol?L-1 0.8 1.6 3.2 6.4 v×108/mol?L-1?min-1 10.2 81.6 652.8 5222.4 (填“>”、“<”或“=”)v(逆),A、C點對應條件下,反應平衡常數較大的是(填“A”或“C”),理由是。組卷:168引用:4難度:0.5


