2022-2023學(xué)年廣東省佛山市S7(李兆基中學(xué)、鄭裕彤中學(xué)、華僑中學(xué)等)高一(下)期中化學(xué)試卷
發(fā)布:2024/11/17 2:30:2
一、選擇題:本小題包括16小題,共44分。第1~10小題,每小題2分;第11~16小題,每小題2分。在每小題給出的四個選項中,只有一項符合題目要求。
-
1.下列材料中不屬于新型無機非金屬材料的是( )
A.高溫結(jié)構(gòu)陶瓷 B.光學(xué)玻璃 C.光導(dǎo)纖維 D.碳納米管 組卷:25引用:1難度:0.5 -
2.下列物質(zhì)類別不是硫在自然界存在形態(tài)的是( )
A.單質(zhì) B.硫化物 C.亞硫酸鹽 D.硫酸鹽 組卷:38引用:1難度:0.8 -
3.下列氮的氧化物中屬于酸性氧化物的是( )
A.N2O5 B.NO2 C.NO D.N2O 組卷:77引用:1難度:0.8 -
4.下列氣體中,不能用濃硫酸干燥的是( )
A.N2 B.SO2 C.NH3 D.Cl2 組卷:12引用:2難度:0.8 -
5.常溫下,下列容器不能用于儲存濃硝酸的是( )
A.銅罐 B.鐵桶 C.鋁罐 D.塑料瓶 組卷:18引用:1難度:0.6 -
6.下列說法中錯誤的是( )
A.SO2可漂白紙漿,不可用于殺菌、消毒 B.熟石膏與水混合成糊狀后能很快凝固,常用于制作模型和醫(yī)療石膏繃帶 C.稀硫酸具有酸性,可用于除去鐵銹 D.硫酸鋇不容易被X射線透過,醫(yī)療上常用作消化系統(tǒng)X射線檢查的內(nèi)服藥劑,俗稱“鋇餐” 組卷:27引用:1難度:0.7
二、非選擇題:本題包括4小題,共56分
-
19.煤燃燒產(chǎn)生的煙氣含有SO2和NOx,石油化工生產(chǎn)過程中產(chǎn)生H2S,需采用有效措施對煙氣和生產(chǎn)過程進(jìn)行脫硫、脫硝,減少對大氣的污染。
Ⅰ.脫H2S
(1)一種脫除回收硫工藝的兩個階段主要反應(yīng)分別如下:
第一階段:2H2S(g)+3O2(g)═2SO2(g)+2H2O(g)
第二階段:4H2S(g)+2SO2(g)═3S2(g)+4H2O(g)
該工藝需控制第一階段與第二階段參加反應(yīng)的H2S的物質(zhì)的量之比約為,若該比值過大會導(dǎo)致SO2不能完全轉(zhuǎn)化為S2而污染大氣。
(2)Fe2(SO4)3溶液脫除空氣中H2S并再生的原理如圖所示。Fe2(SO4)3的作用是。
Ⅱ.脫SO2和NOx
(3)一種利用含有SO2的煙氣制備NaClO2的流程如圖:
①反應(yīng)a的化學(xué)方程式為。
②反應(yīng)b中的氧化劑和還原劑的物質(zhì)的量之比為。
(4)一種綜合處理含的廢水和工業(yè)廢氣(主要含N2、CO2、SO2、NO、CO)的流程如圖:NH+4
已知:用NaOH溶液吸收NOx,反應(yīng)原理為:2NO2+2NaOH═NaNO2+NaNO3+H2O;NO+NO2+2NaOH═2NaNO2+H2O。
①固體1的主要成分有Ca(OH)2、。
②X可以是空氣,其作用是(用化學(xué)方程式表示)。
③捕獲劑所捕獲的氣體主要是。
④處理含廢水時,發(fā)生反應(yīng)的離子方程式為NH+4。組卷:17引用:1難度:0.5 -
20.某實驗小組探究外界條件對化學(xué)反應(yīng)速率的影響,進(jìn)行了以下實驗。
Ⅰ.探究溫度、濃度對硫代硫酸鈉與稀硫酸反應(yīng)速率的影響
(1)寫出Na2S2O3與H2SO4反應(yīng)的離子方程式。
(2)該小組同學(xué)設(shè)計了如下表所示系列實驗:
實驗①和②探究溫度對該反應(yīng)速率的影響,則實驗②中,t1=實驗序號 反應(yīng)溫度/℃ Na2S2O3溶液 稀H2SO4溶液 H2O V/mL c/(mol/L) V/mL c/(mol/L) V/mL ① 20 10.0 0.10 10.0 0.50 0 ② t1 V1 0.10 V2 0.50 V3 ③ t2 V4 0.10 V5 0.50 V6 (填“20℃”或“60℃”)、V2=mL。
實驗①和③探究H2SO4濃度對該反應(yīng)速率的影響,則實驗③中,若V6=5.0mL,則V4=mL、V5=mL。
Ⅱ.探究催化劑對H2O2分解速率的影響
(3)按如圖進(jìn)行定量實驗研究。擠壓注射器使FeCl3溶液全部加入試管中,記錄數(shù)據(jù);用CuCl2溶液代替FeCl3溶液進(jìn)行平行實驗,比較催化劑對反應(yīng)速率的影響。該實驗需測定的實驗數(shù)據(jù)是。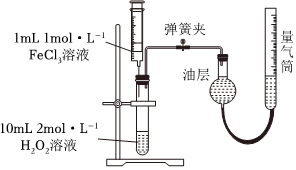
(4)用圖中的裝置,探究MnO2催化H2O2分解的最佳條件。此時注射器中應(yīng)加入的試劑是。擠壓注射器使液體全部加入試管中開始至不再有氣體產(chǎn)生,記錄反應(yīng)時間。反應(yīng)物用量和反應(yīng)時間如下表:
分析表中數(shù)據(jù),從實驗效果和“綠色化學(xué)”的角度考慮,H2O2的濃度一定時,加入MnO2
反應(yīng)時間
H2O20.1g 0.3g 0.8g 10mL1.5% 223s 67s 56s 10mL3.0% 308s 109s 98s 10mL4.5% 395s 149s 116s g的MnO2為較佳選擇。組卷:70引用:3難度:0.6


