2021-2022學年廣西南寧市賓陽中學高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共16小題,每小題3分,共48分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.2022年1月7日,PLOS Biology在線發表了關于玉米生物固氮的研究,為減少化肥使用和發展綠色農業提供重要的理論指導。下列反應中,屬于氮的固定的是( )
A.由氨制成碳酸氫銨或硫酸銨 B.NO2與H2O反應生成HNO3 C.NO和O2反應生成NO2 D.N2和H2在一定條件下合成氨 組卷:56引用:2難度:0.9 -
2.下列化學用語正確的是( )
A.四氯化碳的電子式為 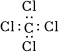
B.CO2的結構式為O=C=O C.NH4Cl的電子式: 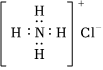
D.甲烷分子的球棍模型: 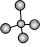 組卷:14引用:2難度:0.8
組卷:14引用:2難度:0.8 -
3.下列關于能量變化的說法正確的是( )
A.可逆反應過程中沒有能量變化 B.燒堿、生石灰溶于水時均為放熱反應 C.植物的光合作用是將太陽能轉化為化學能 D.需要加熱才能發生的反應為吸熱反應 組卷:15引用:1難度:0.7 -
4.下列關于基本營養物質的說法正確的是( )
A.所有蛋白質都可通過顏色反應來鑒別 B.油脂在酸性條件下水解為甘油和高級脂肪酸 C.糖類、蛋白質、油脂都屬于天然高分子化合物 D.糖類、油脂、蛋白質都是由C、H、O三種元素組成的 組卷:25引用:2難度:0.9 -
5.下列物質中,可用作食品抗氧化劑的是( )
A.抗壞血酸 B.硫酸鈣 C.三聚氰胺 D.碳酸鎂 組卷:23引用:2難度:0.7 -
6.下列說法正確的是( )
A.pH<7的酸性降水不一定是酸雨 B.NH4NO3是一種高效氮肥,含NH4NO3的廢水可以任意排入河流 C.綠色化學的核心思想是用化學原理和技術手段治理污染 D.焚燒并回收熱能是廢舊塑料的恰當處理途徑 組卷:23引用:2難度:0.5
二、非選擇題:本題共4小題,共52分。
-
19.為改變生橡膠受熱發粘遇冷變硬的不良性能,工業上常將橡膠硫化來改善橡膠的性能,S2Cl2和SCl2均為改善橡膠性能的重要化工產品。
I.已知下列化學鍵的鍵能及S4的結構式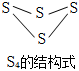
已知反應:S4(g)+4Cl2(g)═4SCl2(g)。1molS4與4molCl2完全反應可放出d kJ熱量,則b=化學鍵 S-S S-Cl Cl-Cl 鍵能/(kJ/mol) a b c (用含a,c,d的代數式表示)。
II資料卡片:
i.二氯化二硫常溫下是一種黃紅色液體,有窒息性、刺激性惡臭,熔點-80℃,沸點135.6℃;
ii.S2Cl2遇水強烈反應。
工業上可以用氯氣和硫單質反應制得S2Cl2,實驗室用下列裝置模擬工業制取少量S2Cl2。
(1)制取少量S2Cl2(必要的加熱裝置未省略)
實驗室可利用硫與少量氯氣在110~140℃反應制得S2Cl2粗品。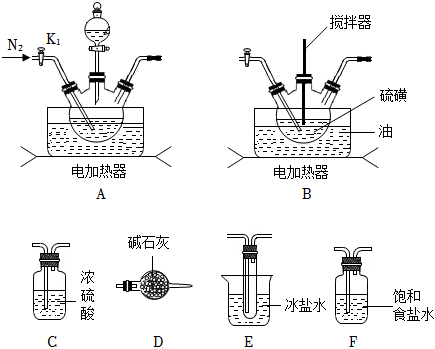
①S2Cl2的電子式是。請寫出實驗室適合A裝置制取氯氣的離子方程式;
②請補充完整實驗裝置連接順序:A→。其中,D裝置的作用是,冰鹽水的作用是。
③實驗過程中,實驗前和停止加熱后,都需通一段時間的氮氣,若停止加熱后沒有繼續通氮氣,S2Cl2的產率將(填“偏高”、“偏低”或“無影響”)。
(2)①S2Cl2遇水強烈反應,已知其中一種氣體產物X能使品紅溶液褪色,加熱后又恢復原狀,且反應過程中只有一種元素化合價發生變化,寫出該反應的化學方程式。
②假設共收集到S2Cl2和水反應生成的混合氣體VL(標準狀況),請利用下列試劑設計實驗方案測定混合氣中氣體X的體積分數:
試劑:HNO3酸化的AgNO3溶液 H2SO4酸化的KMnO4溶液 H2O2溶液 Ba(OH)2溶液實驗步驟 現象 a.取VL混合氣體,通入足量 \ b.向a中充分反應后的溶液中加入 產生白色沉淀 c. ,稱量(填必要的操作名稱)\ d.計算。白色沉淀的質量為m g,則X的體積分數為 %。\ 組卷:14引用:3難度:0.6 -
20.乳酸乙酯(F)是一種食用香料,可用淀粉為原料合成,路線如下
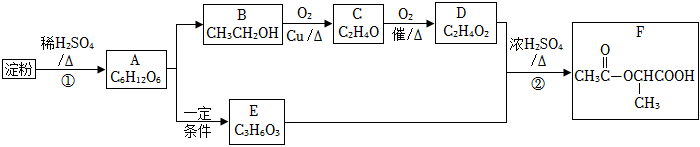
請回答:
(1)A為葡萄糖,所含官能團是、-CHO。
(2)B→C的化學反應方程式是。
(3)D具有酸性,寫出D與NaHCO3反應的化學方程式。
(4)E結構中含有—CH3,且1mol E可以與2mol Na或1mol NaOH反應。
Ⅰ.E的結構簡式為。
Ⅱ.反應②為酯化反應,寫出反應②的化學反應方程式。
(5)下列說法不正確的是。
a.淀粉分子式為(C6H10O5)n,屬于天然有機高分子
b.反應①為水解反應
c.可以用銀氨溶液鑒別C、D(必要時可以加熱)
d.D、E互為同系物
(6)檢驗淀粉在酸性條件下發生水解反應的操作:取少量冷卻后的水解液于試管中,加NaOH溶液至堿性,再加入少量(填:試劑、操作和現象),則證明淀粉已發生水解。組卷:101引用:2難度:0.5


