2022-2023學年四川省成都市樹德中學高二(上)段考化學試卷(11月份)
發布:2024/9/1 5:0:10
一、單項選擇題(1-6題每題2分,7-16題每題3分,共計42分)
-
1.化學與工農業生產、日常生活、材料等有密切的聯系,下列說法不正確的是( )
A.華為公司自主研發的“麒麟9000芯片”需要以高純度的硅為原料 B.修建“火神山”醫院所用的HDPE(高密度聚乙烯)膜是一種無毒、無味的高分子材料 C.在三星堆“祭祀坑”提取到絲綢制品殘留物,其中絲綢主要成分為纖維素 D.火炬“飛揚”在出火口格柵噴涂堿金屬,目的是利用焰色反應讓火焰可視化 組卷:2引用:1難度:0.7 -
2.有機物Z為是合成某藥物的重要中間體,可由下列反應制得。
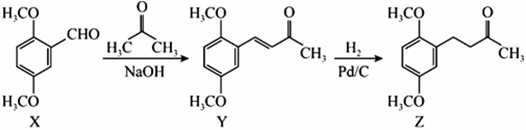
下列有關化合物X、Y和Z的說法正確的是( )A.1molX中含有3mol碳碳雙鍵 B.Y的一氯代物的同分異構體有7種 C.X生成Y的原子利用率為100% D.Z分子與足量H2加成后的產物其沸點比Z高 組卷:2引用:1難度:0.5 -
3.設NA為阿伏加德羅常數的值,下列有關敘述正確的是( )
A.25℃,pH=12的NaOH溶液中含有OH-的數目約為0.01NA B.向含1molCl-的NH4Cl溶液中加入適量氨水使溶液呈中性,此時溶液中 數目為NANH+4C.在1L0.1mol?L-1的Na2CO3溶液中,陰離子總數等于0.1NA D.標準狀況下,盛有11.2LSO3的密閉容器中硫原子數為0.5NA 組卷:1引用:1難度:0.7 -
4.一種新型漂白劑由短周期元素W、X、Y、Z組成,其結構如圖所示,其中W、Y、Z三種元素分別位于不同的短周期且不同主族,W、Y、Z的最外層電子數之和等于X的最外層電子數,W、X對應的簡單離子核外電子層結構相同。下列敘述錯誤的是( )
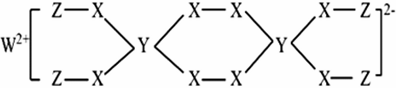
A.元素Y最高價的含氧酸是一種弱酸 B.該漂白劑的漂白原理與漂白粉相似 C.工業上通常采用電解熔融W的氧化物制備單質W D.該漂白劑中X、Y原子最外層均滿足8電子穩定結構 組卷:1引用:1難度:0.5 -
5.將1L0.1mol?L-1BaCl2溶液與足量稀硫酸充分反應放出akJ熱量,將1L0.5mol?L-1HCl溶液與足量CH3COONa溶液充分反應放出bkJ熱量(不考慮醋酸鈉水解);將0.5L1mol?L-1硫酸溶液與足量(CH3COO)2Ba(可溶性強電解質)溶液反應放出的熱量為( )
A.(5a-2b)kJ B.(5a+2b)kJ C.(2b-5a)kJ D.(10a+4b)kJ 組卷:6引用:1難度:0.7 -
6.下列離子方程式書寫正確的是( )
A.硫代硫酸鈉溶于酸:S2 +2H+═H2S+SO3O2-3B.過氧化氫與酸性高錳酸鉀:2 +5H2O2+6H+═2Mn2++5O2↑+8H2OMnO-4C.泡沫滅火劑原理:2Al3++3 +3H2O═2Al(OH)3↓+3CO2↑CO2-3D.重鉻酸鉀溶于水顯堿性:Cr2 +2OH?2O2-7+H2OCrO2-4組卷:5引用:1難度:0.7 -
7.下列說法正確的是( )
A.用容量瓶配好溶液后,應貼上標簽保存 B.仰視量筒刻度量取一定量濃硫酸,則所配制的0.10mol?L-1H2SO4溶液的濃度偏低 C.用NaOH溶液滴定鹽酸,滴定前尖嘴下端有氣泡,滴定后氣泡消失,會使結果偏高 D.用NaOH溶液滴定鹽酸時,用酚酞做指示劑,測量結果比真實鹽酸濃度偏低 組卷:57引用:1難度:0.5
二、填空題(共58分)
-
20.鉛蓄電池的拆解、回收和利用可以減少其對環境的污染,具有重要的可持續發展意義。利用廢鉛蓄電池的鉛膏(主要成分為PbSO4、PbO2,還有少量Pb、Fe2O3、Al2O3)制備PbO的流程如圖:
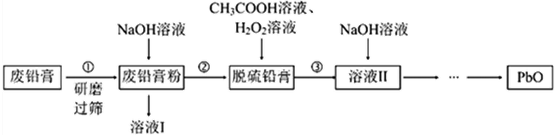
回答下列問題:
(1)步驟①將廢鉛膏研磨過篩的目的是。
(2)向廢鉛膏粉中加入NaOH溶液可將PbSO4轉化為PbO,反應的離子方程式是。
(3)溶液I中主要含有的陰離子有OH-、。
(4)加入CH3COOH溶液和H2O2溶液可將脫硫鉛膏中的含鉛物質轉化為(CH3COO)2Pb。H2O2的電子式為,PbO2轉化為(CH3COO)2Pb的化學方程式是。
(5)若廢鉛膏中鉛元素的質量分數為69%,用上述流程對1kg廢鉛膏進行處理,得到669gPbO,則鉛的回收率為%。[M(Pb)=207、M(O)=16]組卷:3引用:1難度:0.5 -
21.已知25℃時有關弱酸的電離平衡常數如表。
(1)已知常溫下,0.12mol/LH3PO4溶液pH=1.7,則磷酸的Ka1=弱酸 HCN CH3COOH H2S H2SO3 H3PO4 電離平衡常數 4.9×10-10 1.75×10-5 Ka1=1.3×10-7
Ka2=2.6×10-13Ka1=1.5×10-2
Ka2=1.0×10-8Ka1=?
Ka2=4.2×10-7
Ka3=5.6×10-11(已知lg2=0.3)。
(2)等體積等濃度的CH3COONa和NaCN溶液中的離子總數大小關系為:CH3COONaNaCN(填“大于”,“小于”或“等于”)。
(3)向Na2S溶液中通入過量SO2的離子反應方程式為。
(4)H2+PO-4?2PO3-4的平衡常數K=HPO2-4(填數值)。
(5)將1molSO2通入1L1.5mol/LNaOH溶液中充分反應,所得溶液離子濃度大小的關系為:。組卷:22引用:1難度:0.7


