2022-2023學年北京市高三(上)入學定位化學試卷
發布:2024/10/28 17:30:3
一、選擇題本部分共14題,每題3分,共42分。在每題列出的四個選項中,選出最符合題目要求的一項。
-
1.下列物質的用途,利用了氧化還原反應的是( )
A.明礬作凈水劑 B.鐵粉作暖貼發熱劑 C.生石灰作食品干燥劑 D.用熟石灰改良酸性土壤 組卷:145引用:3難度:0.9 -
2.下列說法正確的是( )
A.油脂的皂化屬于化學變化 B.氯堿工業利用的是原電池原理 C.“碳中和”是指利用中和反應吸收CO2 D.工業上用電解氯化鈉溶液的方法冶煉金屬鈉 組卷:5引用:2難度:0.9 -
3.下列化學用語表示正確的是( )
A.CH(CH3)3的名稱是2,2-二甲基乙烷 B.CO2的電子式是: 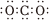
C.基態O原子核外電子的軌道表示式是 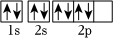
D.S2-的結構示意圖是 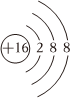 組卷:5引用:2難度:0.6
組卷:5引用:2難度:0.6 -
4.下列說法正確的是( )
A.HF、HCl、HBr的沸點依次增大 B.H原子的1s電子云輪廓圖為球形 C.CH2Cl2分子中的碳原子為手性碳原子 D.H2O分子的VSEPR模型是平面三角形 組卷:18引用:2難度:0.7 -
5.下列反應的方程式表示正確的是( )
A.用濃溴水檢驗水體中的苯酚:2 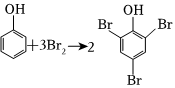 ↓
↓B.向AgNO3溶液中滴入氨水至沉淀剛好消失:Ag++2NH3?H2O═[Ag(NH3)2]++OH- C.實驗室制氯氣:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O△D.“84消毒液”中加少量食醋可增強漂白性:ClO-+H+═HClO 組卷:14引用:2難度:0.6 -
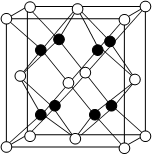 6.鈉的一種氧化物的正方體晶胞如圖所示(“●”或“〇”均表示一個簡單離子)。下列說法正確的是( )
6.鈉的一種氧化物的正方體晶胞如圖所示(“●”或“〇”均表示一個簡單離子)。下列說法正確的是( )A.該氧化物的化學式為Na2O2 B.晶胞中連接“〇”與“●”的線段表示共價鍵 C.晶胞中與“〇”最近且等距的“●”的數目為4 D.該晶體中“〇”與“●”的核外電子排布相同 組卷:86引用:4難度:0.8
二、非選擇題本部分共5題,共58分。
-
18.鉑(Pt)是一種貴金屬,廣泛用于化工領域。從某廢催化劑(主要含有Pt、C、Al2O3、MgO)中回收Pt的一種工藝流程如圖所示。

(1)Ⅰ中焙燒時,C與空氣中的O2生成了CO和CO2,發生的反應如下:C(s)+O2(g)=CO2(g)ΔH1=-393.5kJ?mol-1;2C(s)+O2(g)=2CO(g)ΔH2=-221kJ?mol-1;2CO(g)+O2(g)=2CO2(g)ΔH3=kJ?mol-1。
(2)實驗人員采用三種不同的浸出液分別研究Ⅱ中Pt的浸出率。所用的浸出液分別是HCl-H2SO4-NaClO3、HCl-NaClO3和HCl-H2O2。
①將下列浸出反應的離子方程式補充完整:3Pt+Cl-++ClO-3=3[PtCl6]2-+H2O。
②當NaClO3或H2O2作為氧化劑浸出等量Pt時,n(NaClO3):n(H2O2)=。
③c(H+)相同、浸出時間相同時,三種浸出液對Pt的浸出率如下。[注:c(NaClO3)按照②中的物質的量關系換算成c(H2O2)計]。
a.以HCl-NaClO3為例,說明當其中氧化劑濃度大于0.2mol?L-1時,Pt的浸出率降低的原因:隨著c(NaClO3)增大,其氧化性增強,部分氧化劑濃度/mol?L-1 0.1 0.2 0.3 0.4 甲 HCl-H2SO4-NaClO3對Pt的浸出率/% 72.7 78.2 77.5 75.4 乙 HCl-NaClO3對Pt的浸出率/% 79.6 85.3 82.1 81.6 丙 HCl-H2O2對Pt的浸出率/% 80.0 85.6 83.2 82.5 被ClO-3還原而消耗。
b.氧化劑濃度均為0.2mol?L-1時,甲中Pt的浸出率最低的可能原因:由于三種浸出液中的c(H+)均相同,。
(3)Ⅲ中萃取劑(P3N)的萃取機理如下(O表示有機體系,A表示水溶液體系)。
ⅰ.R3N(O)+H+(A)+Cl-(A)?R3NHCl(O)
ⅱ.2R3NHCl(O)+[PtCl6]2-(A)?(R3NH2)[PtCl6](O)+2Cl-(A)
①分離操作x是。
②Ⅳ中向含Pt的有機物中加入NaOH溶液可使[PtCl6]2-進入水溶液體系,反應的離子方程式是。組卷:3引用:2難度:0.7 -
19.Fe2+在空氣中易被氧化。某小組探究綠礬(FeSO4?7H2O)和莫爾鹽[(NH4)2Fe(SO4)2?6H2O]在空氣中的穩定性。
Ⅰ.探究溶液中的穩定性:配制0.1mol?L-1兩種溶液[A:FeSO4,B:(NH4)2Fe(SO4)2],露置于空氣中一段時間,并檢驗其中的Fe3+,結果如下。
(1)新配制的A溶液pH<7,原因是Fe2+發生了水解,離子方程式是編號 新配制 1h后 24h后 pH 性狀 酸化后滴等量KSCN(aq) pH 性狀 酸化后滴等量KSCN(aq) pH 性狀 A 3.9 無色溶液 幾乎無色 3.4 黃色溶液 變紅 3.3 紅褐色沉淀 B 3.9 無色溶液 幾乎無色 3.3 黃色溶液 變紅 3.2 紅褐色沉淀 。
(2)常溫時0.1mol?L-1(NH4)2SO4溶液pH=5.0,則B溶液中水解程度:Fe2+NH4+(填“>”或“<”),因此新配制的A、B溶液pH幾乎相同。
(3)放置24h后溶液pH均減小,寫出該過程中Fe2+被空氣氧化的離子方程式:。
上述實驗說明兩種溶液中的Fe2+的穩定性差異不大。
Ⅱ.探究晶體的穩定性:將兩種晶體分別在不同條件下放置數天,實驗記錄如下。
(4)上述實驗說明,相同條件下兩種晶體在空氣中穩定性更強的是編號 ⅰ ⅱ ⅲ ⅳ 實驗條件 露置 密閉容器 潮濕的密閉容器 盛有干燥劑的密閉容器 實驗結果 綠礬 晶體逐漸變白,進而出現土黃色;Fe3+含量很多 無明顯變化;Fe3+含量非常少 晶體結塊,顏色不變;Fe3+含量非常少 晶體逐漸變白,最終出現淡黃色;Fe3+含量很多 莫爾鹽 無明顯變化;Fe3+含量非常少 無明顯變化;Fe3+含量非常少 晶體略結塊,顏色不變;Fe3+含量非常少 無明顯變化;Fe3+含量很少 。
(5)甲同學推測綠礬在ⅱ中的結果與ⅰ不同可能是容器中O2不足造成的。乙同學經過對比,分析該推測不成立,其理由是。
(6)該小組同學根據實驗結果進而推測綠礬易被氧化與其失去結晶水有關。
①綠礬晶體失去結晶水的實驗現象是。
②莫爾鹽晶體中離子的存在使結晶水不易失去;該離子與H2O分子之間可能存在的作用是。
(7)同學們經過對兩種晶體結構的比較,分析莫爾鹽在空氣中更穩定,除了上述原因外,還可能的原因:莫爾鹽晶體中離子間的空隙較小,。組卷:12引用:2難度:0.5


