2021-2022學年北京市101中學高一(上)期中化學試卷
發布:2024/11/2 17:30:1
一、選擇題(共42分)(共21道小題,每小題只有一個選項符合題意,每小題2分。)
-
1.下列材料中,主要成分均為非金屬單質的是( )




A、火箭液體發動機的推進劑
——液氧和液氫B、海底光纜
——二氧化硅C、潛水器外殼
——鈦、鋁等D、返回器表面所貼“暖寶寶”主要成分
——鐵粉、碳粉等A.A B.B C.C D.D 組卷:34引用:2難度:0.8 -
2.下列物質中,屬于電解質的是( )
A.鐵 B.氫氧化鈣 C.稀硫酸 D.乙醇 組卷:25引用:2難度:0.6 -
3.氯酸鉀(KClO3)可用于制造煙花、安全火柴等,關于該物質的分類正確的是( )
A.鹽 B.氧化物 C.酸 D.堿 組卷:49引用:4難度:0.9 -
4.同溫同壓下,相同體積的O2和O3具有相同的( )
A.密度 B.質量 C.分子數 D.原子數 組卷:98引用:16難度:0.9 -
5.下列傳統釀醋工藝的主要步驟中,包含溶解和過濾操作的是( )
A.蒸拌原料 B.淀粉發酵 C.清水浸淋 D.放置陳釀 



A.A B.B C.C D.D 組卷:86引用:8難度:0.7 -
6.下列含硫元素的粒子,只有還原性的是( )
A.S B.S2- C.SO42- D.SO2 組卷:142引用:2難度:0.7 -
7.溶液和膠體的本質區別是( )
A.是否有丁達爾現象 B.是否是混合物 C.分散質能否通過濾紙 D.分散質的粒子直徑大小 組卷:52引用:2難度:0.8 -
8.下列關于鈉的說法不正確的是( )
A.密度比水大 B.可以用小刀切割 C.保存在煤油中 D.銀白色固體 組卷:28引用:3難度:0.8
二、非選擇題(共58分)
-
24.利用酸性含錳廢水(主要含Mn2+、Cl-、H+、Fe2+、NH4+、Cu2+)可制備高性能磁性材料(MnCO3)、CuCl2及NH4Cl。工業流程如圖:
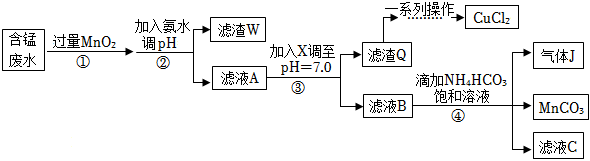
已知:
①大多數氧化物可以在一定的酸性環境中存在。
②金屬離子在沉淀為氫氧化物時,其濃度會隨著pH升高而逐漸降低,直至沉淀完全。幾種金屬離子沉淀為氧化物的pH范圍如下表所示:
回答下列問題:金屬離子 Fe3+ Cu2+ Fe2+ Mn2+ 開始沉淀時的pH 3.2 5.2 7.5 8.8 完全沉淀時的pH 3.7 6.4 9.7 10.4
(1)根據題目信息及表格中數據分析,含錳廢水的pH應為(填序號)。
A.小于3.2
B.等于7
C.大于10.4
D.無法確定
(2)過程①中,MnO2在酸性條件下可將Fe2+氧化為Fe3+,并生成Mn2+,請補全反應的離子方程式:MnO2+Fe2++═Mn2++Fe3++H2O。
(3)過程②所得濾渣W是,調pH范圍應為(填序號)。
A.3.2~5.2
B.3.7~5.2
C.6.4~7.5
D.8.8~9.7
(4)過程③中,試劑X可以選用(填序號)。
A.HCl
B.NH3?H2O
C.Na2CO3
D.Cu(OH)2
(5)已知濾渣Q是Cu(OH)2,請寫出由Cu(OH)2制備CuCl2的化學反應方程式。
(6)過程④中,生成的氣體J可使澄清的石灰水變渾濁,請補全生成MnCO3的離子反應方程式:Mn2++HCO3-=MnCO3↓++H2O。
(7)從濾液C中可得到的產品是(填化學式)。組卷:33引用:1難度:0.6 -
25.某研究小組欲探究Fe2+能否與H2O2溶液反應。
【查閱資料】
ⅰ.Fe2+具有較強的還原性,O2具有較強的氧化性。
ⅱ.Fe3+遇SCN-可生成Fe(SCN)3,Fe(SCN)3溶液呈血紅色,可用于Fe3+的檢驗。
【提出猜想】
(1)小組同學經過討論后,認為H2O2溶液可以與FeSO4溶液反應,請從化合價的角度加以解釋:。
【設計實驗】
(2)實驗Ⅰ:在試管中加入FeSO4溶液和H2O2溶液,再加入KSCN溶液,發現溶液,小組同學認為Fe2+和H2O2溶液反應生成了Fe3+。
(3)甲同學注意到盛放FeSO4溶液的試劑瓶中有空氣,因此不同意該結論,他的理由是。
重新設計實驗:
實驗Ⅱ:在試管中加入FeSO4溶液,然后加入KSCN溶液,發現溶液無明顯變化,再加入H2O2溶液,發現溶液變紅。
【獲得結論】
(4)過氧化氫(填“能”或者“不能”)氧化Fe2+。
【發現異常】
乙同學繼續向實驗Ⅱ所得溶液中滴加H2O2溶液,發現溶液褪色。
小組同學經過重新查閱資料后,發現H2O2可以將SCN-氧化為。乙同學設計實驗Ⅲ并證實了該資料中的說法。SO2-4
(5)補全實驗Ⅲ的方案:在試管中加入H2O2溶液,加入KSCN溶液,再加入,產生。
【總結反思】
(6)小組同學經過討論后,提出了Fe2+的檢驗方法:取待測液于試管中,,證明待測液含有Fe2+。
(7)從上述實驗中可以得出結論,在物質性質的檢驗中,應注意(至少寫出兩條)對實驗結果的影響。組卷:36引用:1難度:0.6


