2021-2022學年福建省三明一中高二(上)開學化學試卷
發布:2024/11/9 12:0:2
一、選擇題:本題共16小題,每小題3分,共48分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.下列反應屬于吸熱反應的是( )
A.Ba(OH)2?8H2O與NH4Cl的反應 B.乙醇燃燒 C.鋁粉與氧化鐵粉末反應 D.NaOH與HCl反應 組卷:94引用:8難度:0.3 -
2.下列過程需要通電才能進行的是( )
①電離 ②電解 ③電鍍 ④電泳 ⑤電化學腐蝕.A.①②③ B.②③⑤ C.②③④ D.全部 組卷:13引用:5難度:0.9 -
3.下列說法不正確的是( )
A.反應CaO+H2O═Ca(OH)2可放出大量的熱,故可把該反應設計為原電池 B.將Fe、Cu用導線連接后放入濃硝酸中組成原電池,Cu為負極,Fe為正極 C.通過原電池裝置,可將反應2H2+O2═2H2O的化學能轉化為電能,為航天器供電 D.某電池反應Fe+2FeCl3═3FeCl2,當電路中有1mol e-通過時,電解質溶液增重28g 組卷:16引用:3難度:0.7 -
4.下列裝置可構成原電池的是( )
A. 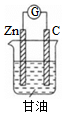
B. 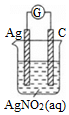
C. 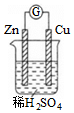
D. 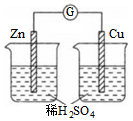 組卷:9引用:1難度:0.5
組卷:9引用:1難度:0.5 -
5.實驗測得:101kPa時,1mol H2完全燃燒生成液態水,放出285.8kJ的熱量:1mol CH4完全燃燒生成液態水和CO2,放出890.3kJ的熱量。下列熱化學方程式的書寫正確的是( )
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=890.3kJ?mol-1
②CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ
③CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ?mol-1
④2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-1A.僅有②④ B.僅有④ C.僅有②③④ D.全部符合要求 組卷:76引用:7難度:0.7 -
6.根據圖中的能量關系,可求得C-H的鍵能為( )
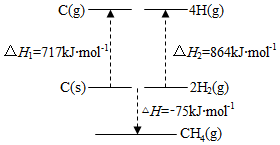
A.414kJ?mol-1 B.377kJ?mol-1 C.235kJ?mol-1 D.197kJ?mol-1 組卷:889引用:13難度:0.6 -
7.堿性鋅錳干電池的總反應為:Zn+2MnO2+2H2O═2MnO(OH)+Zn(OH)2。下列關于該電池的說法中正確的是( )
A.Zn為負極,MnO2為正極 B.工作時電子由MnO2經由外電路流向Zn C.工作時OH-移向正極 D.電池放電過程中,溶液的酸堿性一定不變 組卷:138引用:1難度:0.7
二、非選擇題:本題共5小題,共52分。請根據題目要求作答。
-
20.化學在能源開發與利用中起著十分關鍵的作用。
(1)下列制氫氣方法中最節能的是(填序號)。
A.電解水制氫氣:2H2O2H2↑+O2↑通電
B.高溫使水分解制氫氣:2H2O2H2↑+O2高溫
C.太陽光催化分解水制氫氣:2H2O2H2↑+O2↑TiO2太陽光
D.天然氣制氫氣:CH4+H2OCO+3H2高溫
(2)蘊藏在海底的“可燃冰”是高壓下形成的外觀像冰的甲烷水合物固體。甲烷氣體氧化和水汽化的熱化學方程式分別為:
①CH4(g)+2O2(g)═CO2(g)+2H2O(g) ΔH=-802.3kJ?mol-1
②H2O(l)═H2O(g) ΔH=+44kJ?mol-1
則3.2kg“可燃冰”(分子式為CH4?8H2O)釋放的甲烷氣體完全氧化生成二氧化碳氣體和液態水時放出的熱量為。
(3)家用液化氣的主要成分之一是丁烷(C4H10)。常溫常壓條件下,1g丁烷完全燃燒生成CO2氣體和液態水時放出熱量50kJ,則表示丁烷摩爾燃燒焓的熱化學方程式為。
(摩爾燃燒焓指在一定反應溫度和壓強下,1mol純物質完全氧化為同溫下的指定產物時的焓變)
(4)0.3mol的氣態高能燃料乙硼烷(B2H6)在氧氣中氧化生成固態三氧化二硼和液態水時放出649.5kJ熱量,其熱化學方程式為。
(5)標準摩爾生成焓是指在25℃和101kPa時,最穩定的單質生成1mol化合物的焓變。已知25℃和101kPa時下列反應:
①2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l) ΔH1
②C(s,石墨)+O2(g)═CO2(g) ΔH2
③2H2(g)+O2(g)═2H2O(l) ΔH3
寫出乙烷標準摩爾生成焓的焓變ΔH=(用含ΔH1、ΔH2、ΔH3的式子表示)。組卷:10引用:1難度:0.8 -
21.能源、環境與生產生活和社會發展密切相關。
(1)工業上利用CO和H2在催化劑作用下合成甲醇:CO(g)+2H2?CH3OH(g),已知反應中有關物質的化學鍵鍵能數據如表所示:
則CO(g)+2H2(g)?CH3OH(g) ΔH=化學鍵 H-H C-O C≡O H-O C-H E/(kJ/mol) 436 343 1076 465 413 kJ?mol-1
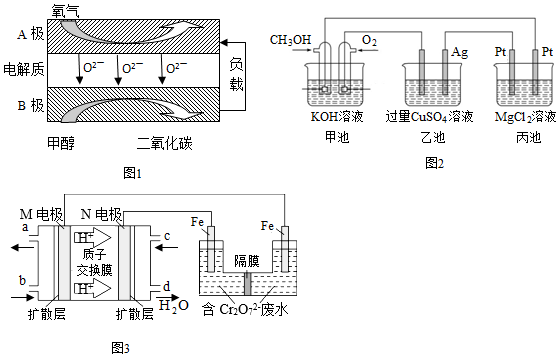
(2)以甲醇為燃料的新型電池,其成本大大低于以氫氣為燃料的傳統燃料電池。圖1是目前研究較多的一類固體氧化物燃料電池工作原理示意圖。B極為電池極,B極的電極反應式為。
(3)如圖2,其中甲池的總反應式為:2CH3OH+3O2+4KOH═2K2CO3+6H2O,下列說法正確的是
①乙、丙池是裝置,丙池中石墨電極的名稱是。
②甲池通入氧氣的電極反應式為。
③電解一段時間后,乙池中溶液的pH將(填“增大”“減小”或“不變”)
④丙池中陰極上發生的電極反應為。
(4)現以甲醇燃料電池,采用電解法來處理酸性含鉻廢水(主要含有Cr2O72-),實驗室利用如圖3裝置模擬該方法:
①N電極為電池的(填“正”或“負”)極,M電極的電極反應式為。
②請闡述電解法除去含鉻廢水中鉻的原理。組卷:57引用:1難度:0.5


