2022年天津市西青區張家窩中學高考化學一模試卷
發布:2024/4/20 14:35:0
一.單項選擇題(本卷有12題,每題3分共36分)在每題給出的四個選項中,只有一項是最符合題目要求的
-
1.化學在工農業生產和日常生活中都有重要應用。下列敘述正確的是( )
A.華為自主研發的“麒麟”芯片與太陽能電池感光板所用材料均為晶體硅 B.食品包裝袋中常有硅膠、生石灰、還原鐵粉等,其作用都是防止食品氧化變質 C.自來水廠常用明礬、O3、ClO2等做水處理劑,其作用都是殺菌消毒 D.用于制造“山東艦”上艦載機降落攔阻索的特種鋼,屬于新型無機非金屬材料 組卷:140引用:3難度:0.6 -
2.下列物質能用玻璃試劑瓶(細口瓶)和玻璃塞保存的是( )
A.KOH溶液 B.Na2SiO3溶液 C.濃硝酸 D.氫氟酸溶液 組卷:26引用:2難度:0.7 -
3.下列實驗裝置能達到實驗目的的是( )
A. 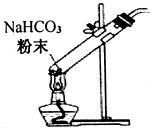
制純堿B. 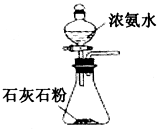
制NH3C. 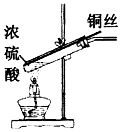
制SO2D. 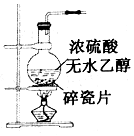
制取乙烯組卷:89引用:2難度:0.5 -
4.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.2.0gH218O與D2O的混合物中所含中子數為NA B.常溫常壓下,4.4g乙醛所含σ鍵數目為0.7 NA C.標準狀況下,5.6L CO2與足量Na2O2反應轉移的電子數為0.5 NA D.50ml 12mol/L鹽酸與足量MnO2共熱,轉移的電子數為0.3 NA 組卷:205引用:8難度:0.7 -
5.25℃時,下列各組離子在指定溶液中一定能大量共存的是( )
A.pH=1的溶液中:Na+、K+、MnO4-、CO32- B.c(H+)=1×10-13mol?L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- C.0.1mol?L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- D.0.1mol?L-1FeCl3溶液中:Fe2+、NH4+、SCN-、SO42- 組卷:1665引用:34難度:0.9 -
6.下列化學用語解釋事實或過程正確的是( )
A.Fe3O4溶于過量稀硝酸中:Fe3O4+8H+═2Fe3++Fe2++4H2O B.鉛蓄電池充電時陰極反應:PbSO4(s)+2e-═Pb(s)+SO42-(aq) C.用足量氨水吸收煙氣中的二氧化硫:SO2+2OH-═SO32-+H2O D.用酸性高錳酸鉀標準溶液滴定草酸:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O 組卷:88引用:2難度:0.5
二、非選擇題
-
18.高鐵酸鹽是優良的多功能水處理劑。K2FeO4為紫色固體,可溶于水,微溶于濃KOH溶液,難溶于有機物;在0~5℃、強堿性溶液中比較穩定,在酸性、中性溶液中易分解放出O2。現某實驗小組制備高鐵酸鉀(K2FeO4)裝置如圖所示,夾持、加熱等裝置略。回答下列問題:
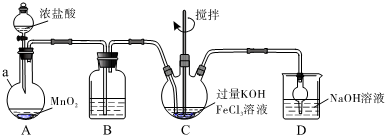
(1)裝置B中除雜質所用試劑是,裝置D的作用是。
(2)C中反應為放熱反應,而反應溫度須控制在0~5℃,反應中KOH必須過量的原因是。
(3)C中制備高鐵酸鉀的反應體系中有六種微粒;Fe3+、Cl2、OH-、FeO42-、Cl-、H2O。寫出總反應的離子方程式:。C中混合物經過重結晶、有機物洗滌純化、真空干燥,得到高鐵酸鉀晶體若反應過程中轉移了0.6mol電子,則還原產物的物質的量為mol。組卷:11引用:1難度:0.6 -
19.國家主席習近平指出,為推動實現碳達峰、碳中和目標,我國將陸續發布重點領域和行業碳達峰實施方案和一系列支撐保障措施,構建起碳達峰碳中和“1+N”政策體系。二氧化碳加氫可轉化為二甲醚,既可以降低二氧化碳排放量,也可以得到性能優良的汽車燃料。
回答下列問題:
(1)制取二甲醚的熱化學方程式為:2CO2(g)+6H2(g)?CH3OCH(g)+3H2O(g) ΔH。則ΔH=。
已知:①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)ΔH1=-49.0kJ?mol-1。
②2CH3OH(g)?CH3OCH3(g)+H2O(g)ΔH2=-23.5kJ?mol-1。
(2)往一容積為2 L的恒容密閉容器中通入2molCO和6molH2,一定溫度下發生反應:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)。起始總壓為Po,20min時達到化學平衡狀態,測得CH3OCH3的物質的量分數為12.5%。
①達到化學平衡狀態時,下列有關敘述正確的是(填字母序號)。
a.容器內氣體壓強不再發生改變
b.正、逆反應速率相等且均為零
c.向容器內再通入1molCO2和3molH2,重新達平衡后CH3OCH3體積分數增大
d.向容器內通入少量氦氣,則平衡向正反應方向移動
②0~20min內,用H2表示的平均反應速率v(H2)=,CO2的平衡轉化率α(CO2)=;該溫度下,反應的平衡常數Kp=(用含P0的式子表達,用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)。
③升高溫度,二甲醚的平衡產率(填“增大”、“減小”或“不變”),簡述理由:。
④工業上,CO2與H2混合氣體以一定的比例和一定流速分別通過填充有催化劑Ⅰ、Ⅱ的反應器,CO2轉化率與溫度的關系如圖。在催化劑Ⅱ作用下,溫度高于T1時,CO2轉化率下降的原因可能是。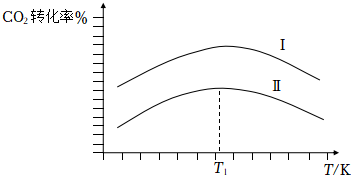 組卷:46引用:3難度:0.5
組卷:46引用:3難度:0.5


