2022-2023學年福建省福州市重點中學高一(下)期中化學試卷
發布:2024/4/20 14:35:0
一、單選題(本大題共16小題,共48.0分)
-
1.下列反應既屬于氧化還原反應,又屬于吸熱反應的是( )
A.鋁片與稀鹽酸反應 B.Ba(OH)2?8H2O與NH4Cl的反應 C.灼熱的碳與CO2的反應 D.甲烷在氧氣中的燃燒反應 組卷:13引用:9難度:0.7 -
2.下列反應必須加入氧化劑且一步反應就能完成的是( )
①N2→NO2
②NO2→NO
③NO2→HNO3
④N2→NO
⑤N2→NH3A.① B.②⑤ C.④ D.③④ 組卷:67引用:7難度:0.6 -
3.白磷與氧氣可發生如下反應:P4+5O2=P4O10。已知斷裂下列化學鍵需要吸收的能量分別為:P-P akJ/mol、P-O bkJ/mol、P=O ckJ/mol、O=O dkJ/mol,根據圖示的分子結構和有關數據估算該反應的ΔH,其中正確的是( )
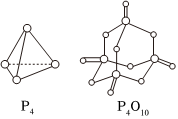
A.(4c+6b-6a-5d)kJ/mol B.(6a+5d-4c-12b)kJ/mol C.(4c+12b-6a-5d)kJ/mol D.(6a+5d-4c-6b)kJ/mol 組卷:30引用:3難度:0.6 -
4.下列各組熱化學方程式中,化學反應的ΔH前者大于后者的是( )
A.C(s)+O2(g)=CO2(g)ΔH1,C(s)+ O2(g)=CO(g)ΔH212B.S(s)+O2(g)=SO2(g)ΔH3,S(g)+O2(g)=SO2(g)ΔH4 C.2H2(g)+O2(g)=2H2O(l)ΔH5,H2(g)+ O2(g)=H2O(l)ΔH612D.CaO(s)+H2O(l)=Ca(OH)2(s)ΔH7,CaCO3(s)=CaO(s)+CO2(g)ΔH8 組卷:162引用:4難度:0.7 -
5.反應3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)在一容積可變的密閉容器中進行,下列條件的改變能使反應速率加快的是( )
①增加鐵的量
②將容器的體積縮小一半
③保持體積不變,充入N2使體系壓強增大
④保持體積不變,充入水蒸氣使體系壓強增大A.①④ B.②③ C.③④ D.②④ 組卷:103引用:3難度:0.6 -
6.反應O2(g)+C(s)?CO(g)+H2(g)在體積和溫度不變的密閉容器中進行。下列事實中,不能作為反應達到化學平衡狀態的標志的是( )
A.反應器內氧氣的濃度不再隨著時間的改變而變化 B.反應器內氣體的壓強不隨著時間的變化而變化 C.反應器內氣體的密度不隨著時間的變化而變化 D.反應器內氧氣的濃度和一氧化碳的濃度相等 組卷:81引用:3難度:0.5 -
7.氫能的低成本、低溫、高效率制取一直是亟待解決的關鍵難題。實驗計算機模擬在催化劑表面水煤氣變換低溫產氫反應(CO+H2O═CO2+H2)過程中能量的變化如圖所示,下列說法正確的是( )

A.CO+H2O═CO2+H2為放熱反應 B.狀態3中物質狀態最穩定 C.過程Ⅰ、Ⅱ、Ⅲ均需要吸收能量 D.該反應類型為置換反應 組卷:59引用:5難度:0.7
三、簡答題(本大題共3小題,共30.0分)
-
 20.電池是人類生產和生活中的重要能量來源,各式各樣電池的發明是化學對人類的一項重要貢獻。
20.電池是人類生產和生活中的重要能量來源,各式各樣電池的發明是化學對人類的一項重要貢獻。
(1)生活中利用原電池原理生產了各種各樣的電池,下列有關電池的敘述正確的是(填字母)。
A.鋅錳電池工作一段時間后碳棒會變細
B.氫氧燃料電池可將化學能直接轉變為電能
C.鉛蓄電池負極是PbO2,正極是Pb
(2)氫氧燃料電池有酸式和堿式兩種,它們放電時的電池總反應式都可表示為:2H2+O2=2H2O。
①酸式氫氧燃料電池的電解質是酸,其正極的電極反應式為。
②工作一段時間后,電解質溶液的pH將(填“變大”、“變小”或“不變”)。
(3)將CH4設計成燃料電池,其利用率更高,裝置如圖所示(A、B為多孔碳棒),電池總反應為:CH4+2O2+2KOH=K2CO3+3H2O。
實驗測得電子定向移向A電極,則(填“A”或“B”)電極入口通甲烷,其電極反應式為。
(4)某同學欲把反應Fe+2FeCl3=3FeCl2設計成原電池,請寫出負極的電極反應式:。組卷:73引用:3難度:0.5 -
21.氮是大氣中含量最多的一種元素,氮及其化合物在生產、生活中有著重要作用。請回答:
(1)下列變化屬于“氮的固定”的是(填字母)。
a.植物從土壤中吸收氮肥
b.硝酸和氨氣反應生成氮肥
c.將空氣中的氮氣轉變為氮的化合物
d.大豆的根瘤菌將含氮的化合物轉變為植物蛋白質
(2)汽車尾氣中的CO、NOx在適宜溫度下采用催化轉化法處理,使它們相互反應生成參與大氣循環的無毒氣體。寫出NO被CO還原的化學方程式:。
(3)工業尾氣中氮的氧化物常采用堿液吸收法處理。
①NO2被燒堿溶液吸收時,生成兩種鈉鹽,其物質的量之比為1:1,寫出該反應的化學方程式:。
②NO與NO2按物質的量之比為1:1被足量NaOH溶液完全吸收后只得到一種鈉鹽,該鈉鹽的化學式是。
(4)足量銅與一定量濃硝酸反應,得到硝酸銅溶液和NO2、N2O4、NO的混合氣體,這些氣體與3.36LO2(標準狀況)混合后通入水中,所有氣體完全被水吸收生成硝酸,若向所得硝酸銅溶液中加入10mol/LNaOH溶液至Cu2+恰好完全沉淀,則消耗NaOH溶液的體積是。
A.60mL
B.45mL
C.30mL
D.15mL組卷:38引用:2難度:0.7


