必修2《第二章化學反應與能量》2017年單元測試卷(江西省銅鼓市)
發布:2024/4/20 14:35:0
一、選擇題(每小題4分,共48分).
-
1.在盛有稀H2SO4的燒杯中放入用導線連接鋅片和銅片,下列敘述正確的是( )
A.正極發生得電子的氧化反應 B.電子通過導線由銅片流向鋅片 C.正極有O2逸出 D.銅片上有H2逸出 組卷:71引用:21難度:0.7 -
2.反應4A(g)+5B(g)?4C(g)+6D(g) 在5L的密閉容器中進行反應,30min后,C的物質的量增加了0.30mol.下列敘述正確的是( )
A.30min中A的平均反應速率是0.010mol?L-1?min-1 B.容器中D的物質的量一定增加了0.45mol C.容器中A、B、C、D的物質的量的比一定是4:5:4:6 D.容器中A的物質的量一定增加0.30mol 組卷:257引用:10難度:0.9 -
3.如圖圖示與對應的敘述不相符的是( )

A.圖1的目的是檢驗裝置的氣密性 B.圖2中分液漏斗振蕩靜置后,上層液體顏色變淺 C.圖3中電流計的指針不發生偏轉 D.圖4液態水分解的熱化學方程式為:2H2O(1)═2H2(g)+O2(g)△H=+571.6KJ/mol 組卷:61引用:2難度:0.9 -
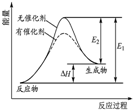 4.某可逆反應的反應過程中能量變化如圖所示(圖中E1表示正反應的活化能,E2表示逆反應的活化能).下列有關敘述正確的是( )
4.某可逆反應的反應過程中能量變化如圖所示(圖中E1表示正反應的活化能,E2表示逆反應的活化能).下列有關敘述正確的是( )A.該反應為放熱反應 B.催化劑能改變反應的焓變 C.催化劑能改變反應的路徑 D.逆反應的活化能大于正反應的活化能 組卷:52引用:7難度:0.7 -
5.下列熱化學方程式或離子方程式中,正確的是( )
A.0.01mol?L-1NH4Al(SO4)2溶液與0.02mol?L-1Ba(OH)2溶液等體積混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3?H2O B.一定條件下,將0.5mol N2(g)和1.5molH2(g)置于密閉的容器中充分反應生成NH3(g),放熱19.3kJ,其熱化學方程式為:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ?mol-1 C.2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ?mol-1,則H2的燃燒熱為571.6 kJ?mol-1 D.CO(g)的燃燒熱是283.0 kJ?mol-1,則CO2分解的熱化學方程式為:2CO2(g)═2CO(g)+O2(g)△H=+283.0 kJ?mol-1 組卷:34引用:4難度:0.9
二、非選擇題(共52分)
-
 15.某校化學興趣小組的同學按圖所示將實驗裝置連接好,進行化學能與熱能轉化的實驗探究.請幫他們回答下列問題:
15.某校化學興趣小組的同學按圖所示將實驗裝置連接好,進行化學能與熱能轉化的實驗探究.請幫他們回答下列問題:
實驗前,在U型管內加入少量品紅溶液(或紅墨水).打開3個T型管螺旋夾,使U型管內兩邊的液面處于同一水平面,再夾緊螺旋夾.
(1)在內部的試管里盛1g氧化鈣,當滴入2mL左右的蒸餾水后,打開a、b螺旋夾,可觀察到U型管里的紅墨水如何變化?.
(2)如果用這個裝置觀察到U型管內出現與上述(1)相反的現象,可在小試管中加入固體后滴入適量的蒸餾水.
(3)若向內部的試管中放入幾小塊銅片,再用滴管滴入10mL稀硝酸,能否得到(1)中現象?,另外可觀察到的現象是;產生上述現象的原因是;寫出有關反應的化學方程式;由此可知,反應后產物的總能量(填“大于”、“小于”、“等于”)硝酸和銅片的總能量.此時該裝置有明顯的不足,原因是,改進的方法是.組卷:49引用:2難度:0.5 -
 16.給你提供純鋅、純銅片、500 mL 0.2 mol/L的H2SO4溶液、導線、1 000 mL量筒.試用如圖裝置來測定鋅和稀硫酸反應時,在某段時間內通過導線的電子的物質的量.
16.給你提供純鋅、純銅片、500 mL 0.2 mol/L的H2SO4溶液、導線、1 000 mL量筒.試用如圖裝置來測定鋅和稀硫酸反應時,在某段時間內通過導線的電子的物質的量.
(1)如圖所示,裝置氣密性良好,且1 000mL量筒中已充滿了水,則開始實驗時,首先要.
(2)①a電極材料為,其電極反應式為.
②b電極材料為,其電極反應式為.
(3)當量筒中收集到672 mL氣體時(已折算到標準狀況下),通過導線的電子的物質的量為.組卷:26引用:4難度:0.5


