2018-2019學年福建省福州市屏東中學高一(上)期末化學試卷
發布:2024/11/27 18:30:6
一、選擇題(共25小題,每小題2分,滿分50分)
-
1.以“賞中華詩詞、尋文化基因、品生活之美”為基本宗旨的《中國詩詞大會》不僅弘揚了中國傳統文化,還蘊含著許多化學知識,下列詩詞分析不正確的是( )
A.詩句“只要功夫深,鐵杵磨成針”,該過程只涉及物理變化 B.杜牧詩句“煙籠寒水月籠沙,夜泊秦淮近酒家”,此處的“煙”指固體 C.王安石詩句“爆竹聲中一歲除,春風送暖入屠蘇”,爆竹的燃放涉及氧化還原反應 D.曹植詩句“煮豆燃豆萁,豆在釜中泣”,這里的能量變化主要是化學能轉化為熱能 組卷:160引用:5難度:0.9 -
2.“分類”是一種思想方法,在化學發展中起到了重要的作用.下列說法正確的是( )
A.Na2O和Na2O2均能與H2O反應生成NaOH,故二者都是堿性氧化物 B.根據分散系是否具有丁達爾現象將分散系分為溶液、膠體和濁液 C.根據水溶液能否導電將化合物分為電解質和非電解質 D.堿性氧化物一定是金屬氧化物,酸性氧化物不一定是非金屬氧化物 組卷:93引用:7難度:0.9 -
3.現有兩瓶無標簽的無色溶液,分別裝有Na2CO3和NaHCO3,用下列試劑或方法能將兩者區分的是( )
①Ca(OH)2 ②鹽酸 ③CaCl2 ④NaOH ⑤加熱A.①③ B.①④ C.②③ D.②⑤ 組卷:122引用:9難度:0.7 -
4.亞硝酸鹽中毒,又名烏嘴病、紫紺病、腸源性青紫病.亞硝酸鹽可將正常的血紅蛋白氧化成高鐵血紅蛋白,血紅蛋白中的鐵元素由二價變為三價,失去攜氧能力,使組織出現缺氧現象.美藍是亞硝酸鹽中毒的有效解毒劑.下列說法不正確的是( )
A.在中毒過程中血紅蛋白被氧化 B.中毒時亞硝酸鹽發生氧化反應 C.藥品美藍應具有還原性 D.解毒時血紅蛋白被還原 組卷:75引用:8難度:0.5 -
5.以下化學反應的離子方程式書寫正確的是( )
A.硫酸與氫氧化鋇溶液反應:H++OH-=H2O B.碳酸鈣與鹽酸反應: +2H+=H2O+CO2↑CO2-3C.鐵與氯化鐵溶液反應:Fe+Fe3+=2Fe2+ D.氯氣與溴化鈉溶液反應:Cl2+2Br-=Br2+2Cl- 組卷:9引用:6難度:0.9 -
6.下列化學用語正確的是( )
A.質子數為17、中子數為20的氯原子: Cl3717B.氟原子的結構示意圖: 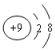
C.明礬的化學式:KAlSO4?12H2O D.次氯酸的電離方程式:HClO=H++ClO- 組卷:31引用:2難度:0.7 -
7.除去鎂粉中混有的少量鋁粉,可選用的溶液是( )
A.鹽酸 B.硝酸 C.氨水 D.氫氧化鈉溶液 組卷:16引用:3難度:0.7 -
8.生活中難免會遇到一些突發事件,我們要善于利用學過的知識,采取科學、有效的方法保護自己.如果發生了氯氣泄漏,以下自救方法得當的是( )
A.只要在室內放一盆水 B.向地勢低的地方撤離 C.觀察風向,順風撤離 D.用濕毛巾或蘸有純堿水的毛巾捂住口鼻撤離 組卷:316引用:27難度:0.9 -
9.下列關于碳酸氫鈉(NaHCO3)的敘述中,不正確的是( )
A.可溶于水 B.溶液顯堿性 C.受熱不分解 D.能與鹽酸反應 組卷:3引用:1難度:0.6 -
10.下列反應不屬于氧化還原反應的是( )
A.2Al+Fe2O3 Al2O3+2Fe高溫B.2Mg+CO2 2MgO+C點燃C.CuSO4+Fe=Cu+FeSO4 D.SiO2+CaO CaSiO3高溫組卷:1引用:1難度:0.9
二、填空題(共4題,共50分)
-
30.某興趣小組用圖1所示實驗裝置(部分夾持儀器已略去)制取并探究Cl2的性質,裝置(I)中發生反應的化學方程式為:MnO2+4HCl(濃)
MnCl2+Cl2+2H2O。△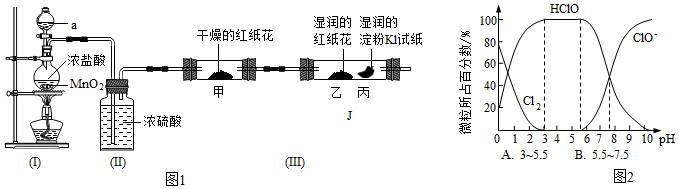
[實驗探究]
(1)裝置(I)中儀器a的名稱是;
(2)裝置(Ⅱ)中濃硫酸的作用是;
(3)實驗進行一段時間后,裝置(m)中的實驗現象與分析:
①對甲、乙兩處紅紙花顏色變化的描述正確的是(填標號)。
A.甲不褪色、乙褪色
B.甲褪色,乙不褪色
②對比甲、乙兩處實驗現象,可知具有漂白性的物質是(填“Cl2”或“HClO”)。
③丙處淀粉KI試紙變為(“藍色”或“紅色”)、某中Cl2和KI發生反應,補充完整下面的化學方程式:Cl2+2KI═2KCl+。
(4)從實驗安全和環境保護的角度考慮,該實驗存在的一個明顯缺陷是。
(5)用8.7gMnO2固體與足量濃鹽酸反應,可生成Cl2氣體體積(標準狀況下)理論上最多為L。(已知MnO2的摩爾質量為87g?mol-1)
[知識應用]Cl2常用于飲用水消毒。Cl2溶于水得到氯水,氯水中HClO的濃度越大殺菌能力越強。
(6)已知25℃時,氯水中Cl2(溶于水的氧氣分子)、HClO、ClO-三種微粒所占百分數與pH的關系如圖2。則用Cl2處理飲用水時,溶液的pH最佳控制范圍是(填標號)。組卷:21引用:1難度:0.5 -
31.實驗室里常用濃鹽酸與二氧化錳反應來制取少量的氯氣,反應的化學方程式為:
MnO2+4HCl (濃)MnCl2+Cl2↑+2H2O,取一定量的濃鹽酸使其與二氧化錳發生反應,產生的氯氣在標準狀況下的體積為22.4L.請回答下列問題:△
(1)該反應中氧化劑和還原劑的物質的量之比是;
(2)用雙線橋法表示該反應電子轉移的方向和數目;
(3)實驗室備用的濃鹽酸質量分數為36.5%,密度為1.19g?cm-3.為使用方便,請計算出該濃鹽酸的物質的量濃度為mol/L.組卷:31引用:4難度:0.3


