2019-2020學年四川省廣安市代市中學高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共16小題,每小題3分,共48分,每題均只有一個正確選項)
-
1.廚房中有很多調味品,它們可以補充食品在加工過程中失去的味道、增強原有的味道或添加一些額外的味道。下列說法不正確的是( )
A.醋能增加食品的酸味,還具有防腐作用 B.人體需控制食鹽攝入量,以降低患高血壓的風險 C.味精的主要成分是谷氨酸的鈉鹽,谷氨酸屬于氨基酸 D.白砂糖的主要成分是蔗糖,蔗糖屬于天然高分子化合物 組卷:137引用:6難度:0.7 -
2.用化學用語表CH4+Cl2
CH3Cl+HCl中的相關微粒,其中錯誤的是( )光照A.Cl的原子結構示意圖 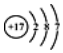
B.HCl的電子式H:Cl C.CH4的比例模型 
D.中子數為20的氯原子 Cl3717組卷:4引用:2難度:0.7 -
3.下列關于周期表的說法正確的是( )
A.第ⅠA族的元素都為金屬元素 B.在周期表中金屬與非金屬分界線附近尋找合成農藥的元素 C.過渡元素全部都是副族元素 D.周期表分為7個主族、7個副族、1個0族和1個Ⅷ族 組卷:4引用:2難度:0.6 -
4.航天飛船可用肼(N2H4)作動力源。已知液態肼和液態過氧化氫反應時放出大量熱量,下列說法錯誤的是( )
A.1mol肼(N2H4)分子中含有4mol N-H鍵 B. 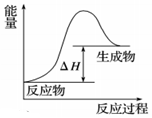 該反應中的熱量變化如圖所示
該反應中的熱量變化如圖所示C.該反應的反應物總鍵能小于生成物總鍵能 D.該反應的化學方程式為:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g),其產物對環境無污染 組卷:38引用:2難度:0.7 -
5.設NA表示阿伏加德羅常數的值,下列說法正確的是( )
A.1mol苯分子中含 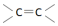 鍵數目為3NA
鍵數目為3NAB.標準狀況下,11.2L CCl4 中含有的共價鍵數目為2NA C.1mol乙烯和乙醇的混合物完全燃燒時消耗O2的分子數為3NA D.常溫常壓下,15g甲基含有的電子總數為10NA 組卷:12引用:1難度:0.8 -
6.硒(Se)被譽為“生命的奇效元素”,富硒食品倍受追捧。已知硒元素與氧元素同族,與鈣元素同周期。下列關于硒的描述錯誤的是( )
A.原子序數是24 B.氣態氫化物化學式是 H2Se C.最高價氧化物是SeO3,是酸性氧化物 D.原子半徑比硫原子的原子半徑大 組卷:3引用:1難度:0.6 -
7.金屬的冶煉就是將金屬元素從它的化合物中還原出來,下列說法錯誤的是( )
A.可用熱分解法獲得金屬銀 B.利用赤鐵礦冶煉金屬鐵,可用一氧化碳、氫氣等作還原劑 C.鈉、鎂、鋁等活潑的金屬,都可以用電解其熔融的氯化物來冶煉 D.鋁熱反應可以用于冶煉難熔的相對較不活潑的金屬,也可以用于焊接鋼軌 組卷:45引用:4難度:0.7
一、第二部分(非選擇題共52分)
-
20.合成氨工業N2(g)+3H2(g)?2NH3(g)在國民經濟中占有重要地位,某溫度下,向體積固定的1L密閉容器中充入1mol N2(g)和3mol H2(g),測得不同時刻反應前后的壓強關系如表所示:
(1)0-15min內,用H2表示的平均反應速率為v(H2)=時間/min 5 10 15 20 25 30 壓強比值P 后/P 前 0.98 0.88 0.80 0.75 0.75 0.75 mol?L-1?min-1。
(2)達到平衡時N2的轉化率為。
(3)如圖為不同條件下反應速率隨時間的變化情況,則a時刻改變的條件可能是。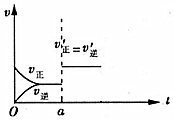
(4)一定條件下的密閉容器中,該反應達到平衡后要提高 H2的轉化率,可以采取的措施有。
A.增加N2的濃度
B.加入催化劑
C.分離出NH3
D.增加H2的濃度組卷:3引用:1難度:0.6 -
21.常見鋅錳干電池因含有汞、酸或堿等,廢棄后進入環境將造成嚴重危害.某化學興趣小組擬采用如下處理方法回收廢電池中的各種資源.
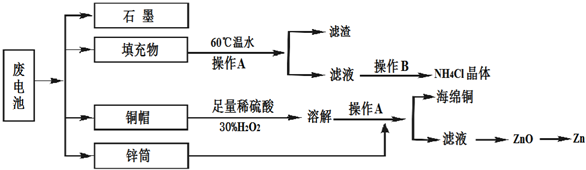
(1)填充物用60℃溫水溶解,目的是.
(2)操作A的名稱為.
(3)銅帽溶解時加入H2O2的目的是(用化學方程式表示).
銅帽溶解完全后,可采用方法除去溶液中過量的H2O2.
(4)堿性鋅錳干電池電解質為KOH,總反應Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其負極的電極反應式為.
(5)濾渣的主要成分為含錳混合物,向含錳混合物中加入一定量的稀硫酸、稀草酸,并不斷攪拌至無氣泡為止.主要反應為
2MnO(OH)+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O.
①當1mol MnO2參加反應時,共有mol電子發生轉移.
②MnO(OH)與濃鹽酸在加熱條件下也可發生反應,試寫出該反應的化學方程式:.組卷:29引用:4難度:0.3


