2021-2022學年遼寧省大連103中高一(下)期中化學試卷
發布:2024/11/29 19:30:2
一、選擇題(本題共15個小題,每小題3分,每小題只有一個選項符合題意)
-
1.新冠肺炎疫情出現以來,一系列舉措體現了中國力量。在各種防護防控措施中,化學知識起到了重要作用。下列有關說法錯誤的是( )
A.使用醫用酒精殺菌消毒的過程中只發生了物理變化 B.使用84消毒液殺菌消毒是利用其強氧化性 C.N95型口罩的核心材料是聚丙烯絲,屬于有機高分子材料 D.醫用防護服的核心材料是微孔聚四氟乙烯薄膜,其單體是CF2=CF2 組卷:12引用:4難度:0.6 -
2.下列有關化學用語表示正確的是( )
A.葡萄糖的最簡式:C6 H12O6 B.羥基的電子式: 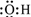
C.乙酸乙酯的分子式:C4H8O2 D.乙烯的球棍模型: 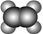 組卷:5引用:1難度:0.7
組卷:5引用:1難度:0.7 -
3.化學要研究如何合理、高效地利用金屬礦物。下列金屬的冶煉方法與工業上冶煉鋁相同的是( )
A.Fe+CuSO4=FeSO4+Cu B.2NaCl(熔融) 2Na+Cl2↑電解C.Fe2O3+3CO 2Fe+3CO2高溫D.2Ag2O 4Ag+O2↑△組卷:65引用:4難度:0.8 -
4.下列關于化學反應與能量變化的說法正確的是( )
A.需要加熱才能發生的反應一定是吸熱反應 B.水汽化需要吸收能量,所以水汽化屬于吸熱反應 C.對于吸熱反應,生成物總能量一定低于反應物總能量 D.X(s)═Y(s)是放熱反應,則Y比X穩定 組卷:13引用:2難度:0.7 -
5.NA為阿伏加德羅常數的值,下列敘述錯誤的是( )
A.1mol乙烯分子含有的極性共價鍵數為4NA B.1mol甲烷完全燃燒轉移的電子數為8NA C.1L0.1mol?L-1的乙酸溶液中含H+的數量為0.1NA D.7g乙烯的氣體中含有原子數1.5NA 組卷:1引用:1難度:0.6 -
6.微型紐扣電池在現代生活中有廣泛應用。一種銀鋅紐扣電池的電極分別為Ag2O和Zn,電解質溶液為KOH,電極反應為Zn+2OH--2e-═ZnO+H2O和Ag2O+H2O+2e-═2Ag+2OH-。下列說法錯誤的是( )
A.在使用過程中,電池負極區溶液的堿性減弱 B.使用過程中,電子由Zn極經外電路流向Ag2O極 C.電池總反應為Ag2O+Zn═2Ag+ZnO D.Zn是負極發生還原反應,Ag2O是正極發生氧化反應 組卷:50引用:5難度:0.6
二、非選擇題
-
 18.CH4、CO等都是重要的能源,也是重要的化工原料。
18.CH4、CO等都是重要的能源,也是重要的化工原料。
(1)一定條件下,甲烷與水蒸氣發生反應:CH4(g)+H2O(g)?CO(g)+3H2(g),工業上可利用此反應生產合成氨原料氣H2。
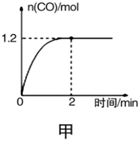
①一定溫度下,向2L恒容密閉容器中充入1.6molCH4和2.4molH2O(g)發生上述反應,CO(g)的物質的量隨時間的變化如圖甲所示。0~2min內的平均反應速率v(H2)=。平衡時CH4的轉化率為。
②下列措施能加快反應速率的是(填字母)。
A.恒壓時充入He
B.升高溫度
C.恒容時充入CH4
D.及時分離出CO
③第1分鐘時v正(CO)第2分鐘時v逆(CO)(填“>”“<”“=”或“無法比較”)。
④下列能說明上述反應達到平衡狀態的是(填字母)。
a.v逆(CH4)=3v正(H2)
b.恒溫恒容時,容器內混合氣體的密度保持不變
c.CH4(g)、H2O(g)濃度保持不變
d.CH4(g)、H2O(g)、CO(g)、H2(g)的物質的量之比為1:1:1:3
e.斷開3molH-H鍵的同時斷開2molO-H鍵
(2)被譽為改變未來世界的十大新科技之一的燃料電池具有無污染、無噪音、高效率的特點。如圖乙為氫氧燃料電池的結構示意圖,電解質溶液為KOH溶液,電極材料為疏松多孔石墨棒。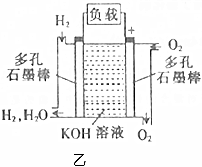
⑤輸入氫氣的一極為極。
⑥寫出正極反應式:。組卷:44引用:1難度:0.5 -
19.海水是巨大的資源寶庫,甲工廠從海水中提取食鹽和溴的工藝流程如圖:
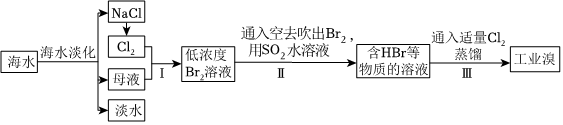
已知:Br2的沸點為59℃,微溶于水,有毒。
(1)海水淡化得到淡水的主要有。(寫出兩種即可)
(2)為了將粗鹽(含雜質Mg2+、、Ca2+)提純,加入的試劑順序可行的是SO2-4。
A.NaOH溶液→Na2CO3溶液→BaCl2溶液→過濾后加鹽酸
B.BaCl2溶液→NaOH溶液→Na2CO3溶液→過濾后加鹽酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→過濾后加鹽酸
D.Na2CO3溶液→NaOH溶液→BaCl2溶液→過濾后加鹽酸
(3)Br2可用熱空氣吹出,其原因是。
(4)步驟Ⅱ在此流程中作用是。寫出步驟Ⅱ的離子反應方程式。
(5)乙工廠在甲工廠的流程設計基礎上進行了改進,步驟Ⅱ中用Na2CO3溶液吸收空氣中Br2。充分反應后,得到含NaBr、NaBrO3等物質的混合溶液。步驟Ⅲ向所得溶液中滴加稀硫酸,蒸餾即得到液溴。請寫出步驟Ⅲ滴加稀硫酸的離子方程式。
(6)與甲工廠相比,乙工廠設計流程的優點為。組卷:11引用:1難度:0.7


