2020年北京市高考化學仿真模擬試卷(6月份)
發布:2024/10/26 19:30:2
一、選擇題本部分共14題,每題3分,共42分.在每題列出的四個選項中,選出最符合題目要求的一項.
-
1.化學在疫情防控中發揮著重要作用,下列說法不正確的是( )
A.二氧化氯可用于自來水消毒 B.醫用消毒酒精是95%的乙醇溶液 C.醫用防護口罩的材料之一是聚丙烯,聚丙烯屬于高分子材料 D.84消毒液和酒精混合消毒作用減弱,可能發生了復雜的化學反應 組卷:70引用:4難度:0.6 -
2.在二氯化鉑的HCl溶液中,通入乙烯氣體,再加入KCl可得K[Pt(C2H4)Cl3]?H2O(蔡氏鹽),相關表示正確的是( )
A.中子數為117,質子數為78的鉑原子: Pt195117B.氯離子的結構示意圖: 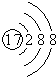
C.乙烯的結構簡式:CH2CH2 D.KCl的電子式: 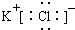 組卷:239引用:4難度:0.9
組卷:239引用:4難度:0.9 -
3.化學在生產和生活中有著廣泛的應用.下列對應關系錯誤的是( )
選項 化學性質 實際應用 A 鎂鋁合金導熱性能好 鎂鋁合金常用于制窗框 B FeCl3的氧化性大于CuCl2 FeCl3溶液用于蝕刻銅制線路板 C SO2具有還原性 海水制溴工業中用SO2的水溶液吸收Br2 D 鋁易與氧結合且該反應放熱 鋁用于冶煉Cr、Mn等難熔金屬 A.A B.B C.C D.D 組卷:23引用:6難度:0.7 -
4.海水是巨大的資源寶庫,下列關于海水綜合利用的說法不正確的是( )
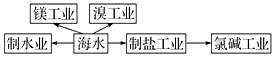
A.海水制淡水主要有蒸餾法、離子交換法等 B.氯堿工業中在陽極上產生Cl2 C.海水提取溴時,富集溴一般先用空氣和水蒸氣吹出單質溴,再用SO2將其氧化吸收 D.工業上用電解熔融MgCl2的方法制取金屬鎂 組卷:49引用:1難度:0.5 -
5.設NA為阿伏加德羅常數的值。下列說法正確的是( )
A.1L 0.1mol?L-1NaClO溶液中含有ClO-的數目為0.1NA B.密閉容器中1mol PCl3與1mol Cl2充分反應,生成PCl5分子的數目為NA C.1L 0.1mol?L-1NaHSO4溶液中含有的陽離子數目為0.1NA D.將1mol CH3COONa溶于稀醋酸中使溶液呈中性,溶液中含CH3COO-數目為NA 組卷:90引用:2難度:0.8 -
6.在給定條件下,下列選項所示物質間轉化均能實現的是( )
A.C(焦炭) CO2SiO2高溫CaCO3CaCl2B.MgO(s) MgCl2(aq)HClaqMg(s)電解C.FeS2(s) Fe2O3(s)O2高溫Fe(s)CO高溫D.CH3CH2Br CH2=CH2NaOH/H2O一定條件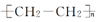 組卷:68引用:1難度:0.7
組卷:68引用:1難度:0.7
二、非選擇題本部分共5題,共58分.
-
18.常溫下,在鎂屑和無水乙醚的混合體系中,滴加鹵代烷,反應后得到的有機鎂化合物稱為格氏試劑。制備的格氏試劑不需要分離就可直接用于有機合成,是重要的有機合成中間體。反應原理為:
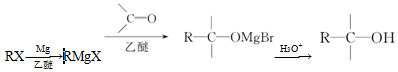 利用A(
利用A(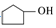 )來合成
)來合成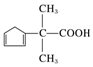 的流程圖如圖所示:
的流程圖如圖所示:
(1)物質A的名稱為;A→B的反應類型是。
(2)寫出由A制備環戊酮(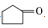 )的化學方程式。
)的化學方程式。
(3)寫出由F生成G、G生成H的化學方程式。
(4)D的同分異構體中含有六元環且能發生銀鏡反應的有種。
(5)寫出符合下列要求的I的同分異構體的結構簡式。(寫出一種即可,已知同一個C原子上不能連接2個羥基)
①芳香族化合物 ②二元醇 ③分子中有5種不同化學環境的H原子組卷:20引用:1難度:0.5 -
19.某學生對Na2SO3與AgNO3在不同 pH 下的反應進行探究.
(1)測得Na2SO3溶液 pH=10、AgNO3 溶液 pH=5.
(2)調節 pH,實驗記錄如表:
查閱資料得知:實驗 pH 現象 a 10 產生白色沉淀,稍后溶解,溶液澄清 b 6 產生白色沉淀,一段時間后,沉淀未溶解 c 2 產生大量白色沉淀,一段時間后,產生海綿狀棕黑色物質X
ⅰ.Ag2SO3:白色,難溶于水,溶于過量的Na2SO3 溶液.
ⅱ.Ag2O:棕黑色,不溶于水,能和酸反應.
該學生對 a 中的白色沉淀提出了兩種假設:
①白色沉淀為Ag2SO3
②白色沉淀為Ag2SO4,推測的依據是.
(3)取 b、c 中白色沉淀,置于Na2SO3溶液中,沉淀溶解.該同學設計實驗確認了白色沉淀不是Ag2SO4.實驗方法是:另取Ag2SO4固體置于溶液中,未溶解.
(4)將 c 中 X 濾出、洗凈,為確認其組成,實驗如下:
Ⅰ.向 X 中滴加稀鹽酸,無明顯變化.
Ⅱ.向 X 中加入過量濃硝酸,產生紅棕色氣體.
Ⅲ.用Ba(NO3)2、BaCl2溶液檢驗Ⅱ中反應后的溶液,前者無明顯變化,后者產生白色
沉淀.
①實驗Ⅰ的目的是.
②根據上述現象,分析 X 的成分是.
③Ⅱ中反應的化學方程式是.
(5)該同學綜合以上實驗,分析 X 產生的原因是:隨著酸性的增強,體系的還原性強.組卷:225引用:2難度:0.1


