2022-2023學年浙江省寧波市九校高一(下)期末化學試卷
發(fā)布:2024/7/27 8:0:9
一、選擇題(本大題有25小題,每小題2分共50分。每小題均只有一個選項符合題意)
-
1.根據(jù)物質(zhì)的組成對物質(zhì)進行分類,NaHCO3屬于( )
A.酸 B.堿 C.鹽 D.氧化物 組卷:93引用:2難度:0.9 -
2.下列物質(zhì)中,能夠?qū)щ姷碾娊赓|(zhì)是( )
A.二氧化硅 B.鹽酸 C.熔融的氧化鋁 D.銅 組卷:128引用:1難度:0.8 -
3.儀器名稱為圓底燒瓶的是( )
A. 
B. 
C. 
D.  組卷:15引用:1難度:0.8
組卷:15引用:1難度:0.8 -
4.下列有關(guān)化學用語表示正確的是( )
A.聚丙烯的結(jié)構(gòu)簡式: 
B.乙酸的空間填充模型: 
C.乙炔分子的球棍模型: 
D.HClO的結(jié)構(gòu)式:H-Cl-O 組卷:10引用:1難度:0.7 -
5.下列說法正確的是( )
A.用海水為原料,經(jīng)一系列過程制得氧化鎂固體,H2還原得鎂 B.食品中添加適量的二氧化硫可以起到漂白、防腐和抗氧化的作用 C.二氧化硫、氮氧化物以及它們在大氣中發(fā)生反應后的生成物溶于水會形成酸雨,常溫下,pH小于7的雨水稱之為酸雨 D.滴滴涕(DDT)有較高和較寬廣的殺蟲活性,對人體的急性毒性較低,故可全面推廣、生產(chǎn)、使用 組卷:26引用:2難度:0.7 -
6.關(guān)于反應3LiFePO4+13HNO3═3LiNO3+3Fe(NO3)3+3H3PO4+NO↑+2H2O,下列說法不正確的是( )
A.每生成0.5molNO,則HNO3失去1.5mol電子 B.LiFePO4是還原劑 C.氧化產(chǎn)物和還原產(chǎn)物的物質(zhì)的量之比為3:1 D.若反應中轉(zhuǎn)移3mol電子,被還原的硝酸的物質(zhì)的量為1mol 組卷:101引用:2難度:0.5 -
7.下列說法正確的是( )
A.1H2O和2H2O互為同位素 B.SO2和SO3互為同素異形體 C.乙酸和硬脂酸屬于同系物 D. 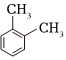 和
和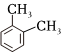 互為同分異構(gòu)體組卷:22引用:2難度:0.8
互為同分異構(gòu)體組卷:22引用:2難度:0.8 -
8.下列說法不正確的是( )
A.中國華為集團自主研發(fā)的“麒麟”芯片生產(chǎn)時需要用到硅 B.工業(yè)上可以用鐵和氯化銅溶液制印刷電路板 C.從海水中制得的氯化鈉除了供食用,還作為化工原料用于生產(chǎn)純堿、燒堿等 D.硬鋁是一種鋁合金,是制造飛機和宇宙飛船的理想材料 組卷:25引用:1難度:0.7 -
9.下列關(guān)于化學反應熱效應描述正確的是( )
A.已知:H2(g)+Cl2(g)═2HCl(g) ΔH=-184.6kJ?mol-1,則每生成1molHCl,放出的熱量為184.6kJ B.已知:2SO2(g)+O2(g)?2SO3(g) ΔH=-198kJ?mol-1,則在一定條件下,2molSO2和1molO2充分反應后,釋放的熱量為198kJ C.已知:25℃、101kPa時,2C(s)+O2(g)═2CO(g) ΔH=-221kJ?mol-1,則C的燃燒熱為110.5kJ?mol-1 D.已知:C(石墨,s)?C(金剛石,s) ΔH=+1.5kJ?mol-1,可判斷石墨比金剛石更穩(wěn)定 組卷:125引用:1難度:0.5 -
10.下列有關(guān)實驗的說法中正確的是( )
A.實驗室電器設(shè)備著火,可用水進行滅火 B.使用完后的藥品如KMnO4、KClO3、Na2O2等固體不能隨便丟棄 C.實驗室采用加熱氯化銨固體,用堿石灰除去氯化氫的方法制備氨氣 D.用容量瓶配制溶液,定容時若加水超過刻度線,立即用滴管吸出多余液體 組卷:9引用:1難度:0.7
非選擇題部分
-
29.不同濃度的硫酸與鋅反應時,硫酸可以被還原為SO2,也可被還原為氫氣。某校研究性學習小組擬設(shè)計實驗驗證這一事實,并進行數(shù)據(jù)測定和相關(guān)計算。

請回答:
(1)橡膠管的作用是什么?。
(2)按圖組裝完裝置后,在加藥品前欲檢查裝置的氣密性,應如何操作?。
(3)寫出圓底燒瓶中可能發(fā)生的化學反應方程式。
(4)若燒瓶中投入ag鋅且完全反應,氫氧化鈉溶液洗氣瓶增重bg,量氣管中收集到VmL氣體(標準狀況),請用一個代數(shù)式表示出a,b,V之間的關(guān)系。
(5)反應結(jié)束后,為了準確測量氣體體積,讀數(shù)時視線應與液面最低處相平外,若量氣管右側(cè)液面高于左側(cè)液面,則的數(shù)值n(H2)n(SO2)(填“偏大”、“偏小”或“無影響”)。組卷:25引用:1難度:0.5 -
30.完成下列問題:
(1)已知20℃下,飽和食鹽水的質(zhì)量分數(shù)為26.5%,密度為1.17g/mL,則該飽和食鹽水的物質(zhì)的量濃度為mol?L-1。
(2)向27.2g由Fe和Fe2O3組成的固體混合物加入2L一定濃度的稀硫酸后固體恰好溶解,可收集到標準狀況下氣體2.24L,再向反應后的溶液中滴入KSCN溶液,無明顯現(xiàn)象(忽略反應前后溶液的體積變化),反應后溶液中FeSO4的物質(zhì)的量濃度為。
(3)100mL0.200mol?L-1CuSO4溶液與1.95g鋅粉在量熱計中充分反應。已知:反應Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)的ΔH=-209kJ?mol-1,反應前后,溶液的比熱容均近似為4.18J?g-1?℃-1、溶液的密度均近似為1.00g?cm-3,忽略溶液體積、質(zhì)量變化和金屬吸收的熱量。實驗測得反應前溫度為20.1℃,請計算反應后測得的最高溫度為℃。組卷:43引用:1難度:0.5


