2010年第二十屆“天原杯”全國初中學生化學素質和實驗能力競賽(河南賽區)初賽試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括20小題,每題1分,共20分,每題只有一個選項符合題意)
-
1.環保部門為了使城市生活垃圾得到合理利用,近年來逐步實施了對生活垃圾分類投放的辦法,其中塑料袋、廢紙、舊橡膠制品等屬于( )
A.非金屬單質 B.鹽類 C.有機物 D.無機物 組卷:23引用:4難度:0.5 -
2.2009年12月在哥本哈根召開了聯合國氣候變化大會,“低碳生活”成為熱門話題,下列減緩全球氣候變暖的對策中,不恰當的是( )
A.提倡乘坐公共交通工具、騎自行車或步行的方式出行 B.廣泛使用一次性筷子、一次性塑料袋 C.在生產和生活中提倡使用節能技術和節能用具 D.開發無污染的太陽能、風能、地熱能等 組卷:25引用:15難度:0.9 -
3.下列各組物質發生的變化,均屬于化學變化的是( )
A.木炭在空氣中燃燒,發光、放熱;燈泡通電,發光、放熱 B.少量酒精在空氣中揮發不見了;少量酒精在空氣中燃燒后不見了 C.澄清石灰水中通入適量二氧化碳后變渾濁;澄清的飽和石灰水加熱升溫后變渾濁 D.塊狀生石灰在空氣中逐漸變為白色粉末;鎂帶在空氣中燃燒后變為白色粉末 組卷:11引用:7難度:0.9 -
4.銅和鋁是日常生活和生產中重要的金屬.鈦(Ti)有許多神奇的性能,越來越引起人們的關注,是21世紀的重要金屬之一.依據三種金屬的性質和用途,判斷下列說法錯誤的是( )
A.鋁是地殼中含量最多的金屬元素 B.將大小、厚薄相同的銅、鋁、鈦分別放入等質量、等濃度的稀鹽酸中,觀察到鈦表面緩慢放出氣泡,鋁的放出氣泡較快,而銅的無現象,由此可推測三種金屬的活動性順序為Al>Cu>Ti C.鈦或鈦合金放到海水中數年后仍光亮如初,這說明原因是金屬鈦具有很強的抗腐蝕性 D.高層建筑常采用鋁合金門窗而不采用鐵門窗,主要原因是鋁的密度小且表面易形成一層致密的氧化物薄膜 組卷:27引用:2難度:0.7 -
5.我國盛產的香料八角中存在莽草酸(化學式為C7H10O5),由它合成的達菲(化學式為C16H31O8N2P)是抗甲型H1N1流感的一種藥物.下列說法正確的是( )
A.莽草酸屬于氧化物 B.莽草酸中碳、氫、氧的質量比為7:10:5 C.達菲的相對分子質量為174 D.用莽草酸合成達菲時需要含氮的物質 組卷:14引用:2難度:0.9 -
6.將下列四種家庭常用的調味品分別放入水中,不能形成溶液的是( )
A.芝麻油 B.食鹽 C.味精 D.蔗糖 組卷:41引用:22難度:0.9 -
7.能證明分子在化學變化中可分的是( )
A.打開汽水瓶,有氣體逸出 B.10mL水與10mL酒精混合,體積小于20mL C.加熱氧化汞得銀白色汞與氧氣 D.水蒸發為水蒸氣 組卷:21引用:21難度:0.9 -
8.下列生活小實驗不能成功的是( )
A.用食醋除去水壺中的水垢 B.用灼燒的方法區分羊毛和滌綸 C.用紫卷心菜等自制酸堿指示劑 D.用食鹽水區分硬水和飲用純凈水 組卷:9引用:2難度:0.9 -
9.使用滅火器撲滅圖書檔案、貴重設備、精密儀器等火災時,最好不要留下任何痕跡,下列滅火器中最適宜的是( )
A.干粉滅火器 B.泡沫滅火器 C.高壓水槍 D.液態二氧化碳滅火器 組卷:53引用:4難度:0.9 -
10.可以用加熱氯酸鉀和二氧化錳混合物的方法在實驗室制取氧氣。下列是反應生成氧氣和氯化鉀的質量與反應時間的關系坐標圖,其中合理的是( )
A. 
B. 
C. 
D.  組卷:1083引用:29難度:0.9
組卷:1083引用:29難度:0.9 -
11.某種元素的化合價在化學反應前后發生了變化,則該反應為氧化還原反應.據此可判斷下列化學反應屬于氧化還原反應的是( )
A.Fe2O3+3H2SO4=Fe2(SO4)3+3H2O B.Fe2O3+3CO═2Fe+3CO2 C.Na2CO3+2HCl=2NaCl+H2O+CO2↑ D.H2CO3=H2O+CO2↑ 組卷:18引用:5難度:0.9 -
12.鑒別下列各組物質,選用試劑或方法(括號內)正確的是( )
A.水和過氧化氫溶液(二氧化錳) B.純堿和燒堿溶液(酚酞) C.生石灰和氫氧化鈉固體(水) D.CO2和N2(燃著的木條) 組卷:8引用:4難度:0.5
四、綜合應用題(本題包括2個小題,每小題10分,共20分)
-
35.在通常狀況下,氯氣是一種黃綠色氣體,密度比空氣大,易溶于水。在工業上、實驗室中可以制作氯氣,用來研究氯氣的性質,并將其廣泛用于實際生產和生活中。
(1)在工業上,制取氯氣的主要工藝流程如下:
①利用風吹日曬可以從海水中提取粗鹽,該過程主要發生(“物理”或“化學”)變化。
②要除去食鹽水中混有的少量泥沙,可選擇的操作方法是。
③氯化鈉溶液在通電條件下發生反應的化學方程式為。
(2)在實驗室中,可以用加熱二氧化錳和濃鹽酸來制取氯氣,可采用如圖裝置制取氯氣并測量產生Cl2的體積。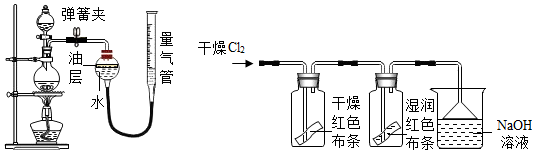
①能采用該氣體發生裝置的理由是。
②該裝置中油層的作用是。
(3)氯氣在常溫下能分別與水、堿類等物質發生反應,并可以產生具有殺菌消毒、漂白(是有色物質褪色)等作用的物質。
①氯氣與氫氧化鈉溶液反應的化學方程式為Cl2+2NaOH=NaCl+NaClO+H2O.氯氣與石灰乳反應可制漂白粉,有關化學方程式為。
②氯氣和水反應的原理是:Cl2+H2O=HCl+HclO.為了證明把氧氣通入水的過程中,起漂白作用的物質是次氯酸(化學式為HClO),小明同學進行了如圖所示的探究實驗。你認為小明設計的方案能夠達到目的嗎?若能,請說明理由。若不能,請補充實驗幫助小明達到實驗目的(寫出實驗步驟、現象及結論)。
(4)請計算:吸收14.2g氯氣,需要消耗20%的氫氧化鈉溶液多少克?組卷:41引用:1難度:0.5 -
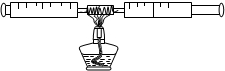 36.(1)課外活動小組對空氣中氧氣含量的測定做了如下實驗:在由兩個注射器組成的密閉系統內有50mL空氣,如圖.然后給裝有銅絲的玻璃管加熱.同時交替推動兩個注射器活塞,至玻璃管內銅絲變黑且較長時間內無進一步變化時停止.停止加熱后,待冷卻至室溫將氣體全部推至一個注射器內.
36.(1)課外活動小組對空氣中氧氣含量的測定做了如下實驗:在由兩個注射器組成的密閉系統內有50mL空氣,如圖.然后給裝有銅絲的玻璃管加熱.同時交替推動兩個注射器活塞,至玻璃管內銅絲變黑且較長時間內無進一步變化時停止.停止加熱后,待冷卻至室溫將氣體全部推至一個注射器內.
①驗結束后,注射器內空氣的體積減少了約mL,這是因為
②在實驗的加熱過程中,交替緩慢推動兩個注射器的目的是.
③上述實驗只是粗略測定空氣中氧氣含量的一種方法,你認為造成該實驗不夠精確的可能原因是.
(2)課外活動小組發現紅熱的銅絲變黑后,為了回收再利用銅絲,在研究如何除去黑色物質的討論中,制定了下列方案.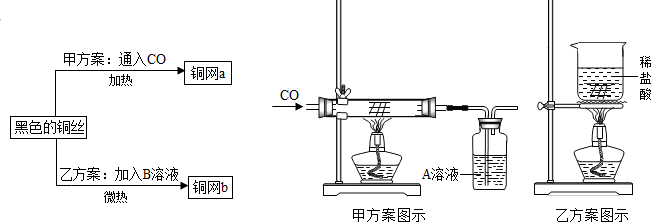
①乙方案的燒杯中發生反應的化學方程式為.
兩種方案相比,方案更好,其原因是
②若采用甲、乙兩種方案處理此變成黑色的銅絲,并且充分反應,則回收的銅絲a的質量(填“<”、“>”、“=”)銅絲b的質量.請通過分析和計算,采用甲、乙兩種方案分別回收銅絲,所得到銅絲的質量理論上最多相差多少克?(提示:假設該實驗中所取空氣中氧氣的密度為1.30g/L.要求:計算結果精確到0.01g.)組卷:192引用:4難度:0.3


