2013-2014學年河北省保定市高陽中學高二(上)第七次周練化學試卷
發布:2024/12/17 10:0:2
一、選擇題(每小題3分,共45分)
-
1.對于A2+3B2?2AB3反應來說,以下反應速率表示反應最快的是( )
A.v(AB3)=0.5 mol/(L?min) B.v(B2)=0.6 mol/(L?min) C.v(A2)=0.4 mol/(L?min) D.無法判斷 組卷:21引用:8難度:0.9 -
2.在一定溫度下的恒容密閉容器中,當下列哪些物理量不再發生變化時,表明下述反應:A(g)+2B(g)?C(g)+2D(g)已達到平衡狀態( )
A.混合氣體的壓強 B.混合氣體的密度 C.各氣體的物質的量 D.氣體的總物質的量 組卷:38引用:6難度:0.7 -
3.下列是4位同學在學習“化學反應的速率和化學平衡“一章后,聯系工業生產實際所發表的觀點,你認為不正確的是( )
A.化學反應速率理論是研究怎樣在一定時間內快出產品 B.化學平衡理論是研究怎樣使用有限原料多出產品 C.化學反應速率理論是研究怎樣提高原料轉化率 D.化學平衡理論是研究怎樣使原料盡可能多地轉化為產品 組卷:356引用:61難度:0.9 -
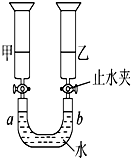 4.常溫常壓下,注射器甲中裝有NO2氣體,注射器乙中裝有相同體積的空氣,注射器與U 形管連通,如圖所示,打開兩個止水夾,同時向外拉兩注射器的活塞,且拉動的距離相等,將會看到U形管中液面(不考慮此條件下NO2與水的反應)( )
4.常溫常壓下,注射器甲中裝有NO2氣體,注射器乙中裝有相同體積的空氣,注射器與U 形管連通,如圖所示,打開兩個止水夾,同時向外拉兩注射器的活塞,且拉動的距離相等,將會看到U形管中液面(不考慮此條件下NO2與水的反應)( )A.a端上升,b端下降 B.a端下降,b端上升 C.U形管中液面無變化 D.無法判斷 組卷:122引用:11難度:0.7 -
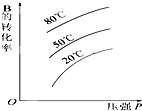 5.可逆反應A(s)+B?C達到平衡后,B的轉化率與壓強、溫度的關系如圖所示.下列說法正確的是( )
5.可逆反應A(s)+B?C達到平衡后,B的轉化率與壓強、溫度的關系如圖所示.下列說法正確的是( )A.B是固體,C是固體,正反應是吸熱反應 B.B是氣體,C是固體,正反應是吸熱反應 C.B是氣體,C是固體,正反應是放熱反應 D.B、C都是氣體,正反應是放熱反應 組卷:37引用:9難度:0.7 -
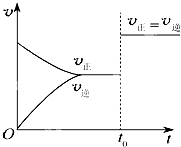 6.可逆反應aX(g)+bY(g)?cZ(g)在一定溫度下的密閉容器內達到平衡后,t0時改變某一外界條件,化學反應速率(v)-時間(t)圖象如圖.下列說法正確的是( )
6.可逆反應aX(g)+bY(g)?cZ(g)在一定溫度下的密閉容器內達到平衡后,t0時改變某一外界條件,化學反應速率(v)-時間(t)圖象如圖.下列說法正確的是( )A.若a+b=c,則t0時只能是增大反應體系的壓強 B.若a+b=c,則t0時只能是加入催化劑 C.若a+b≠c,則t0時只能是加入催化劑 D.若a+b≠c,則t0時只能是增大體系的壓強 組卷:129引用:27難度:0.7 -
7.化學平衡常數(K)是化學反應限度的一個重要參數,該常數表示的意義是可逆反應進行的程度,K值越大,表示的意義錯誤的是( )
A.溫度越高 B.反應物濃度越小 C.反應進行的越完全 D.生成物濃度越大 組卷:66引用:6難度:0.9
二、非選擇題(共7小題,滿分55分)
-
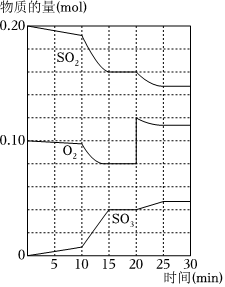 21.在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+O2 (g)?2SO3(g) (△H<0)
21.在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+O2 (g)?2SO3(g) (△H<0)
(1)寫出該反應的化學平衡常數表達式 K=
(2)降低溫度,該反應K值,二氧化硫轉化率,化學反應速度(以上均填增大、減小或不變)
(3)600℃時,在一密閉容器中,將二氧化硫和氧氣混合,反應過程中SO2、O2、SO3物質的量變化如圖,反應處于第一次平衡狀態的時間是.
(4)據圖判斷,反應進行至20min時,曲線發生變化的原因是(用文字表達),10-15min的曲線變化的原因能是(填寫編號)
a.加了催化劑 b.縮小容器體積 c.降低溫度 d.增加SO3的物質的量.組卷:323引用:29難度:0.5 -
22.在密閉容器中進行如下反應:2SO2(g)+O2(g)═2SO3(g)
SO2的起始濃度是0.4mol/L,O2的起始濃度是1mol/L.當SO2的轉化率為80%時,反應達到平衡狀態.
(1)求該反應的平衡常數.
(2)若將平衡時反應混合物的壓強增大1倍,平衡將如何移動?
(3)若將平衡時反應混合物的壓強減小1倍,平衡將如何移動?
(4)平衡時保持體積不變,向平衡混合氣體中充入稀有氣體Ar,使體系總壓變為原來的3倍,平衡又將如何移動?組卷:11引用:2難度:0.3


