2019-2020學年山西省長治市名校高二(下)期末化學試卷
發(fā)布:2024/12/7 13:0:2
一.選擇題(本題包括14小題,每小題3分,共42分。每小題只有一個選項符合題意)
-
1.2020年6月5日是第49個世界環(huán)境日,其主題為“關愛自然,刻不容緩”。下列做法與該主題相符合的是( )
A.大量生產(chǎn)和使用一次性超薄塑料袋 B.推廣使用含Na5P3O10的洗衣粉 C.推進垃圾分類管理,實現(xiàn)資源回收利用 D.過度開采自然資源,滿足快速發(fā)展需求 組卷:1引用:1難度:0.8 -
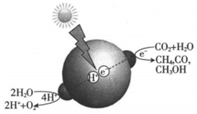 2.利用“人工樹葉”可將CO2和H2O轉變?yōu)镃H4、O2、CO及CH3OH。下列說法正確的是( )
2.利用“人工樹葉”可將CO2和H2O轉變?yōu)镃H4、O2、CO及CH3OH。下列說法正確的是( )A.該轉變過程放出能量 B.人工樹葉將化學能轉變?yōu)楣饽?/label> C.上述物質均只含有共價鍵 D.CH3OH和H2O均為非電解質 組卷:3引用:1難度:0.8 -
3.下列化學用語表示正確的是( )
A.HClO的結構式:H-Cl-O B.35Cl的結構示意圖: 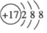
C.CH4的球棍模型: 
D.NH3的電子式: 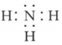 組卷:2引用:1難度:0.7
組卷:2引用:1難度:0.7 -
4.在進行滴定實驗時,圖示操作正確的是( )
A. 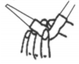
如圖所示操作為排出堿式滴定管中的氣泡B. 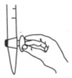
如圖所示操作為滴定時旋轉酸式滴定管的旋塞C. 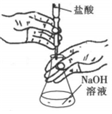
如圖所示操作為用鹽酸滴定NaOH溶液D. 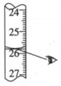
如圖所示操作為讀取滴定管讀數(shù)組卷:1引用:1難度:0.7 -
5.常溫常壓條件下,下列不能滿足組內(nèi)三種物質兩兩之間均能發(fā)生反應的選項是( )
A.N2、O2、Cl2 B.FeCl2溶液、硝酸溶液、NaOH溶液 C.SiO2、NaOH溶液、氫氟酸 D.SO2、Ca(OH)2溶液、NH4HCO3溶液 組卷:1引用:1難度:0.6 -
6.有關合成氨反應:N2+3H2
2NH3,下列說法正確的是( )催化劑加熱、加壓A.加熱或加壓均能改變該反應的化學平衡常數(shù) B.當3v正(N2)=v逆(H2)時,反應達到平衡 C.平衡時再充入H2,H2的轉化率一定增大 D.N2和H2的平衡轉化率之比一定是1:3 組卷:3引用:1難度:0.5
二、非選擇題(本題包括4小題,共58分)
-
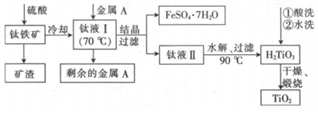 17.金屬鈦素有“太空金屬”“未來金屬”等美譽。工業(yè)上以鈦鐵礦(主要成分為FeTiO3)為原料制備二氧化鈦并得到副產(chǎn)品FeSO4?7H2O的工藝流程如圖所示。
17.金屬鈦素有“太空金屬”“未來金屬”等美譽。工業(yè)上以鈦鐵礦(主要成分為FeTiO3)為原料制備二氧化鈦并得到副產(chǎn)品FeSO4?7H2O的工藝流程如圖所示。
已知:酸溶時發(fā)生的化學方程式為FeTiO3+2H2SO4═FeSO4+TiOSO4+2H2O。
回答下列問題:
(1)TiOSO4中Ti元素的化合價為,金屬A為(填化學式)。
(2)“鈦液Ⅰ”需冷卻至70℃左右,若溫度過高會導致產(chǎn)品TiO2回收率降低,原因是。
(3)向“鈦液Ⅱ”中加入Na2CO3粉末易得到固體H2TiO3。請結合平衡移動原理和化學用語解釋其原因:。
(4)判斷H2TiO3固體已經(jīng)洗凈的實驗方案是。
(5)測定樣品中TiO2純度的方法:稱取0.20g樣品放入錐形瓶中,加入硫酸和硫酸銨的混合溶液,加強熱使其溶解;冷卻后,加入一定量的稀鹽酸得到含TiO2+的溶液;加入金屬鋁,將TiO2+全部轉化為Ti3+;待過量的金屬鋁完全溶解并冷卻后,加入KSCN溶液作指示劑,用0.10mol?L-1的NH4Fe(SO4)2溶液滴定至終點。(已知:Ti3++Fe3++H2O═TiO2++Fe2++2H+)。
①滴定至終點時的現(xiàn)象為。
②配制100mL 0.10mol?L-1NH4Fe(SO4)2溶液,需要的玻璃儀器有、、玻璃棒、燒杯等。
③重復上述操作3次,記錄實驗數(shù)據(jù)如下表,樣品中TiO2的質量分數(shù)為%,若實驗中觀察讀數(shù)時,滴定前仰視,滴定后俯視,則會導致測定結果(填“偏高”“偏低”或“無影響”)。序號 滴定前讀數(shù)/mL 滴定后讀數(shù)/mL 1 0.00 24.01 2 1.00 24.99 3 0.00 25.00 組卷:3引用:1難度:0.5 -
18.汽車尾氣(碳氫化合物、氮氧化物及一氧化碳等)是許多城市PM2.5污染的主要來源之一。
(1)在汽車尾氣系統(tǒng)中安裝催化轉換器,可有效減少尾氣中的CO、NOx,和碳氫化合物等廢氣。
已知:N2(g)+O2(g)═2NO(g)△H1
CO(g)+O2(g)═CO2(g)△H212
2NO(g)+2CO(g)═2CO2(g)+N2(g)△H3
則△H3=(用含△H1和△H2的代數(shù)式表示)。
(2)氨氧化物及一氧化碳的電化學原理分別如圖1和圖2所示: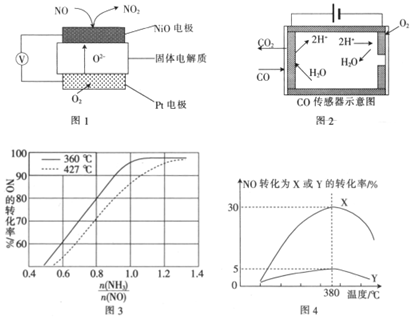
圖1中Pt電極為(填“正極”或“負極”),圖2中陽極的電極反應式為。
(3)已知:N2(g)+O2(g)?2NO(g)△H1=+180kJ?mol-1 K1=2.0×10-25
2NO(g)+O2?2NO2(g)K2=6.4×109
①汽車啟動后,氣缸內(nèi)溫度越高,單位時間內(nèi)NO的排放量越大,原因是。
②反應N2(g)+2O2(g)?2NO2(g)K=。
(4)常溫下,某PM2.5試樣溶于水得到的溶液中,各離子濃度(僅省略H+和OH-)如下:
則此時溶液的pH為離子 SO42- NO3- Cl- NH4+ 濃度/(mol?L-1) 8.35×10-4 6.80×10-3 1.50×10-4 8.61×10-3 。
(5)汽車加氨催化還原NO的主要反應為4NH3+4NO+O24N2+6H2O,測得NO的轉化率隨催化劑及溫度的變化關系如圖3所示,該反應的正反應為n(NH3)n(NO)(填“放”或“吸”)熱反應。
(6)某科研機構用鈷基催化劑催化去除柴油車模擬尾氣中的碳煙(C)和NOx。在不同溫度下,相同量的尾氣以相同的流速通過該催化劑,測得產(chǎn)物(N2、N2O)與NO轉化的相關數(shù)據(jù)如圖4所示。
380℃時,當有10mol尾氣通過該催化劑時,測得排出的氣體中含0.45mol O2和0.0525mol CO2,則圖中X的化學式為柴油車模擬尾氣 氣體(10mol) 碳煙(a mol) NO O2 He 物質的量分數(shù) 0.25% 5% 94.75% / 。組卷:5引用:1難度:0.7


