2021-2022學年吉林省長春希望高中高二(上)期末化學試卷
發布:2024/12/15 10:0:2
一、單項選擇題,本題共27小題,其中1-10題,每小題1分;11-27題,每小題1分。
-
1.下列有關電解質的說法正確的是( )
A.碳酸氫鋇是強電解質 B.乙醇是弱電解質 C.石墨能導電,所以石墨是電解質 D.食鹽水能導電,所以食鹽水是電解質 組卷:26引用:4難度:0.6 -
2.下列物質的水溶液因水解而呈酸性的是( )
A.HF B.NaHCO3 C.H2SO4 D.NH4Cl 組卷:22引用:3難度:0.8 -
3.已知銀氨溶液中存在如下平衡:[Ag(NH3)2]?Ag++2NH3.向銀氨溶液中加入或通入少量下列物質時,能使上述平衡向逆反應方向移動的是( )
A.KI B.HNO3 C.NH3 D.H2O 組卷:28引用:4難度:0.5 -
4.pH相同的①NH4Cl②HCl兩種溶液,其水的電離程度大小關系正確的是( )
A.①<② B.①>② C.①=② D.無法比較 組卷:20引用:1難度:0.8 -
5.下列材料制成的水龍頭與鐵質自來水管連接,水管生銹最快的是( )
A.鋁 B.銅 C.鐵 D.塑料 組卷:3引用:1難度:0.7 -
6.下列化學用語表示不正確的是( )
A.醋酸的電離:CH3COOH?CH3COO-+H+ B.碳酸氫鈉在水溶液中的電離:NaHCO3═Na++HCO3- C.氯化銨的水解:NH4++H2O═NH3?H2O+H+ D.碳酸鈣的溶解平衡:CaCO3(s)?Ca2+(aq)+CO32-(aq) 組卷:27引用:1難度:0.7 -
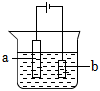 7.模擬鐵制品鍍銅的裝置如圖,下列說法正確的是( )
7.模擬鐵制品鍍銅的裝置如圖,下列說法正確的是( )A.a電極為鐵制品 B.可用CuSO4溶液作電鍍液 C.b電極上發生氧化反應 D.電鍍過程中,溶液中Cu2+濃度不斷減小 組卷:92引用:8難度:0.8 -
8.下列因素不可能影響化學平衡移動的是( )
A.溫度 B.催化劑 C.反應物的濃度 D.壓強 組卷:17引用:6難度:0.6 -
9.能夠使CH3COONa溶液pH增大且水解程度也增大的條件是( )
A.加水 B.升溫 C.加壓 D.加CH3COONa固體 組卷:503引用:9難度:0.7 -
10.分析下列反應在任何溫度下均能自發進行的是( )
A.2N2(g)+O2(g)═2N2O(g)ΔH=+163kJ?mol-1 B.Ag(s)+ Cl2(g)═AgCl(s)ΔH=-127kJ?mol-112C.HgO(s)═Hg(l)+ O2(g)ΔH=+91kJ?mol-112D.H2O2(l)═ O2(g)+H2O(l)ΔH=-98kJ?mol-112組卷:274引用:36難度:0.5
二、非選擇題,共56分。
-
31.回答下列問題:
(1)已知t℃時,水的離子積常數Kw=1.0×10-12,該溫度下測得0.1mol?L-1Na2A溶液的pH=6。則t℃25℃(填“>”、“<”或“=”)。H2A在水溶液中的電離方程式為。
(2)已知氫氟酸、次氯酸、碳酸在室溫下的電離常數分別為:
根據上述數據,回答下列問題:HF Ka=6.8×10-4mol?L-1 HClO Ka=2.9×10-8mol?L-1 H2CO3 Ka1=4.4×10-7mol?L-1
Ka2=4.7×10-11mol?L-1
①比較同濃度的NaF、NaClO溶液的pH值大小:NaFNaClO。
②少量的CO2通入NaClO溶液中,寫出反應的離子方程式。
(3)用標準NaOH溶液對測定白醋中醋酸的濃度,完全反應時所得溶液的pH大致為9。
①該實驗應選用作指示劑:判斷酸堿中和滴定反應到達滴定終點時的現象為。
②為減小實驗誤差,一共進行了三次實驗,假設每次所取白醋體積均為VmL,NaOH標準液濃度為cmol/L,三次實驗結果記錄如表:
從上表可以看出,第一次實驗中記錄消耗NaOH溶液的體積明顯多于后兩次,其原因可能是實驗次數 第一次 第二次 第三次 消耗NaOH溶液體積/mL 26.02 25.35 25.30 。
A.實驗結束時,俯視刻度線讀取滴定終點時NaOH溶液的體積
B.滴定前堿式滴定管尖嘴有氣泡,滴定結束尖嘴部分充滿溶液
C.盛裝白醋溶液的滴定管用蒸餾水洗過,未用白醋溶液潤洗
D.錐形瓶預先用食用白醋潤洗過
E.滴加NaOH溶液時,未充分振蕩,剛看到溶液變色,立刻停止滴定
(4)25℃時,有c(NH3?H2O)+c(NH4+)=0.1mol?L-1的一組NH3?H2O、NH4Cl混合溶液,溶液中c(NH3?H2O)和c(NH4+)與溶液pH的關系如圖所示。下列說法錯誤的是。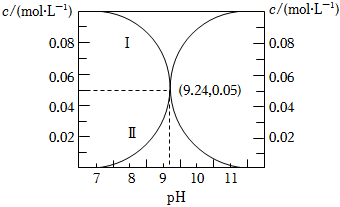
A.曲線Ⅰ表示c(NH4+)
B.Kb(NH3?H2O)的數量級為10-10
C.pH=7時,c(NH4+)=c(Cl-)>c(OH-)=c(H+)
D.pH=9.24時,c(NH3?H2O)=c(Cl-)+c(OH-)-c(H+)組卷:23引用:1難度:0.7 -
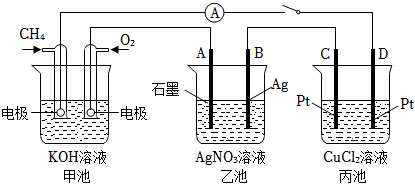 32.某實驗小組依據甲烷燃燒的反應原理,設計如圖所示的裝置.
32.某實驗小組依據甲烷燃燒的反應原理,設計如圖所示的裝置.
(1)甲池中負極的電極反應式為.
(2)乙池中A(石墨)電極的名稱為(填“正極”“負極”“陰極”或“陽極”),乙池中總反應為.
(3)若乙池中溶液體積為500mL,當B電極質量增加5.4g時,其pH為(忽略溶液體積變化);甲池中理論上消耗O2的體積為mL(標準狀況下);假設乙池、丙池中的溶液均足量,丙池中(填“C”或“D”)極析出g銅.組卷:47引用:2難度:0.5


