2013-2014學年江蘇省鹽城中學高二(下)暑假化學作業(8)
發布:2024/4/20 14:35:0
一、選擇題
-
1.美國“海狼”號潛艇上的核反應堆內使用了液體鋁鈉合金作載熱介質,下列關于Al、Na原子結構的分析中正確的是( )
A.原子半徑:Al>Na B.第一電離能:Al>Na C.電負性:Na>Al D.基態原子未成對電子數:Na>Al 組卷:99引用:17難度:0.9 -
2.以下表示氦原子結構的化學用語中,對電子運動狀態描述最詳盡的是( )
A.He B. 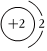
C.1s2 D. 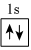 組卷:184引用:20難度:0.9
組卷:184引用:20難度:0.9 -
3.下列各組原子中,彼此化學性質一定相似的是( )
A.原子核外電子排布式為1s2的X原子與原子核外電子排布式為1s22s2的Y原子 B.原子核外M層上僅有兩個電子的X原子與原子核外N層上僅有兩個電子的Y原子 C.2p軌道上有一個空軌道的X原子與3p軌道上有一個空軌道的Y原子 D.最外層都只有一個電子的X、Y原子 組卷:20引用:9難度:0.7 -
4.對Na、Mg、Al的有關性質的敘述正確的是( )
A.堿性:NaOH<Mg(OH)2<Al(OH)3 B.第一電離能:Na<Mg<Al C.電負性:Na>Mg>Al D.還原性:Na>Mg>Al 組卷:93引用:71難度:0.7 -
5.下列說法錯誤的是( )
A.ns電子的能量可能低于(n-1)p電子的能量 B.6C的電子排布式1s22s22px2反了洪特規則 C.電子排布式(21Sc)1s22s22p63s23p63d3違反了能量最低原理 D.電子排布式(22Ti)1s22s22p63s23p10違反了泡利原理 組卷:88引用:10難度:0.7
二、非選擇題
-
15.有5 種短周期元素的原子序數按E、D、B、A、C的順序依次增大;A、C同周期,B、C同主族;A與B可形成離子化合物A2B,A2B中所有粒子的電子數相同,且電子總數為30;D和E可形成4核10電子的分子。試回答下列問題:
(1)寫出五種元素的名稱:ABCDE。
(2)用電子式表示離子化合物A2B的形成過程:。組卷:7引用:1難度:0.6 -
16.1932年美國化學家鮑林首先提出了電負性的概念。電負性(用X表示)也是元素的一種重要性質,如表給出的是原子序數小于20的16種元素的電負性數值:
請仔細分析,回答下列有關問題:元素 H Li Be B C N O F 電負性 2.1 1.0 1.5 2.0 2.5 3.0 3.5 4.0 元素 Na Mg Al Si P S Cl K 電負性 0.9 1.2 1.5 1.7 2.1 2.3 3.0 0.8
(1)預測周期表中電負性最大的元素應為;估計鈣元素的電負性的取值范圍:<x<。
(2)根據表中的所給數據分析,同主族內的不同元素X的值變化的規律是;簡述元素電負性X的大小與元素金屬性、非金屬性之間的關系。
(3)想驗規律告訴我們:當形成化學鍵的兩原子相應元素的電負性差值大于1.7時,所形成的一般為離子鍵;當小于1.7時,一般為共價鍵。試推斷AlBr3中形成的化學鍵的類型為,其理由是。組卷:9引用:2難度:0.5


