2020-2021學年福建省福州一中高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共20小題,每小題3分,滿分60分)
-
1.我國毛筆的制作技藝屬于國家非物質文化遺產,相傳古人制作該毛筆的過程為“以枯木為管,鹿毛為柱,羊毛為被(外衣)”,則下列說法正確的是( )
A.枯木的主要成分為蛋白質 B.鹿毛、羊毛均只含有C、H、O三種元素 C.枯木、鹿毛的主要成分互為同分異構體 D.采用灼燒法可以區分枯木、毛筆的“外衣” 組卷:79引用:3難度:0.7 -
2.下列烴中屬于飽和烴的是( )
A.C2H4 B.C2H2 C.C5H12 D.C6H6 組卷:71引用:1難度:0.8 -
3.下列說法正確的是( )
A.雞蛋清溶液中加入醋酸鉛溶液會變性 B.淀粉和纖維素互為同分異構體,化學式均為(C6H10O5)n C.乙酸乙酯在堿性條件下的水解反應為皂化反應 D.淀粉、纖維素、蛋白質和油脂均屬于天然高分子化合物 組卷:45引用:1難度:0.8 -
4.NA是阿伏加德羅常數的值。下列說法正確的是( )
A.7.8g Na2O2中含有的陰陽離子總數為0.3NA B.常溫下,11.2L CO2中含有的質子數為11NA C.5.6g鐵粉與0.1mol FeCl3充分反應,轉移的電子總數為0.2NA D.1L 1mol?L-1NaAlO2水溶液中含有的氧原子數為2NA 組卷:37引用:2難度:0.8 -
5.已知:①1mol H2分子中化學鍵斷裂時需要吸收436kJ的能量,②1mol I2蒸氣中化學鍵斷裂時需要吸收151kJ的能量,③由H原子和I原子形成1mol HI分子時釋放299kJ的能量.下列判斷不正確的是( )
A.I2蒸氣比H2分子穩定 B.2 mol HI(g)發生分解反應吸收11 kJ熱量 C.HI與NaOH反應屬于放熱反應 D.0.5 mol H2(g)與0.5 mol I2(g)完全反應釋放出5.5 kJ 熱量 組卷:59引用:9難度:0.7 -
6.據報道,科學家開發出了利用太陽能分解水的新型催化劑。下列有關水分解過程的能量變化示意圖正確的是( )
A. 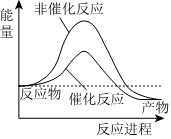
B. 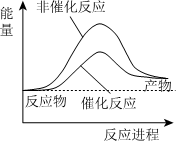
C. 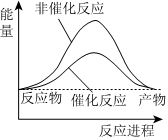
D. 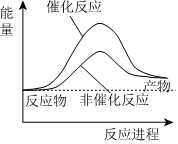 組卷:1217引用:121難度:0.9
組卷:1217引用:121難度:0.9 -
7.某濃度時,在2L密閉容器中,X.Y.Z三種氣體物質的物質的量隨時間的變化曲線.如圖所示,由圖中數據分析,該反應的化學方程式和反應開始至2min末Z的平均速率分別為( )
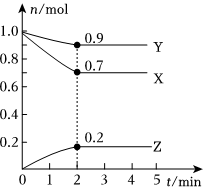
A.X+Y  2Z;0.05mol/(L?min)
2Z;0.05mol/(L?min)B.X+Y  2Z;0.1mol/(L?min)
2Z;0.1mol/(L?min)C.X+3Y  2Z;0.1mol/(L?min)
2Z;0.1mol/(L?min)D.3X+Y  2Z;0.05mol/(L?min)組卷:58引用:2難度:0.9
2Z;0.05mol/(L?min)組卷:58引用:2難度:0.9 -
8.用下列實驗裝置完成對應的實驗(部分儀器已省略),能達到實驗目的的是( )
A. 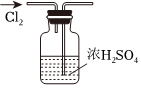
干燥Cl2B. 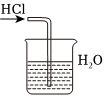
吸收HClC. 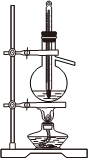
石油的蒸餾D. 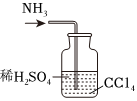
吸收NH3組卷:52引用:8難度:0.7
二、解答題(共4小題,滿分40分)
-
23.(1)紅葡萄酒密封儲存時間越長,質量越好,原因之一是儲存過程中生成了有香味的酯。在實驗室也可以用如圖所示的裝置制取乙酸乙酯,請回答下列問題。
①試管A中發生反應的化學方程式為。
②反應一段時間之后,試管B中可以觀察到的現象是。實驗完成后,分離B中的液體混合物需要用到的主要玻璃儀器是。
(2)酸牛奶中含有乳酸,其結構簡式為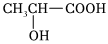 。回答下列問題:
。回答下列問題:
①1mol乳酸能與mol金屬鈉發生反應;
②在濃硫酸存在下,兩分子乳酸發生酯化反應,生成鏈狀物質的結構簡式為。組卷:33引用:1難度:0.7 -
24.某同學在實驗室進行鐵鹽與亞鐵鹽相互轉化實驗。實驗如圖所示。
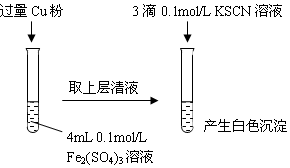
實驗Ⅰ:將Fe3+轉化為Fe2+
(1)Fe3+與Cu粉發生反應的離子方程式為:。
(2)探究白色沉淀產生的原因,請填寫實驗方案:
查閱資料:①SCN-的化學性質與I-相似;②2Cu2++4I-═2CuI↓+I2實驗方案 現象 結論 步驟1:取4mL0.1mol/LCuSO4溶液,向其中滴加3滴0.1mol/L KSCN溶液 產生白色沉淀 CuSO4與KSCN反應產生了白色沉淀 步驟2:取4mL0.2mol/LFeSO4溶液,向其中滴加3滴0.1mol/LKSCN溶液 無明顯現象
Cu2+與SCN-反應的離子方程式為。
實驗Ⅱ:將Fe2+轉化為Fe3+
探究上述現象出現的原因:實驗方案 現象 向3mL 0.1mol/L FeSO4溶液中加入1mL 8mol/L稀硝酸 溶液變為棕色,放置一段時間后,棕色消失,溶液變為黃色
查閱資料:Fe2++NO?Fe(NO)2+(棕色)
(3)用離子方程式解釋NO產生的原因。
(4)反應Ⅰ:Fe2+與HNO3反應;反應Ⅱ:Fe2+與NO反應
依據實驗現象,甲認為反應Ⅰ的速率比反應Ⅱ(填“快”或“慢”)。組卷:119引用:1難度:0.6


