2022-2023學年遼寧省大連市高二(上)期末化學試卷
發布:2024/12/20 9:0:3
一、選擇題:本題共15小題,每小題3分,共45分。在每小題給出的4個選項中,只有一項是符合題目要求的。
-
1.化學與生產、生活、科技等密切相關。下列說法不正確的是( )
A.除去CuCl2溶液中少量的FeCl3,可選用CuO固體 B.Sb2O3可用作白色顏料和阻燃劑等,在實驗室中可用SbCl3的水解反應制取 C.處理鍋爐水垢中的硫酸鈣,可以先用飽和碳酸鈉溶液浸泡,再用酸除去 D.氯堿工業中使用陽離子交換膜,主要目的是使電解池中形成閉合回路 組卷:34引用:4難度:0.7 -
2.下列說法不正確的是( )
A.原子半徑:Mg>Al>N B.第一電離能:S>P>Si C.酸性:CF3COOH>CH3COOH D.電負性:F>Cl>S 組卷:20引用:1難度:0.8 -
3.蛋白質和核酸是生命的物質基礎,其中都含有氮元素。下列化學用語表示正確的是( )
A.氮分子的結構式:N≡N B.基態氮原子最外能級的電子云輪廓圖: 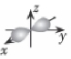
C.NH3的球棍模型: 
D.基態氮原子核外電子的軌道表示式: 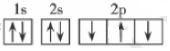 組卷:87引用:4難度:0.8
組卷:87引用:4難度:0.8 -
4.下列說法或表示方法中正確的是( )
A.已知2C(s)+2O2(g)=2CO2(g)ΔH=akJ?mol-1,2C(s)+O2(g)=2CO(g)ΔH=bkJ?mol-1,則a>b B.實驗測得在25℃和101kPa時,1molCH4完全燃燒放出890.3kJ的熱量,則CH4的燃燒熱ΔH=-890.3kJ?mol-1 C.氫氣的燃燒熱ΔH=-285.8kJ/mol-1,則水分解的熱化學方程式為:2H2O(l)=2H2(g)+O2(g)ΔH=+285.8kJ?mol-1 D.在稀溶液中,H+(aq)+OH-(aq)=H2O(1)ΔH=-57.3kJ/mol-1,若向1L1mol/L的稀鹽酸中加入1molNaOH固體,放出的熱量為57.3kJ 組卷:48引用:1難度:0.5 -
5.研究表明N2O與CO在Fe+的作用下會發生如下反應:
①N2O+Fe+→FeO++N2,
②FeO++CO→Fe++CO2。
其能量變化示意圖如圖所示。下列說法不正確的是( )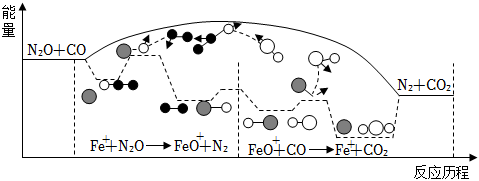
A.Fe+使反應的活化能變小 B.該催化劑不能有效提高反應物的平衡轉化率 C.N2O與CO在不同催化劑表面上轉化成N2與CO2的反應歷程完全相同 D.反應①過程中,N2O中的極性鍵發生了斷裂 組卷:928引用:1難度:0.5 -
6.下列說法不正確的是( )
A.鍵角:BF3>NH3 B.沸點:NH3>PH3 C.ClO3-的空間結構為平面三角形 D.NCl3是極性分子 組卷:62引用:1難度:0.6
二、非選擇題:本題共4小題,共55分。
-
18.以鎂鋁復合氧化物(MgO-Al2O3)為載體的負載型鎳銅雙金屬催化劑(Ni-Cu/MgO-Al2O3)是一種新型的高效加氫或脫氫催化劑,其制備流程如圖:
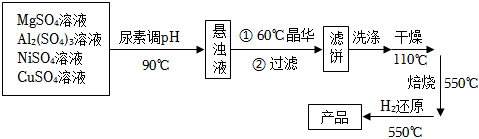
已知:常溫下,Ksp[Cu(OH)2]=2.21×10-20,Ksp[Al(OH)3]=1.3×10-33。回答下列問題:
(1)在元素周期表中,Ni在(填“s”“p”“d”“f”或“ds”)區,基態銅原子的價電子排布式為。
(2)在加熱條件下,尿素[CO(NH2)2]在水中發生水解反應,放出和(填化學式)兩種氣體。
(3)“晶化”過程中,需保持恒溫60℃,可采用的加熱方式為。
(4)常溫下,若“懸濁液”中=1.7×1010,則溶液的pH=c(Cu2+)c(Al3+)。
(5)Al2(SO4)3在消防工業中常用于與小蘇打、發泡劑組成泡沫滅火劑,請寫出其滅火原理(用離子方程式表示)。組卷:20引用:1難度:0.6 -
19.我國對世界鄭重承諾:2030年前實現碳達峰,2060年前實現碳中和。研發針對二氧化碳的碳捕捉和碳利用技術是其中的關鍵。
(1)工業尾氣中的CO2可以用NaOH溶液捕獲。常溫下,如果實驗測得捕獲CO2后的溶液中c(HCO3-):c(CO32-)=2:1,則此時溶液的pH=(已知常溫下,H2CO3的Ka1=4.0×10-7;Ka2=5.0×10-11)。
(2)利用CO2制備甲醇,其反應方程式為CO2(g)+3H2(g)CH3OH(g)+H2O(g)。已知CO2(g)+H2(g)?CO(g)+H2O(g)ΔH=+41.3kJ?mol-1;CO(g)+2H2(g)=CH3OH(g)ΔH=-90.8kJ?mol-1,則該反應的ΔH=催化劑。
(3)為探究用CO2生產甲醇的反應原理CO2(g)+3H2(g)CH3OH(g)+H2O(g)。現進行如下實驗:在2L恒溫密閉容器中,充入0.04molCO2和0.08molH2,測得其壓強(p)隨時間(t)變化(如圖1)曲線Ⅰ所示。催化劑
①用CO2來表示5min內的化學反應速率。
②其他條件相同時,若只改變某一條件,曲線由Ⅰ變化為Ⅱ,則改變的條件是。
③該溫度下,此反應的平衡常數Kp=Pa-2(保留三位有效數字)。(用平衡分壓代替平衡濃度計算,分壓=總壓×)該組分的物質的量各組分的總物質的量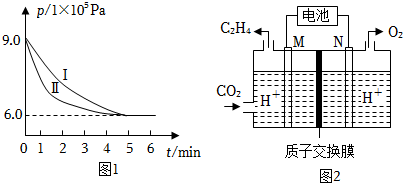
(4)工業上利用太陽能電池將CO2轉化為乙烯,以稀硫酸為電解質溶液,工作原理如圖2所示。則N極上的電極反應式為;該電解池中所發生的總反應的化學方程式為。組卷:39引用:1難度:0.5


