2021-2022學年寧夏石嘴山市平羅中學高一(上)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題只有一個正確答案,每題2分,共計44分)
-
1.古詩詞是我國重要的文化遺產,下列詩句中加點字部分涉及化學變化的是( )
A.月波成露露成霜,借與南枝作淡妝 B.莫道雪融便無跡,雪融成水水成冰 C.寶劍鋒從磨礪出,梅花香自苦寒來 D.春蠶到死絲方盡,蠟炬成灰淚始干 組卷:55引用:2難度:0.7 -
2.下列敘述正確的是( )
A.1molCO2的質量為44g/mol B.H2SO4的摩爾質量為98 C.1molH2O中含有1molH2 D.O2的相對分子質量為32 組卷:12引用:4難度:0.7 -
3.下列電離方程式書寫正確的是( )
A.Al2O3(熔融)═2Al3++3O2- B.NaHCO3═Na++H++CO32- C.H2CO3?2H++CO32- D.CH3COONH4?NH4++CH3COO- 組卷:8引用:3難度:0.7 -
4.下列有關氯氣的敘述不正確的是( )
A.氯氣和水反應生成的次氯酸不穩定,易分解 B.干燥的氯氣沒有漂白性 C.氯氣有毒,不能用于合成藥物 D.鐵能在氯氣中燃燒,但干燥的氯氣可以儲存在鋼瓶中 組卷:8引用:2難度:0.6 -
5.科學家指出,食用蝦類等水生甲殼類動物的同時服用維生素C容易中毒,這是因為對人體無害的+5價砷類物質在維生素C的作用下,能夠轉化為有毒的+3價砷類化合物。下列說法不正確的是( )
A.維生素C具有還原性 B.上述過程中砷元素發生還原反應 C.上述過程中+5價砷類物質作氧化劑 D.還原性:Vc小于+3價砷類化合物 組卷:30引用:4難度:0.7 -
6.下列溶液中Cl-的物質的量濃度最大的是( )
A.200mL0.2mol?L-1MgCl2溶液 B.250mL0.2mol?L-1AlCl3溶液 C.300mL1.0mol?L-1KClO3溶液 D.500mL0.5mol?L-1NaCl溶液 組卷:20引用:1難度:0.8 -
7.下列變化過程中,屬于氧化反應的是( )
A.SO3→SO2 B.Zn→Zn2+ C.MnO2→Mn D.HNO3→NO 組卷:12引用:3難度:0.7 -
8.某同學想利用所學的知識去探究SO2的性質,設計了如下研究程序,合理的是( )
A.分類(預測SO2的化學性質)→觀察(得出SO2的物理性質)→實驗→比較并得出結論 B.觀察(得出SO2的物理性質)→分類(預測SO2的化學性質)→實驗( 觀察實驗現象、驗證預測)→比較并得出結論,對于異常現象再預測,再實驗,再驗證 C.觀察(得出 SO2 的物理性質)→實驗→分類(預測SO2 的化學性質)→比較并得出結論 D.實驗→分類(預測SO2的化學性質)→觀察(得出SO2的物理性質)→比較并得出結論 組卷:8引用:2難度:0.6 -
9.下列關于鈉的說法中不正確的是( )
A.金屬鈉和氧氣反應,條件不同,產物不同 B.大量的鈉著火時可以用沙子撲滅,少量的鈉應保存在煤油中 C.將一小塊鈉投入裝有氯化鎂溶液的試管里,鈉熔成小球并在液面上游動 D.將一小塊鈉投入稀鹽酸中,鈉與水反應生成NaOH和H2,生成的NaOH再與HCl反應生成NaCl和H2O 組卷:7引用:7難度:0.6
二、(非選擇題共計56分)
-
26.如圖所示為利用分類法對一組物質進行的分類。回答下列問題:

(1)按照分類法,CO2屬于(填“酸性”或“堿性”)氧化物,書寫CO2與Na2O2反應的化學方程式,依據該反應,可以說明Na2O2(填“屬于”或“不屬于”)堿性氧化物。
(2)上述物質中屬于電解質的是。
(3)某學生完成鈉與水反應的實驗,實驗過程如圖①、②、③所示,下列有關實驗現象及結論的敘述不正確的是。(填序號)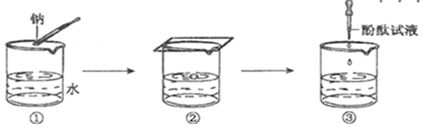
A.圖②中鈉熔成小球,說明鈉與水反應放熱且鈉的熔點低
B.圖②中鈉四處游動并嘶嘶作響,說明反應產生了氣體
C.圖③中滴加酚酞試液后溶液變紅,說明有堿性物質生成
D.鈉與水反應的離子方程式是:2Na+2H+?═2Na++H2↑
(4)工業上常用Cl2與NaOH溶液反應制取消毒液,該反應的化學方程式為。
(5)向NaHSO4溶液中加入NaOH溶液,對應的離子方程式為。
(6)用一種試劑除去下列各物質的雜質(括號內為雜質,填寫試劑名稱):
CO2(HCl),試劑:;SO42-(CO32-),試劑:。組卷:3引用:1難度:0.6 -
27.一個體重50kg的健康人體內含鐵元素2g,這2g鐵元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以給貧血者補充鐵時,應補充含Fe2+的亞鐵鹽(如FeSO4)。服用維生素C可使食物中的Fe3+轉化成Fe2+,有利于人體對鐵的吸收。請回答下列問題:
(1)缺鐵性貧血患者應補充Fe2+。用綠礬制成的補鐵劑藥片外表包有一層特殊的糖衣,試推測糖衣的作用是。
(2)向某溶液中加入KSCN溶液,溶液立即變成紅色,則原溶液中含有(填離子符號),要除去FeCl3溶液中少量的氯化亞鐵,可行的辦法是(填字母)。
A.加入銅粉
B.加入鐵粉
C.通入氯氣
D.加入KSCN溶液
(3)某工廠用FeCl3溶液腐蝕鍍有銅的絕緣板生產印刷電路,此反應的離子方程式為。
(4)已知下列反應:
ⅰ:Cu+2H2SO4(濃)CuSO4+SO2↑+2H2O,△
ⅱ:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+。
①Cu、SO2、Fe2+還原性由強到弱的順序為。
②當反應ⅰ中有0.2molH2SO4被還原時,被氧化的物質的質量為g。
③用單線橋表示反應ⅰ電子轉移的方向和數目。組卷:5引用:1難度:0.6


