2021-2022學年廣西南寧市賓陽中學高二(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共20小題,每小題2分,滿分40分)
-
1.能源是國民經濟和社會發展的重要物質基礎,下列屬于二次能源的是( )
A.煤炭 B.地熱 C.電力 D.風能 組卷:27引用:4難度:0.9 -
2.下列過程在一定條件下能自發進行但不能用熵增解釋的是( )
A.花香四溢 B.冰塊融化 C.Na2CO3?10H2O風化 D.水蒸氣冷凝 組卷:51引用:3難度:0.7 -
3.向稀氨水中分別加入以下物質,水的電離平衡會正向移動的是( )
A.NH4Cl B.濃氨水 C.NaOH D.Na2SO4 組卷:35引用:2難度:0.7 -
4.下列溶液顯酸性,解釋其原因的化學用語錯誤的是( )
A.碳酸溶液:H2CO3?2H++CO32- B.硫酸溶液:H2SO4═2H++SO42- C.硫酸氫鈉溶液:NaHSO4═Na++H++SO42- D.NH4Cl溶液:NH4++H2O?NH3?H2O+H+ 組卷:31引用:4難度:0.5 -
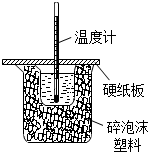 5.已知:反應HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)ΔH=-57.3kJ/mol.現分別取50mL0.50mol/L醋酸與50mL0.55mol/LNaOH溶液進行中和反應,用如圖實驗裝置測定該反應的中和熱ΔH,下列敘述正確的是( )
5.已知:反應HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)ΔH=-57.3kJ/mol.現分別取50mL0.50mol/L醋酸與50mL0.55mol/LNaOH溶液進行中和反應,用如圖實驗裝置測定該反應的中和熱ΔH,下列敘述正確的是( )A.圖中裝置缺少銅絲攪拌棒 B.為了讓反應充分進行,NaOH分三次倒入 C.該實驗測定的反應熱ΔH>-57.3kJ/mol D.用50mL0.50mol/LNaOH溶液更準確 組卷:68引用:5難度:0.7 -
6.以下應用與鹽類水解無關的是( )
A.用熱堿去除廢鐵屑表面油污 B.配制Na2S溶液時需將Na2S溶于NaOH濃溶液 C.用硫酸鋁溶液和碳酸氫鈉溶液混合滅火 D.用FeCl3溶液刻蝕銅制電路板 組卷:40引用:3難度:0.5 -
7.H-H鍵鍵能為436kJ/mol,下列關于反應H2(g)+Cl2(g)═2HCl(g) ΔH=akJ/mol的能量變化敘述正確的是( )
A.1molH-H斷裂放出熱量436kJ B.a值由鍵能決定,與狀態無關 C.光照和點燃條件下a的數值不同 D.使用催化劑不能改變ΔH 組卷:44引用:3難度:0.5 -
8.常溫下,濃度均為0.1mol/L的醋酸和鹽酸溶液在水中的電離示意圖如圖所示,下列描述錯誤的是( )
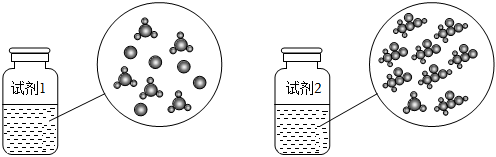
A.  代表H3O+
代表H3O+B.冰醋酸是強電解質 C.pH:試劑1<試劑2 D.中和等體積兩份溶液,耗堿量相同 組卷:25引用:2難度:0.8
二、解答題(共5小題,滿分60分)
-
24.天然水加熱時產生水垢.天然水中含Ca(HCO3)2與Mg(HCO3)2,Mg(HCO3)2熱分解產物有MgCO3、Mg(OH)2.回答下列問題:
(1)加熱Ca(HCO3)2的化學方程式為;持續加熱,MgCO3沉淀可轉換為Mg(OH)2,說明更難溶.
(2)濃縮海水得粗鹽水中主要含有Mg2+、Ca2+、SO42-等離子.粗鹽水精制食鹽過程中,按除雜順序寫出除雜試劑的化學式為、、,過濾取濾液,加過量鹽酸酸化后,蒸發結晶純化.
(3)工業上通常用Ca(OH)2除去天然水中Mg2+,已知某天然水中Mg2+開始沉淀的pH為9.6,則溶液中Mg2+的初始濃度是.(Ksp[Mg(OH)2]=10-11.3)
(4)工業上制備輕質氧化鎂流程如圖.輕質氧化鎂相比重質氧化鎂質量更輕,更加疏松多孔.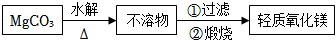
①水解過程加熱的作用是;
②不用重質MgO而用輕質MgO酸溶制備MgSO4的原因是.組卷:25引用:2難度:0.5 -
25.烯烴是化工生產的重要原料,低碳烷烴脫氫制低碳烯烴對提高化石能源利用率有著重要作用.乙烷脫氫的反應為:C2H6(g)═C2H4(g)+H2(g)ΔH 反應Ⅰ
(1)有關物質的燃燒熱如表.則ΔH=.
(2)在一定溫度下,有利于提高C2H6平衡轉化率的措施是物質 C2H6 C2H4 H2 燃燒熱/(kJ/mol) -1559.8 -1411.0 -285.8 (寫一條).
(3)研究發現,向反應的恒容體系中充入一定量的CO2發生反應:CO2+H2═CO+H2O.相同條件下,充入CO2和未充入CO2時C2H6的平衡轉化率(α)隨溫度變化曲線如圖.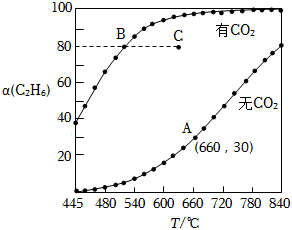
①向2L恒容體系下充入2mol的C2H6,30min達到A點,反應Ⅰ的平均反應速率v(C2H6)=mol?L-1?min-1;
②圖中C點與B點相同充料,則此時C點u正v逆(填“>”、“<”或“=”);B點的v正C點的v逆(填“>”、“<”或“=”).
③向反應中加入CO2制備乙烯具有明顯優勢,其原因是.組卷:24引用:2難度:0.6


