2021-2022學年北京八中高二(上)期末化學試卷
發布:2024/11/28 4:0:2
一、每小題只有一個選項符合題意,每小題3分,共42分
-
1.下列設備工作時,將化學能轉化為熱能的是( )
A.硅太陽能電池 B.鉛蓄電池 C.燃氣灶 D.電烤箱 組卷:91引用:5難度:0.8 -
2.下列關于原子結構的說法中,不正確的是( )
A.原子結構決定元素的性質 B.2px、2py、2pz軌道相互垂直,且能量相等 C.隨核電荷數遞增,電子總是填滿一個能層,再填下一個能層 D.電子云是電子在原子核外空間的概率密度分布的形象化描述 組卷:110引用:3難度:0.8 -
3.常溫下,下列事實能說明HClO是弱電解質的是( )
A.HClO在光照條件下易分解成HCl和O2 B.0.01mol/L NaClO溶液的pH>7 C.NaClO的電離方程式:NaClO═Na++ClO- D.HClO與Na2SO3溶液反應,可以得到Na2SO4 組卷:134引用:5難度:0.7 -
4.下列溶液肯定顯酸性的是( )
A.c(H+)>c(OH-)的溶液 B.含H+的溶液 C.pH<7的溶液 D.加酚酞顯無色的溶液 組卷:101引用:11難度:0.6 -
5.下列化學用語表示正確的是( )
A.Ca2+的結構示意圖: 
B.基態碳原子的軌道表示式: 
C.水的電子式: 
D.基態鉻原子(24Cr)的價層電子排布式:3d54s1 組卷:51引用:7難度:0.8 -
6.下列方程式與所給事實不相符的是( )
A.用硫化鈉溶液除去廢水中的Cu2+:Cu2++S2-═CuS↓ B.用飽和Na2CO3溶液處理鍋爐水垢中的CaSO4:Ca2++CO32-═CaCO3↓ C.酚酞滴入醋酸鈉溶液中變為淺紅色:CH3COO-+H2O?CH3COOH+OH- D.用明礬[KAl(SO4)2?12H2O]作凈水劑:Al3++3H2O?Al(OH)3(膠體)+3H+ 組卷:51引用:3難度:0.6
二、解答題(共5小題,滿分58分)
-
18.海洋資源的開發與利用具有廣闊的前景.海水的pH一般在7.5~8.6之間.某地海水中主要離子的含量如表:
(1)海水顯弱堿性的原因是(用離子方程式表示):成分 Na+ K+ Ca2+ Mg2+ Cl- SO2-4HCO3- 含量/mg?L-1 9360 83 200 1100 16000 1200 118 ,該海水中Ca2+的物質的量濃度為mol/L.
(2)電滲析法是近年發展起來的一種較好的海水淡化技術,其原理如圖1所示.其中陰(陽)離子交換膜只允許陰(陽)離子通過.
①陰極的電極反應式為.
②電解一段時間,陰極區會產生水垢,其成分為CaCO3和Mg(OH)2,寫出生成CaCO3的離子方程式.
③淡水的出口為a、b、c中的出口.
(3)海水中鋰元素儲量非常豐富,從海水中提取鋰的研究極具潛力.鋰是制造化學電源的重要原料,如LiFePO4電池某電極的工作原理如圖2所示:
該電池電解質為能傳導 Li+的固體材料.放電時該電極是電池的極(填“正”或“負”),電極反應式為.
(4)利用海洋資源可獲得MnO2.MnO2可用來制備高錳酸鉀:將MnO2與KOH混合后在空氣中加熱熔融,得到綠色的錳酸鉀(K2MnO4),再利用氯氣將錳酸鉀氧化成高錳酸鉀.該制備過程中消耗相同條件下空氣和氯氣的體積比為(空氣中氧氣的體積分數按20%計). 組卷:74引用:3難度:0.5
組卷:74引用:3難度:0.5 -
19.實驗小組對NaHSO3溶液分別與CuCl2、CuSO4溶液的反應進行探究。
已知:實驗 裝置 試劑x 操作及現象
Ⅰ
1 mol?L-1 CuCl2溶液加入2mL CuCl2溶液,得到綠色溶液,30s時有無色氣泡和白色沉淀產生,上層溶液顏色變淺。 Ⅱ 1 mol?L-1 CuSO4溶液 加入2mL CuSO4溶液,得到綠色溶液,3分鐘未見明顯變化。
Ⅰ.Cu2+[Cu(NH3)4]2+(深藍色溶液)濃氨水
Ⅱ.Cu+[Cu(NH3)2]+(無色溶液)濃氨水[Cu(NH3)4]2+(深藍色溶液)露置在空氣中一段時間
(1)推測實驗Ⅰ產生的無色氣體為SO2,實驗證實推測正確:用蘸有碘水的淀粉試紙接近試管口,觀察到,反應的離子方程式為。
(2)對實驗Ⅰ產生SO2的原因進行分析,提出假設:
假設a:Cu2+水解使溶液中c(H+)增大;
假設b:Cl-存在時,Cu2+與反應生成CuCl白色沉淀,溶液中c(H+)增大。HSO-3
①假設a不合理,實驗證據是;
②實驗表明假設b合理,實驗I反應的離子方程式有、H++═SO2↑+H2O。HSO-3
(3)對比實驗Ⅰ、Ⅱ,提出假設:Cl-增強了Cu2+的氧化性。
下述實驗Ⅲ證實了假設合理,裝置如圖。實驗方案:閉合K,電壓表的指針偏轉至“X”處;向U形管(補全實驗操作及現象)。
(4)將實驗Ⅱ的溶液靜置24小時或加熱后,得到紅色沉淀。經檢驗,紅色沉淀中含有Cu+、Cu2+和。SO2-3
①通過實驗Ⅳ證實紅色沉淀中含有Cu+和Cu2+。
實驗Ⅳ: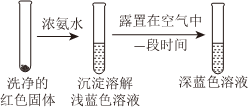
證實紅色沉淀中含有Cu+的實驗證據是;
②有同學認為實驗Ⅳ不足以證實紅色沉淀中含有Cu2+,設計實驗Ⅳ的對比實驗Ⅴ,證實了Cu2+的存在。實驗Ⅴ的方案和現象是:。組卷:105引用:6難度:0.5


