2021-2022學年重慶市好教育聯盟高一(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共14小題,每小題3分,共42分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.化學與生活息息相關,下列有關說法不正確的是( )
A.熟石膏與水混合成糊狀物會很快凝固,醫療上可用來制作石膏繃帶 B.硫酸鋇不溶于水.不溶于酸且不能被X射線透過,可用作X射線檢測的“鋇餐” C.彩色玻璃是制玻璃過程中加入一些金屬氧化物或鹽制得的,可用于建筑和裝飾 D.國產飛機C919用到的氮化硅陶瓷是新型有機非金屬材料 組卷:9引用:1難度:0.6 -
2.已知ΔH>0表示吸熱反應,ΔH<0表示放熱反應。反應A+B→C(ΔH>0)分兩步進行:①A+B→X(ΔH<0);②X→C(ΔH>0)。下列示意圖中,能正確表示總反應過程中能量變化的是( )
A. 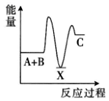
B. 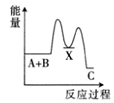
C. 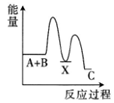
D. 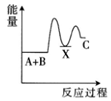 組卷:134引用:4難度:0.7
組卷:134引用:4難度:0.7 -
3.下列生活中的常見物品或設施,其主要成分為硅單質的是( )
A.磚瓦 B.計算機芯片 C.門窗玻璃 D.石英鐘 組卷:18引用:4難度:0.6 -
4.化學在生產和日常生活中有著重要的應用,下表中用途與其性質或原理對應關系錯誤的是( )
選項 用途 性質或原理 A 葡萄酒中添加適量的SO2起到保質作用 SO2具有殺菌、抗氧化作用 B Al(OH)3膠體可用作自來水凈水劑 Al(OH)3膠體具有吸附性 C 在食品包裝袋中放入裝有硅膠、鐵粉的透氣小袋,可防止食物受潮、氧化變質 硅膠具有吸水性,鐵粉具有氧化性 D 用小蘇打治療胃酸過多 NaHCO3可與胃液中的酸反應 A.A B.B C.C D.D 組卷:5引用:4難度:0.6 -
5.下列表示的物質中屬于含有非極性共價鍵的離子化合物的是( )
A. 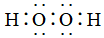
B. 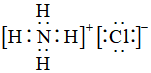
C. 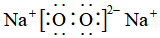
D. 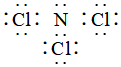 組卷:73引用:3難度:0.5
組卷:73引用:3難度:0.5 -
6.下列有關氮及其化合物的說法正確的是( )
A.氮氧化物與光化學煙霧的形成有關 B.濃硝酸氧化性強,不能用鐵質或鋁質容器貯運 C.鎂、鋅等活潑金屬可與稀硝酸反應,生成氫氣 D.氮的固定只有在高溫、高壓、催化劑存在的條件下才能實現 組卷:38引用:3難度:0.9
二、非選擇題:本題共4小題,共58分。
-
17.氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用。
(1)N2(g)和H2(g)反應生成1molNH3(g)過程中的能量變化示意圖如圖。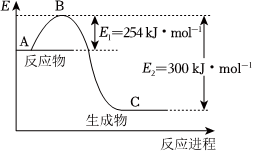
①寫出N2和H2反應生成NH3的化學方程式:。
②已知化學鍵的鍵能是形成或斷開1mol化學鍵放出或吸收的能量,單位為kJ?mol-1。若已知下列數據:
試根據表中及圖中數據計算N-H的鍵能為化學鍵 H-H N≡N 鍵能/(kJ?mol-1) 435 943 kJ?mol-1。
(2)汽車尾氣中的氮氧化物是城市空氣的主要污染物之一,如何降低汽車尾氣污染已成為環保領域的熱點。使用氫能源可以減少汽車尾氣中有害氣體的排放,利用甲醇與水蒸氣反應可以制備氫氣:CH3OH(g)+H2O(g)?CO2(g)+3H2(g)。在體積為2L的恒溫恒容密閉容器中,充入1molCH3OH(g)和1molH2O(g),一定條件下發生上述反應,測得H2(g)和CH3OH(g)的物質的量隨時間變化如表所示。
①3~9min內,v(CO2)=0min 3min 6min 9min 12min n(H2)/mol 0 1.53 1.95 2.16 2.16 n(CH3OH)/mol 1 0.49 0.35 0.28 0.28 mol?L-1?min-1;第10min時,c(H2)=mol?L-1。
②能說明上述反應達到化學平衡狀態的是(填標號)
A.反應中CO2與CH3OH的物質的量之和為1mol
B.H2O(g)的物質的量濃度不再改變
C.單位時間內生成3molH2的同時生成1molCH3OH
D.CH3OH(g)與H2O(g)的物質的量之比為1:1
③在上述反應條件下,反應到6min末時,氣體的總物質的量為mol。
④12min末時,混合氣體中CO2(g)和H2O(g)的質量之比是。組卷:14引用:2難度:0.6 -
18.氮在自然界中的轉化是一個復雜的過程,氮循環是生態系統物質循環的重要組成部分。
(1)在一定條件 下,NH3可用于脫除氮氧化物的煙氣,其反應原理為4xNH3+6NOx(2x+3)N2+6xH2O。該反應中的還原劑為一定條件(填化學式)。
(2)氨的催化氧化是制備硝酸的重要過程,實驗室按如圖所示裝置進行氨的催化氧化實驗。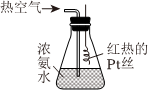
實驗操作:將濃氨水倒入錐形瓶中,從導氣管通入熱空氣,將紅熱的鉑絲伸入錐形瓶中。
實驗現象:a.紅熱的鉑絲始終保持紅熱狀態;b.瓶中有紅棕色氣體生成,瓶內還有白煙生成。
回答下列問題:
①鉑絲始終保持紅熱狀態的可能原因是。
②通入熱空氣的作用是。
③請寫出氨氣的催化氧化反應的化學方程式:。
④紅棕色氣體的化學式為,此氣體可用NaOH溶液吸收,有NaNO2和NaNO3生成,寫出該反應的離子方程式:。
(3)氨是氮循環中的重要物質,在人類的生產和生活中有著廣泛的應用。高濃度的氨氮廢水是造成河流及湖泊富營養化的主要因素,研究表明在微生物作用下,可實現→NH+4的轉化。寫出在堿性條件下,NO-3被氧氣氧化為NH+4的反應的離子方程式:NO-3。每生成1,轉移的電子的物質的量為molNO-3mol。再往含的廢水中加入甲醇,可將NO-3轉化為N2,實現廢水的無害化處理。NO-3組卷:32引用:3難度:0.8


