2022-2023學年天津市咸水沽一中高二(上)期末化學試卷
發布:2024/4/20 14:35:0
一、單選題(本題共15小題,每題3分,共45分)
-
1.下列說法正確的是( )
A.強電解質溶液的導電能力一定比弱電解質溶液的強 B.同溫同壓下,H2(g)+Cl2(g)═2HCl(g)在光照和點燃條件下的ΔH不同 C.等濃度等體積的鹽酸和醋酸溶液中和同種NaOH溶液,消耗氫氧化鈉一樣多 D.在氯化銀的沉淀溶解平衡體系中,加入蒸餾水,氯化銀的Ksp增大 組卷:39引用:1難度:0.5 -
2.下列說法或表示正確的是( )
A.等量的硫蒸氣和硫固體分別完全燃燒,后者放出熱量多 B.已知2C(s)+2O2(g)═2CO2(g)ΔH1;2C(s)+O2(g)═2CO(g)ΔH2;則ΔH1>ΔH2 C.在稀溶液中:H+(aq)+OH-(aq)═H2O(l)ΔH=-57.3kJ?mol-1,若將含1molCH3COOH的醋酸溶液與含1molNaOH的溶液混合,放出的熱量小于57.3kJ D.在101kPa時,2gH2完全燃燒生成液態水,放出285.8kJ熱量,氫氣燃燒的熱化學方程式表示為2H2(g)+O2(g)═2H2O(l)ΔH=-285.8kJ?mol-1 組卷:32引用:1難度:0.7 -
3.下列事實不能說明醋酸是弱電解質的是( )
A.醋酸的pH比鹽酸pH大 B.0.1mol?L-1醋酸溶液的pH=2 C.CH3COOK溶液能使酚酞試液變紅色 D.醋酸溶液中存在醋酸分子 組卷:45引用:1難度:0.7 -
4.下列不能用勒夏特列原理解釋的是( )
A.Fe(SCN)3溶液中加入固體KSCN后顏色變深 B.石灰石與稀鹽酸在密閉瓶中反應結束后,打開瓶塞,溶液中有氣泡產生 C.使用新型催化劑可使氮氣與氫氣在常溫常壓下合成氨氣 D.NO2、N2O4平衡混合氣加壓后顏色先變深后變淺 組卷:55引用:5難度:0.7 -
5.下列敘述正確的是( )
A.常溫下,將1mL1×10-6mol/L鹽酸稀釋至1000mL,所得溶液的pH約為9 B.常溫下,pH=12的氨水與pH=2的H2SO4等體積混合,所得溶液顯堿性 C.已知Ksp(BaCO3)稍大于Ksp(BaSO4),所以BaSO4和Na2CO3不可能轉化成BaCO3 D.100℃時,pH=12的強堿溶液與pH=2的強酸溶液混合,若所得混合液的pH=7,則強堿與強酸的體積比是1:1 組卷:94引用:2難度:0.5 -
6.下列各項敘述中,正確的是( )
A.鎂原子由1s22s22p63s2→1s22s22p63p2時,原子釋放能量,由基態轉化成激發態 B.價電子排布為3d104s1的元素位于第四周期第ⅠA族,是s區元素 C.在現代化學中,常利用原子光譜上的特征譜線來鑒定元素,稱為光譜分析 D.p軌道電子能量一定高于s軌道電子能量 組卷:99引用:1難度:0.7
二、填空題題(本題共5小題,共55分)
-
19.常溫下,有濃度均為0.1mol?L-1的下列4種溶液:①NaCN溶液②NaOH溶液③CH3COONa溶液④NaHCO3溶液
(1)這4種溶液pH由大到小的順序是HCN H2CO3 CH3COOH Ka=4.9×10-10 Ka1=4×10-7
Ka2=5.6×10-11Ka=1.7×10-5 (填序號)。
(2)若分別向等體積的③和④中滴加鹽酸至呈中性,則消耗鹽酸的體積③④(填“>”“<”或“=”)。
(3)向NaCN溶液中通入少量CO2,則發生反應的離子方程式為。
(4)泡沫滅火器中通常裝有NaHCO3溶液和Al2(SO4)3溶液,請寫出這兩種溶液混合時反應的離子方程式:。
(5)已知25℃時,CO32-第一步水解的平衡常數Kh=2×10-4,當溶液中c(HCO3-):c(CO32-)=20:1時,溶液的pH=。組卷:56引用:1難度:0.6 -
 20.某同學用酸性KMnO4溶液測定綠礬產品中Fe2+含量,請回答下列問題:
20.某同學用酸性KMnO4溶液測定綠礬產品中Fe2+含量,請回答下列問題:
反應原理為:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O(Mn2+在溶液中為無色)
a.稱取11.5g綠礬產品,溶解,配制成1000mL溶液;
b.量取25.00mL待測溶液于錐形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至終點。
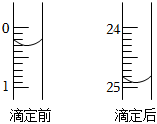
(1)若甲學生在實驗過程中,記錄滴定前后滴定管內液面讀數如圖所示,則此時消耗標準溶液的體積為mL。
(2)此滴定實驗達到終點的顏色變化為。
(3)重復滴定4次,每次消耗酸性KMnO4標準溶液的體積如表所示:
計算上述樣品中FeSO4?7H2O的質量分數為第一次 第二次 第三次 第四次 V(KMnO4溶液)/mL 17.10 19.98 20.00 20.02 。(FeSO4?7H2O M=278g/mol,小數點后保留一位)
(4)若滴定前平視讀數,滴定終點時仰視讀數,則所測Fe2+含量:。(填“無影響”、“偏高”或“偏低”)。組卷:24引用:1難度:0.5


