2021-2022學年云南省普洱市鎮沅一中高一(下)開學化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共25小題,每小題2.0分,共50分)
-
1.下列說法中正確的是( )
A.標準狀況下,18g水的體積為22.4L B.1molH2的質量只有在標準狀況下才約為2g C.氣體摩爾體積指1mol任何氣體所占的體積約為22.4L D.H2和O2的混合氣體1mol在標準狀況下的體積約為22.4L 組卷:72引用:1難度:0.8 -
2.根據下列反應判斷有關物質還原性由強到弱的順序是( )
①H2SO3+I2+H2O═2HI+H2SO4
②2FeCl3+2HI═2FeCl2+2HCl+I2
③3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3A.H2SO3>I->Fe2+>NO B.I->Fe2+>H2SO3>NO C.Fe2+>I->H2SO3>NO D.NO>Fe2+>H2SO3>I- 組卷:622引用:117難度:0.7 -
3.某同學用如圖裝置制備并檢驗氯氣的性質。下列說法正確的是( )
A. 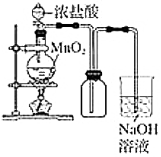
如圖:若二氧化錳過量,則濃鹽酸可全部消耗完B. 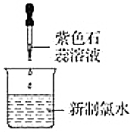
如圖:僅證明新制氯水具有酸性C. 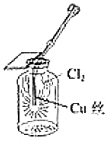
如圖:產生了棕黃色的霧D. 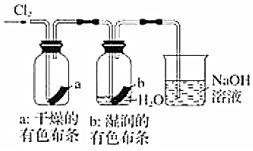
如圖:濕潤的有色布條褪色組卷:10引用:1難度:0.8 -
4.若aAm+與bBn-的核外電子排布相同,則下列關系不正確的是( )
A.b=a-n-m B.離子半徑Am+<Bn- C.原子半徑A<B D.A的原子序數比B大(m+n) 組卷:33引用:28難度:0.9 -
5.下列說法中正確的是( )
A.液態氯化氫、固態氯化鈉都不導電,所以氯化氫、氯化鈉都是非電解質 B.氨氣、二氧化碳的水溶液都能導電,所以氨氣、二氧化碳都是電解質 C.蔗糖、酒精在水溶液里或熔融狀態時都不導電,所以它們是非電解質 D.銅、石墨都導電,所以它們都是電解質 組卷:17引用:2難度:0.8 -
6.在周期表中,所含元素種類最多的族是( )
A.第Ⅷ族 B.第ⅠA族 C.0族 D.第ⅢB族 組卷:7引用:1難度:0.9 -
7.相同質量的兩份鋁,分別放入足量的鹽酸和氫氧化鈉溶液中,放出的氫氣在同溫同壓下的體積比為( )
A.1:1 B.1:6 C.2:3 D.3:2 組卷:217引用:65難度:0.7 -
8.下列關于氯氣的敘述正確的是( )
A.鈉在氯氣中燃燒產生白色煙霧 B.紅熱的銅絲可以在氯氣中燃燒,產生棕黃色煙霧 C.純凈的氫氣可以在氯氣中安靜地燃燒,發出蒼白色火焰 D.氯氣可用于漂白,這是氯氣的漂白作用 組卷:30引用:4難度:0.9 -
9.下列關于Na2CO3、NaHCO3,說法正確的是( )
A.受熱時Na2CO3較NaHCO3更不穩定,更易分解產生CO2 B.等質量的Na2CO3、NaHCO3與足量鹽酸反應,前者產生的CO2更多 C.常溫下,等量水中完全溶解等質量的Na2CO3、NaHCO3所得溶液,前者堿性更強 D.向Na2CO3、NaHCO3溶液中分別滴加澄清石灰水,前者產生白色沉淀,后者無沉淀 組卷:5引用:2難度:0.7 -
10.已知1.6g某氣體所含分子數目約為3.01×1022,此氣體摩爾質量為( )
A.32g B.32g?mol-1 C.64mol D.64g?mol-1 組卷:3引用:1難度:0.5
二、非選擇題(共5小題,共50分)
-
29.現用質量分數為98%、密度為1.84g?cm-3的濃H2SO4來配制500mL、0.2mol?L-1的稀H2SO4.可供選擇的儀器有:①玻璃棒②燒瓶③燒杯④膠頭滴管⑤量筒⑥容量瓶⑦托盤天平⑧藥匙。請回答下列問題:
(1)上述儀器中,在配制稀H2SO4時用不到的有(填代號)。
(2)經計算,需濃H2SO4的體積為。現有①10mL②50mL③100mL三種規格的量筒,你選用的量筒是(填代號)。
(3)將濃H2SO4加適量蒸餾水稀釋后,冷卻片刻,隨后全部轉移到mL的容量瓶中,轉移時應用玻璃棒。轉移完畢,用少量蒸餾水洗滌2-3次,并將洗滌液全部轉移到容量瓶中,再加適量蒸餾水,振蕩容量瓶,使溶液混合均勻。然后緩緩地把蒸餾水直接注入容量瓶直到液面接近刻度處。改用加蒸餾水到瓶頸刻度的地方,使溶液的。 振蕩、搖勻后,裝瓶、貼簽。
(4)在配制過程中,其他操作都準確,下列操作中錯誤的是(填代號,下同),能引起誤差偏高的有。
①洗滌量取濃H2SO4后的量筒,并將洗滌液轉移到容量瓶中
②未等稀釋后的H2SO4溶液冷卻至室溫就轉移到容量瓶中
③將濃H2SO4直接倒入燒杯,再向燒杯中注入蒸餾水來稀釋濃H2SO4
④定容時,加蒸餾水超過標線,又用膠頭滴管吸出
⑤轉移前,容量瓶中含有少量蒸餾水
⑥定容搖勻后,發現液面低于標線,又用膠頭滴管加蒸餾水至標線
⑦定容時,俯視標線。組卷:313引用:11難度:0.5 -
30.已知常溫下的反應:2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O。
(1)元素得電子,元素被氧化(填元素名稱)。
(2)氧化劑與還原劑的數目之比是,氧化產物與還原產物的數目之比為。
(3)若有7.3g氯化氫被消耗,則產生氯氣的質量為g。
(4)該反應的離子方程式為。組卷:2引用:1難度:0.7


