2021-2022學年陜西省渭南市韓城市高二(下)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本大題共16小題,每小題3分,計48分。每小題只有一個選項是符合題意的)
-
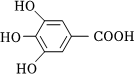 1.300多年前,著名化學家波義耳發現了鐵鹽與沒食子酸(結構式如圖所示)的顯色反應,并由此發明了藍黑墨水.與制造藍黑墨水相關的基團可能是( )
1.300多年前,著名化學家波義耳發現了鐵鹽與沒食子酸(結構式如圖所示)的顯色反應,并由此發明了藍黑墨水.與制造藍黑墨水相關的基團可能是( )A.苯環 B.羧基 C.羧基中的羥基 D.酚羥基 組卷:108引用:14難度:0.9 -
2.我國科學家利用C16H34、C18H38的固態和液態轉化提出“綠色制冷”新思路。C16H34、C18H38屬于( )
A.烷烴、烯烴 B.烯烴、芳香烴 C.烷烴、烷烴 D.烷烴、芳香烴 組卷:47引用:3難度:0.8 -
3.下列系統命名正確的是( )
A.2,3-二乙基-1-戊烯 B.2-甲基-4-乙基戊烷 C.2-甲基-3-丁炔 D.2,3,3-三甲基丁烷 組卷:33引用:2難度:0.7 -
4.下列不涉及蛋白質變性的是( )
A.給重金屬中毒的病人服用大量牛奶 B.在雞蛋清溶液中加入飽和硫酸銨溶液,有沉淀析出 C.在雞蛋清溶液中加入醋酸鉛溶液,有沉淀析出 D.用福爾馬林溶液浸泡動物標本 組卷:71引用:1難度:0.8 -
5.下列實驗操作或安全事故處理中正確的是( )
A.苯酚不慎沾到皮膚上,應立即用濃NaOH溶液清洗 B.配制氫氧化銅懸濁液時,需在5mL2%CuSO4溶液中滴入3~4滴5%NaOH溶液 C.進行蒸餾操作時,若忘記加碎瓷片,應立即停止加熱,待溶液冷卻后加入碎瓷片再加熱 D.用濃氨水洗滌做過銀鏡反應的試管 組卷:0引用:2難度:0.5 -
6.我國科學家以二氧化碳為原料,不依賴植物光合作用,可直接人工合成淀粉。通過核磁共振等檢測方法發現,人工合成淀粉分子與天然淀粉分子的結構組成一致。下列說法正確的是( )
A.該成果有利于國家糧食安全以及實現“碳達峰、碳中和” B.在咀嚼淀粉類食物時,淀粉會水解產生葡萄糖 C.可利用含碘的化合物檢驗淀粉的存在 D.淀粉中含有C、H、O、N四種元素 組卷:9引用:2難度:0.7 -
7.乙酸苯甲酯可作茉莉、白蘭、月下香等香精的調和香料。它可以用甲苯和乙醇為原料進行人工合成。合成路線如圖:
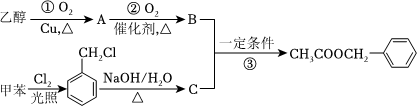
下列說法錯誤的是( )A.②③的反應類型為氧化反應,取代反應 B.甲苯的一氯代物有4種 C.有機物A能與飽和CuSO4溶液在加熱條件下反應生成磚紅色沉淀 D.加入過量的有機物B可以提高有機物C的轉化率 組卷:37引用:2難度:0.4
二、非選擇題(本大題共5小題,計52分)
-
20.苦杏仁酸在醫藥工業可用于合成頭孢羥唑、羥芐唑、匹莫林等的中間體,如圖路線是合成苦杏仁酸及其衍生物的一種方法:
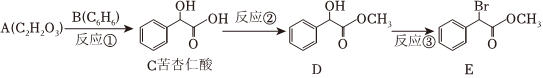
完成下列填空:
(1)試寫出A的結構簡式,C中含氧官能團的名稱為。
(2)反應①的反應類型為,反應②的條件為。
(3)反應③的化學方程式為。
(4)兩個C分子可以反應生成具有三個六元環的化合物F,則F的結構簡式為。
(5)寫出滿足下列條件的C的一種同分異構體。
a.既能發生銀鏡反應,又能發生水解反應
b.苯環上有2種化學環境的氫原子
(6)乙醇酸可用于工業制備聚乙醇酸,已知:RCH2COOHRCHClCOOH,請以乙醇為原料(無機試劑任選)設計制備乙醇酸(HOCH2COOH)的合成路線PCl3△。(合成路線的表示方式為:甲乙…反應試劑反應條件目標產物)反應試劑反應條件組卷:89引用:4難度:0.5 -
21.苯甲醇與苯甲酸都是常見化工原料,在化工生產中有廣泛應用。工業上常在堿性條件下由苯甲醛來制備。某實驗室模擬其生產過程,實驗原理、實驗方法及步驟如下:
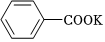
實驗原理:2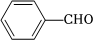 +KOH→
+KOH→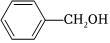 +
+
有關資料:
苯甲醛空氣中極易被氧化,生成白色苯甲酸。名稱 相對分子質量 熔點
(℃)沸點
(℃)溶解性 水 醇 醚 苯甲醛 106 -26 179.62 微溶 易溶 易溶 苯甲酸 122 122.13 249 微溶 易溶 易溶 苯甲醇 108 -15.3 205.7 微溶 易溶 易溶 乙醚 74 -116.3 34.6 微溶 易溶 --
實驗步驟及方法如下:
Ⅰ.向盛有足量KOH溶液的反應器中,分批加入新蒸過的13.5mL(14.0g)苯甲醛,持續攪拌至反應混合物變成白色蠟糊狀A,轉移至錐形瓶中靜置24小時以上;反應裝置如圖1。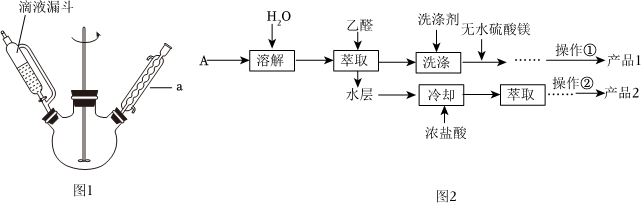
Ⅱ.步驟Ⅰ所得產物后續處理如圖2。
(1)儀器a的名稱為。
(2)步驟1中苯甲醛需要分批加入且適時冷卻,其原因是。
(3)為獲取產品1,將乙醚萃取液依次用飽和亞硫酸氫鈉溶液、10%碳酸鈉溶液和水進行洗滌并分液。乙醚萃取液的密度小于水,取分液后(填“上”或“下”)層液體加入無水MgSO4,其作用為,操作①含多步操作,其中最后一步分離操作是對乙醚和產品1進行分離,其名稱為。
(4)水層中加入濃鹽酸發生反應的離子方程式為。
(5)操作②包含溶解、蒸發濃縮、結晶、晾干,下列儀器中在該操作中不需要用到的有。(填序號)
A.分液漏斗
B.蒸發皿
C.研缽
D.玻璃棒
(6)①若產品2產率比預期值稍高,可能原因是。
A.過濾后未干燥完全
B.產品中混有其他雜質
C.過濾時濾液渾濁
D.部分苯甲醛被直接氧化為苯甲酸
②產品2經干燥后稱量,質量為6.1g,計算其產率為。(保留3位有效數字,寫出計算過程)組卷:18引用:3難度:0.5


