2016-2017學年福建省龍巖一中高一(下)第三次模塊化學試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(共20小題,每小題2分,滿分40分)
-
1.重水(
H2O)是重要的核工業(yè)原料,關于氘原子(21H)說法正確的是( )21A.通過化學變化可實現 H與21H的相互轉化11B. H與21H的核外電子排布方式相同,化學性質相同11C. H與21H核外電子數和中子數均為111D. H與H2互為同素異形體21組卷:21引用:1難度:0.9 -
2.對Al、Fe二種金屬元素,下列說法正確的是( )
A.鋁能夠穩(wěn)定存在于空氣中,而鐵很容易生銹,說明鐵比鋁活潑 B.等物質的量的Al、Fe分別與足量鹽酸反應放出等質量的H2 C.二者的氫氧化物都不可以通過氧化物化合反應直接制備 D.二者的單質都能與強堿溶液反應生成H2 組卷:75引用:4難度:0.7 -
3.北京大學和中國科學院的化學工作者已成功研制出堿金屬與C60形成的球碳鹽K3C60,實驗測知該物質屬于離子化合物,具有良好的超導性。下列有關分析正確的是( )
A.K3C60中只有離子鍵 B.K3C60中不含共價鍵 C.該晶體在熔融狀態(tài)下能導電 D.C60與12C互為同位素 組卷:57引用:4難度:0.9 -
4.有些科學家提出硅是“21世紀的能源”,下列關于硅及其化合物的說法正確的是( )
A.石英坩堝耐高溫,可用來加熱熔化燒堿、純堿等固體 B.高純度的硅單質廣泛用于制作光導纖維 C.水泥、玻璃、水晶飾物都是硅酸鹽制品 D.陶瓷是人類應用很早的硅酸鹽材料 組卷:58引用:1難度:0.9 -
5.如圖表示堿金屬的某些性質與核電荷數的變化關系,下列各性質中不符合圖示關系的是( )
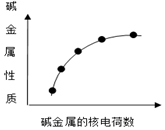
A.還原性 B.與水反應的劇烈程度 C.最高價氧化物對應水化物的堿性 D.簡單陽離子的氧化性 組卷:45引用:1難度:0.9 -
6.下列變化過程中,共價鍵被破壞的是( )
A.冰融化成水 B.氯氣溶于水 C.氯化鈉熔化 D.酒精溶于水 組卷:29引用:1難度:0.7 -
7.下列屬于氧化還原反應同時能量的變化符合如圖的是( )
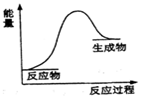
A.Ba(OH)2?8H2O與NH4Cl反應 B.鋁與稀鹽酸 C.灼熱的炭與水蒸氣生成一氧化碳和氫氣的反應 D.煤與O2的燃燒反應 組卷:28引用:1難度:0.7 -
8.質量數為A,核內中子數為N的R2+離子與16O所形成的Wg氧化物中所含質子的物質的量為( )
A. (A-N+8)molWA+16B. (A-N+10)molWA+16C.(A-N+8)mol D. (A-N+6)molWA組卷:62引用:50難度:0.7 -
9.將某份鐵鋁合金樣品均分為兩份,一份加入足量鹽酸,另一份加入足量NaOH溶液,同溫同壓下產生的氣體體積比為3:2,則樣品中鐵、鋁物質的量之比為( )
A.3:2 B.2:1 C.3:4 D.4:3 組卷:159引用:27難度:0.7
二、填空題(共4題,共56分)
-
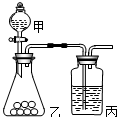 27.某同學探究同周期元素性質的遞變規(guī)律,并討論影響化學反應速率的因素,選用的試劑如下,鎂條、鋁條、鈉、高錳酸鉀固體、Na2S溶液、濃鹽酸、0.5mol/L的鹽酸,酚酞試液,其設計的實驗方案及部分實驗現象如下表:請回答下列問題:
27.某同學探究同周期元素性質的遞變規(guī)律,并討論影響化學反應速率的因素,選用的試劑如下,鎂條、鋁條、鈉、高錳酸鉀固體、Na2S溶液、濃鹽酸、0.5mol/L的鹽酸,酚酞試液,其設計的實驗方案及部分實驗現象如下表:請回答下列問題:
(1)實驗①②表明同周期元素從左往右金屬性逐漸實驗步驟 實驗現象 ①將一小塊金屬鈉放入滴有酚酞試液的冷水中 鈉塊浮在水面上,熔化成閃亮的小球,做不定向移動,隨之消失,溶液變紅色 ②將表面積大致相同的鎂條和鋁條(均已用砂紙打磨過),分別投入足量的相同體積的0.5mol/L的鹽酸中 鎂條劇烈反應,迅速產生大量的無色氣體,而鋁條反應不十分劇烈,產生無色氣體,鎂條消失比鋁條快 (填“增大”、“減小”或“不變”)。
(2)已知高錳酸鉀常溫下可氧化濃鹽酸生成氯氣。用右圖所示裝置比較氯與硫的非金屬性。甲、乙所裝藥品分別為、。裝置丙中實驗現象為有淡黃色沉淀生成,離子方程式為
(3)由實驗②可得出決定化學反應快慢的主要因素是。
(4)請設計一個實驗方案證明濃度對反應速率的影響:。組卷:6引用:1難度:0.5 -
 28.已知A、B、C、D、X、Y、Z七種短周期主族元素的原子序數依次增大,A是元素周期表中原子半徑最小的,B的最高價氧化物的水化物與其氫化物反應生成鹽,且B的核電荷數比Y的最外層電子數多1.C原子的最外層電子數是次外層電子數的3倍,D原子半徑在同周期中除稀有氣體外最大,X是同周期中簡單離子半徑最小的元素。請回答下列問題:
28.已知A、B、C、D、X、Y、Z七種短周期主族元素的原子序數依次增大,A是元素周期表中原子半徑最小的,B的最高價氧化物的水化物與其氫化物反應生成鹽,且B的核電荷數比Y的最外層電子數多1.C原子的最外層電子數是次外層電子數的3倍,D原子半徑在同周期中除稀有氣體外最大,X是同周期中簡單離子半徑最小的元素。請回答下列問題:
(1)B在元素周期表的位置為。
(2)C、D、Y、Z三種元素形成的簡單離子的半徑由大到小的順序為(用離子符號表示)。
(3)Y的離子結構示意圖,A與C形成的10電子分子的電子式為。
(4)下列事實能證明C與Y非金屬性強弱的是(選填字母序號)。
A.常溫下,Y的單質呈固態(tài),C的單質呈氣態(tài)
B.C的氫化物的穩(wěn)定性強于Y的氫化物
C.C與Y形成的化合物中,Y呈正價
D.C的氫化物的沸點高于Y的氫化物
E、C的最高價氧化物對應的水化物酸性強于Y的最高價氧化物對應的水化物
(5)已知Y、Z兩種元素形成的化合物H,H結構與過氧化氫相似,屬于(填“離子”或“共價”)化合物。6.75g的H中含有的共用電子對數目為。
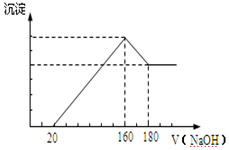
(6)將一定質量的X與鎂的合金投入100mL一定濃度的鹽酸中,合金完全溶解。向所得溶液中滴加濃度為5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的體積關系如圖。(橫坐標體積單位是mL,縱坐標質量單位是 g)求:
①加入NaOH溶液160-180mL過程中反應的離子方程式為。
②合金中Mg的質量為g,
所用HCl 的物質的量濃度為mol/L。組卷:26引用:1難度:0.1


