2020-2021學年山東省東營市東營區九年級(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括12小題,共40分。1至8題每題3分,9至12題每題4分,每小題只有一個選項符合題意)
-
1.下列屬于化學性質的是( )
A.還原性 B.硬度 C.導電性 D.延展性 組卷:28引用:1難度:0.9 -
2.下列屬于化學變化的是( )
A.海水曬鹽 B.金屬生銹 C.油水乳化 D.塑料成型 組卷:11引用:1難度:0.8 -
3.下列說法錯誤的是( )
A.化學反應伴隨著能量的吸收和釋放 B.風能、水能、地熱能屬于二次能源 C.天然的食品添加劑對健康是無害的 D.玻璃鋼屬于復合材料 組卷:62引用:1難度:0.8 -
4.稀硫酸中能使紫色石蕊試液變紅色的微粒是( )
A.硫酸分子 B.氫離子 C.硫酸根離子 D.水分子 組卷:340引用:1難度:0.6 -
5.對于粗鹽提純的有關認識錯誤的是( )
A.除去食鹽水中可溶性雜質的化學原理是使雜質離子以沉淀或氣體的形式從食鹽水中分離出去 B.只用物理方法就能除去食鹽水中的雜質離子 C.海水曬鹽屬于蒸發結晶 D.蒸發結晶食鹽時,若待水分全部蒸發才停止加熱,會引起食鹽“迸濺” 組卷:125引用:1難度:0.6 -
6.保護環境,人人有責。下列說法正確的是( )
A.在車用汽油中添加乙醇,目的是為了汽油的燃燒效率 B.用3Cu+8HNO3(稀)═3Cu(NO3)2(稀)+2NO↑+4H2O反應制Cu(NO3)2,符合“綠色化學”理念 C.只要消除煤炭燃燒產生的二氧化硫就能消除酸雨 D.在目前推行的垃圾分類中,充電電池屬于有害垃圾 組卷:10引用:1難度:0.7
三、實驗題(共16分)
-
17.實驗室有一瓶失去標簽的稀鹽酸,化學興趣小組的同學欲用氫氧化鈉標準溶液測定此稀鹽酸中溶質的質量分數,請根據所學知識完成以下問題。
(1)【配制20g 10%氫氧化鈉標準溶液】如圖為能制操作流程圖: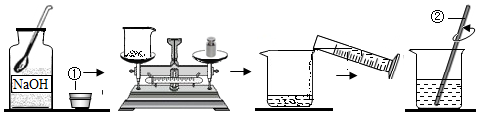
固體氫氧化鈉的顏色是,稱量的質量是,稱量時用小燒杯盛放的原因是;①的名稱是(選填“橡皮塞”或“玻璃塞”),圖中的錯誤是;②操作的名稱是。
(2)【氫氧化鈉與稀鹽酸反應】為便于觀察反應終點,提前向20g 10%氫氧化鈉標準溶液中滴加指示劑,然后逐滴加入待測稀鹽酸,同時輕輕搖動混合溶液,待溶液顏色時表示恰好完全反應,此時消耗稀鹽酸的質量為25g。可計算得出稀鹽酸的質量分數為,反應的化學方程式是,反應類型屬于。
(3)【實驗評價與反思】稱量出的氫氧化鈉固體,若放置在空氣中一段時間后再加水配制,其它操作、條件不變,會導致計算稀鹽酸質量分數(選填“偏大”、“偏小”或“無影響”)。從微觀角度分析,氫氧化鈉與稀鹽酸反應的實質是。在反應達到終點前,下列能表示溶液中微粒存在狀態的圖示為(選填字母序號)。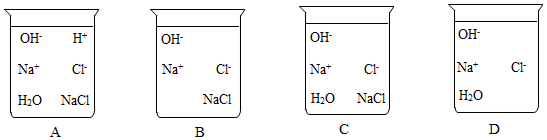
(4)向氫氧化鈉溶液中滴加鹽酸反應過程中,混合溶液除了pH有變化外同時還伴隨著能量的變化。下列能正確表示相應變化的圖象是(選填字母序號)。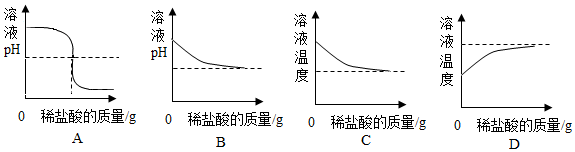 組卷:44引用:1難度:0.5
組卷:44引用:1難度:0.5
四、計算題(共9分)
-
18.為了測定某銅鋅合金(即銅鋅混合物)中鋅的質量分數,某同學利用該合金與稀硫酸的反應,進行了三次實驗,所得相關的實驗數據記錄如下(實驗中的誤差忽略不計):
(1)試計算該銅鋅合金中鋅的質量分數.第一次 第二次 第三次 所取合金的質量/g 25 25 50 所用稀硫酸的質量/g 120 160 100 生產氫氣的質量/g 0.4 0.4 0.4
(2)從上表數據分析,當所取合金與所用稀硫酸的質量比為時,表明合金中的鋅與稀硫酸中的硫酸恰好完全反應.組卷:317引用:6難度:0.3


