2022-2023學年山東省青島市即墨區高一(上)期中化學試卷
發布:2024/12/16 23:1:51
一、選擇題:(本題共16小題,每小題3分,共48分。每小題只有一個選項符合題目要求。)
-
1.下列科學研究領域中,不屬于化學研究范疇的是( )
A.國家游泳館水立方采用的覆蓋膜為先進的EFET膜,具有防火、抗老化等功能 B.兩個氫原子核聚變成一個氦核,釋放出巨大能量,用于發電 C.利用分子組裝技術組裝分子機器 D.研究物質性質,用于合成殺死新型冠狀病毒的物質 組卷:17引用:1難度:0.7 -
2.化學與生活生產科技環境等關系密切。下列說法錯誤的是( )
A.用過氧化鈉作潛水艇的供氧劑 B.我國成功研制出Zn5(OH)8(NO3)2納米片,該化合物屬于堿式鹽 C.小蘇打(NaHCO3)用于制作糕點 D.地震災區和洪澇災區都用漂白粉消毒,主要是利用漂白粉溶液的堿性 組卷:9引用:1難度:0.7 -
3.朱自清在《荷塘月色》中寫道:“薄薄的青霧浮起在荷塘……光是隔了樹照過來的,高處叢生的灌木,落下參差的斑駁黑影……”在這段美文中包含的化學知識正確的是( )
A.荷塘上方的薄霧不具有穩定性,容易沉降 B.月光穿過薄霧時產生了丁達爾效應 C.“大漠孤煙直”中的孤煙成分和這種薄霧的成分相同 D.薄霧中的微粒直徑大約是2.5pm(1pm=1.0×10-12m) 組卷:12引用:3難度:0.8 -
4.下列物質的應用錯誤的是( )
A.金屬鈉可用于冶煉金屬鈦 B.活性炭用于殺菌除異味 C.ClO2用作漂白劑和消毒劑 D.鈉、鉀合金用于核工業原子反應堆導熱劑 組卷:12引用:1難度:0.7 -
 5.在海洋碳循環中,通過如圖所示的途徑固碳。下列說法錯誤的是( )
5.在海洋碳循環中,通過如圖所示的途徑固碳。下列說法錯誤的是( )A.該循環過程中未涉及氧化還原反應 B.碳酸氫鈉的電離方程式為NaHCO3═Na++HCO3- C.該循環減少了碳的排放,有利于實現“碳達峰、碳中和” D.鈣化作用的離子方程式之一為Ca2++2HCO3-═CaCO3↓+CO2↑+H2O 組卷:79引用:12難度:0.7 -
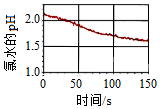 6.數字化實驗將傳感器、數據采集器和計算機相連,可利用信息技術對化學實驗進行數據的采集和分析。如圖是數字化實驗得到的光照過程中氯水的pH變化情況。對此,下列有關說法正確的是( )
6.數字化實驗將傳感器、數據采集器和計算機相連,可利用信息技術對化學實驗進行數據的采集和分析。如圖是數字化實驗得到的光照過程中氯水的pH變化情況。對此,下列有關說法正確的是( )A.光照使氯水中的次氯酸分解為鹽酸,溶液的酸性增強 B.隨著對氯水光照時間的延長,氯水的漂白性將增強 C.光照過程中,氯水pH減小的同時,溶液中Cl-的濃度也不斷減小 D.pH減小的主要原因是光照引起了Cl2溶解度的減小,氯氣逸出,導致了溶液中H+濃度減小 組卷:285引用:20難度:0.7
二、非選擇題:(本題共4小題,共52分)
-
19.Ⅰ.NaNO2是一種可溶性鹽,它能被常見的強氧化劑氧化。回答下列問題:
(1)金屬加工后的廢液中含有2%~5%的NaNO2,它是一種環境污染物。人們用NH4Cl溶液來處理此廢液,使亞硝酸鈉轉化為無毒物質。該反應分兩步進行:
第一步:NaNO2+NH4Cl═NaCl+NH4NO2
第二步:NH4NO2N2↑+2H2O△
下列對上述反應的敘述中正確的是(填字母)。
①兩步均為氧化還原反應
②第二步NH4NO2僅發生氧化反應
③第二步NH4NO2發生了分解反應
④第二步中NH4NO2既被氧化又被還原
⑤第一步為復分解反應
A.①③
B.①④
C.②③④
D.③④⑤
(2)實驗室中,亞硝酸鈉可用來處理過量的疊氮化鈉,有關反應的化學方程式如下:
a.NaNO2+H2SO4═HNO2+NaHSO4
b.2NaN3+2HNO2═3N2↑+2NO↑+2NaOH
用單線橋法標出b反應中電子轉移情況:。
(3)Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O組成的一個氧化還原反應體系中,發生BiO3-→Bi3+的反應過程。
①該反應中,被氧化的元素是(填元素符號),氧化劑是(填離子符號)。
②將以上物質分別填入下面對應的橫線上,并配平該反應:++═++H2O。
Ⅱ.某次實驗需用450mL0.35mol/L的H2SO4溶液,某同學用密度為1.4g?cm-3質量分數49%的H2SO4溶液進行配制,請回答下列問題:
(1)實驗需要的玻璃儀器除了燒杯、量筒、玻璃棒,還有、。
(2)計算:配制本次實驗需要的稀硫酸需用量筒量取上述49%的H2SO4mL。
(3)配制過程:①用量筒量取所需質量分數為49%的H2SO4溶液
②將濃硫酸緩緩注入盛有適量蒸餾水的燒杯中,邊加邊攪拌
③用玻璃棒引流將燒杯中的溶液轉移到已經檢漏的合適規格的容量瓶中
④洗滌燒杯和玻璃棒2~3次,洗滌液也注入容量瓶中,輕輕搖動容量瓶,使溶液混合均勻
⑤向容量瓶中加入蒸餾水,在距離刻度1~2cm時,改用膠頭滴管加蒸餾水至刻度線
⑥蓋好瓶塞,反復上下顛倒,搖勻
⑦將配制好的溶液轉移至試劑瓶中待用
上述配制溶液的步驟存在缺失,缺少的步驟是,應放在步驟之前進行(填“序號”)。
(4)在橫線上填寫下列各種情況對所配制溶液濃度的影響(選填“偏高”、“偏低”或“無影響”)。
①所用的濃硫酸長時間放置在密封不好的容器中。
②用量筒量取濃硫酸時仰視液面。組卷:16引用:2難度:0.4 -
20.回答下列問題
(1)標準狀況下,8gCH4與LH2S氣體含有相同的氫原子數。
(2)19g某二價金屬的氯化物RCl2中含有0.4mol的Cl-,則R的相對原子質量為。
(3)如圖是“康師傅”牌飲用礦泉水的標簽的部分內容。
請認真閱讀標簽內容,計算:康師傅飲用礦物質水
凈含量:350mL
配料表:純凈水硫酸鎂氯化鉀
保質期:12個月
主要成分:
鉀離子(K+):1.0~27.3mgL
鎂離子(Mg2+):0.1~4.8mg/L
氯離子(Cl-):10~27.3mg/L
硫酸根離子(SO42-):0.4~19.2mgL
①鎂離子的物質的量濃度的最大值是。
②一瓶合格的這種礦泉水中硫酸根離子的物質的量不能超過mol。
(4)VLFe2(SO4)3溶液中含Fe3+mg,則溶液中SO42-的物質的量濃度為mol?L-1。
(5)摩爾是以0.012kg12C中所含的原子數目為標準,來衡量其它粒子集體中所含粒子數目的多少。如果定義3.01×1023個12C原子的物質的量為1mol,那么此時標準狀況下,氣體摩爾體積的數值約為L/mol。組卷:36引用:3難度:0.4


