2021-2022學年湖北省部分名校聯考高一(上)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共15小題,每小題3分,共45分.在每小題給出的四個選項中,只有一項是符合題目要求的.
-
1.瓷器是中國勞動人民的重要發明之一,是中國勞動人民智慧和力量的結晶.下列制瓷工序中涉及化學變化的是( )
A.粉碎瓷石 B.淘洗瓷粉 C.取泥制坯 D.開窯燒制 組卷:3引用:2難度:0.8 -
2.下列物質的分類正確的是( )
酸 堿 鹽 酸性氧化物 堿性氧化物 A HNO3 NaOH CaCO3 SO3 Fe2O3 B NaHSO4 Ca(OH)2 NaCl CO2 Na2O2 C HCl Na2CO3 CuSO4?5H2O SO2 MgO D H2SO4 KOH NaHCO3 CO CaO A.A B.B C.C D.D 組卷:19引用:4難度:0.7 -
3.實驗室需要250mL0.1mol?L-1NaOH溶液。下列儀器中配制溶液時肯定不需要的是( )
A. 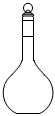
B. 
C. 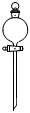
D. 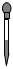 組卷:30引用:5難度:0.7
組卷:30引用:5難度:0.7 -
4.下列物質中,物質的量為0.05mol的是( )
A.4.0gMgO B.3.2gFe2O3 C.2.8gN2 D.4.9gH2SO4 組卷:6引用:2難度:0.7 -
5.下列有關鈉的取用方法、保存及存在形式的描述正確的是( )
A.實驗中,取用少量的金屬鈉可用手直接取 B.實驗室中,鈉通常保存在煤油或石蠟油中 C.實驗后剩余的金屬鈉要丟入垃圾桶,不能放回原試劑瓶中 D.鈉在自然界中主要以化合態形式存在,少量以游離態形式存在 組卷:98引用:5難度:0.6 -
6.下列反應中屬于氧化還原反應的是( )
A.HCl+NaOH═NaCl+H2O B.ZnO+H2SO4═ZnSO4+H2O C.3Cl2+6KOH 5KCl+KClO3+3H2O加熱D.NaHSO4+BaCl2═BaSO4↓+NaCl+HCl 組卷:10引用:2難度:0.7
二、非選擇題:本題共4小題,共55分.
-
18.NaHCO3是一種工業用化學品,50℃以上開始逐漸分解生成碳酸鈉、二氧化碳和水,270℃時完全分解。NaHCO3在水中的溶解度小于Na2CO3在水中的。回答下列問題:
(1)可用于治療胃酸過多的是(填“NaHCO3”或“Na2CO3”),不能用澄清石灰水區分NaHCO3和Na2CO3的原因是。
(2)實驗室將CO2、NH3通入飽和食鹽水中來制備NaHCO3,先通入的是(填“CO2”或“NH3”),反應的化學方程式為NaCl+H2O+CO2+NH3═NaHCO3↓+NH4Cl;該反應不宜在超過50℃的水浴中進行,原因是。
(3)制取NaHCO3所需要的CO2采用圖甲裝置進行制備。當錐形瓶中的固體為石灰石時,分液漏斗中應盛放(填試劑名稱),為獲得較為純凈的CO2,凈化裝置(圖乙)中試劑A為(填化學式)。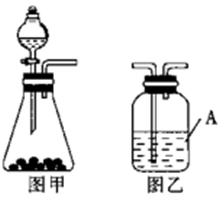
(4)通過該實驗所獲得的NaHCO3晶體常含有NaCl(假設僅含此一種雜質)。現稱取上述NaHCO3晶體試樣9.36g于燒杯中,加入過量稀HNO3使固體樣品充分反應,再加入過量的硝酸銀溶液。經過濾、洗滌、干燥得到沉淀物的質量為5.74g,則NaHCO3樣品中NaCl的質量分數為.寫出上述反應涉及的離子方程式:、。組卷:5引用:2難度:0.6 -
19.設NA為阿伏加德羅常數的值,請回答下列問題:
(1)O2的摩爾質量為g?mol-1,1mol O2中含有個O2分子.
(2)用14.2g無水硫酸鈉配制成500mL溶液,溶質的物質的量濃度為mol?L-1;若從中取出50mL,則取出的溶液中溶質的物質的量濃度為mol?L-1,溶質的質量為g,若將這50mL溶液加水稀釋到100mL,則所得溶液中Na+的物質的量濃度為mol?L-1.
(3)將6.5g鋅投入100mL某濃度的稀硫酸中,鋅和稀硫酸恰好完全反應,則:
①反應中生成的H2在標準狀況下的體積約為L.
②若用質量分數為98%的濃硫酸(ρ=1.84g?mL-1)來配制上述稀硫酸,需要濃硫酸的體積為(保留一位小數)mL.組卷:11引用:2難度:0.6


