2022-2023學年寧夏銀川市賀蘭一中高一(上)期中化學試卷(A卷)
發布:2024/11/18 21:30:2
一、選擇題(每小題2.5分,共計50分)
-
1.按照物質的樹狀分類法和交叉分類法,HNO3應屬于( )
①酸②氫化物③氧化物④含氧酸⑤難揮發性酸⑥一元酸⑦化合物A.①②③④⑤⑥⑦ B.①④⑥⑦ C.①⑦ D.①④⑤⑥ 組卷:14引用:2難度:0.6 -
2.下列關于電解質的說法正確的是( )
A.氯化鈉晶體不導電,所以NaCl不是電解質 B.銅能導電,所以銅是電解質 C.CO2溶于水能導電,所以CO2是電解質 D.BaSO4在熔融下能導電,所以BaSO4是電解質 組卷:17引用:3難度:0.7 -
3.下列反應能用離子方程式CO32-+2H+═CO2↑+H2O表示的是( )
A.Na2CO3+2CH3COOH═2CH3COONa+CO2↑+H2O B.NH4HCO3+HNO3═NH4NO3+CO2↑+H2O C.BaCO3+2HCl═BaCl2+CO2↑+H2O D.K2CO3+2HCl═2KCl+CO2↑+H2O 組卷:50引用:3難度:0.6 -
4.下列物質在水溶液中的電離方程式錯誤的是( )
A.HCl═H++Cl- B.MgCl2═Mg2++2Cl- C.NaHSO4═Na++HSO4- D.Ba(OH)2═Ba2++2OH- 組卷:17引用:1難度:0.9 -
5.在強酸性溶液中能大量共存并且溶液為無色透明的離子組是( )
A.Ba2+、Na+、NO3-、SO42- B.Mg2+、Cl-、Al3+、SO42- C.K+、Cl-、CO32-、NO3- D.Ca2+、Na+、Fe3+、NO3- 組卷:80引用:7難度:0.6 -
6.亞硝酸(HNO2)既可作氧化劑又可作還原劑,當它在反應中作氧化劑時,可能生成的產物是( )
A.N2 B.N2O3 C.HNO3 D.NO2 組卷:28引用:2難度:0.7 -
7.根據下列反應進行判斷,各微粒氧化性強弱順序正確的是( )
①2Fe3++2I-═2Fe2++I2②2Fe2++Cl2═2Fe3++2Cl-A.Cl2>Fe3+>I2 B.Cl?>I->Fe2+ C.Cl2>I2>Fe3+ D.I->Fe2+>Cl- 組卷:86引用:3難度:0.8 -
8.為除去下列物質中所含的雜質,選用的實驗操作方法正確的是( )
A.FeCl2溶液(FeCl3):加入稍過量的鐵粉,過濾 B.Cl2(HCl氣體):通過足量的NaOH溶液 C.CO2(HCl):通過盛有飽和Na2CO3溶液的洗氣瓶 D.NaHCO3固體(Na2CO3):加熱至固體質量不再變化 組卷:3引用:1難度:0.5
二、填空題
-
24.根據所學知識,完成下列問題。
(1)取少量Fe2O3粉末于試管中加入適量鹽酸,反應后得到的溶液呈色。將該溶液中滴入NaOH溶液,可以觀察到的現象,反應的離子反應方程式為。
(2)在小燒杯中加入25mL蒸餾水,加熱至沸騰后,向沸水中加入2mLFeCl3溶液,繼續煮沸至溶液呈紅褐色,即可制得Fe(OH)3膠體。該過程發生的化學反應方程式為:,用激光筆照射燒杯中的液體,可以看到。
用制得的Fe(OH)3膠體進行下列實驗:
①將其裝入U形管中,用石墨電極接通直流電,通電一段時間后,發現陰極附近的顏色加深,這種現象稱為。
②向其中滴入過量稀硫酸,先產生紅褐色沉淀,后沉淀全部溶解,其原因是。
③提純此分散系常用的方法是。組卷:12引用:1難度:0.6 -
25.回答下列問題。
(1)實驗室常用如圖所示裝置來制取和觀察Fe(OH)2在空氣中被氧化時顏色的變化。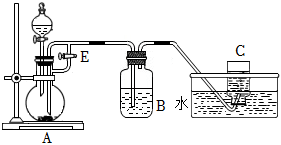
實驗時在A中加入鐵屑和稀硫酸,B中加入一定量的NaOH溶液,則A中發生的反應的離子方程式是:。實驗開始時先將活塞E(填“打開”或“關閉”),C中收集到氣體的主要成分是。實驗結束后拔去裝置B中的橡皮塞,使空氣進入,裝置B中發生的現象為。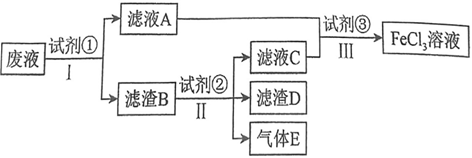 (2)從制造印刷電路板的腐蝕廢液(主要含FeCl3、FeCl2、CuCl2)中回收銅,并重新獲得FeCl3溶液,處理流程如圖所示:
(2)從制造印刷電路板的腐蝕廢液(主要含FeCl3、FeCl2、CuCl2)中回收銅,并重新獲得FeCl3溶液,處理流程如圖所示: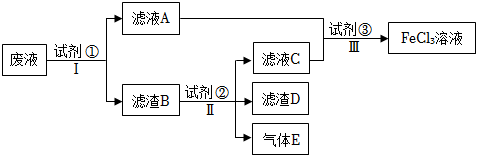
已知試劑①為鐵,試劑②為稀鹽酸,則濾渣B的成分為,若試劑③為氯水,則步驟Ⅱ的離子反應方程式為,檢驗廢液中Fe3+存在的最佳試劑是(填標號),檢驗時實驗現象為。
A.氫氧化鈉溶液
B.酸性KMnO4溶液
C.氯水
D.KSCN溶液組卷:160引用:1難度:0.7


