2021-2022學年江蘇省常州市八校高一(下)期末化學試卷
發布:2025/1/7 23:0:2
一、單選題:共15題,每題3分,共45分。每題只有一個選項最符合題意。
-
1.化學與社會、生產、生活密切相關。下列說法正確的是( )
A.纖維素、油脂、蛋白質均是天然高分子化合物 B.煤的液化、石油的裂化和油脂的皂化都屬于化學變化 C.聚乙烯能使高錳酸鉀溶液褪色 D.棉花、羊毛、蠶絲等天然纖維的成分都是纖維素 組卷:21引用:1難度:0.5 -
2.下列表示不正確的是( )
A.CH4分子的空間填充模型: 
B.硫離子結構示意圖 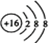
C.NH3的結構式為 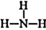
D.乙醛的結構簡式CH3COH 組卷:41引用:2難度:0.7 -
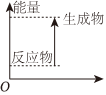 3.下列反應中熱量變化與圖一致的是( )
3.下列反應中熱量變化與圖一致的是( )A.天然氣的燃燒能量生成物 B.鋅與稀硫酸反應 C.NaOH溶液和HNO3溶液反應反應物 D.Ba(OH)2?8H2O晶體和NH4Cl晶體反應 組卷:48引用:1難度:0.8 -
4.反應2NO+2CO
N2+2CO2可應用于汽車尾氣凈化,下列關于該反應的說法正確的是( )一定條件A.升高溫度能加快反應速率 B.減小NO濃度能加快反應速率 C.使用恰當的催化劑不能加快反應速率 D.達到化學平衡時,CO能100%轉化為產物 組卷:37引用:3難度:0.6 -
5.室溫下,下列各組離子在指定溶液中能大量共存的是( )
A.FeCl2溶液中:K+、H+、NO3-、SO42- B.無色透明溶液中:K+、Mg2+、Cl-、NO3- C.強酸性溶液中:K+、Na+、HCO3-、Cl- D.FeCl3溶液中:Na+、SO42-、SCN-、NO3- 組卷:111引用:1難度:0.6 -
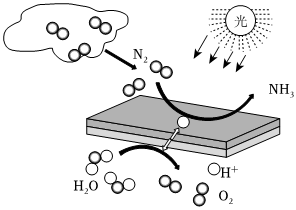 6.近年來,利用半導體光催化實現還原氮氣制備氨氣引起全世界極大關注。如圖是在半導體光催化的作用下,N2被光催化材料捕獲進而被還原實現“N2→NH3”的轉化示意圖。下列說法正確的是( )
6.近年來,利用半導體光催化實現還原氮氣制備氨氣引起全世界極大關注。如圖是在半導體光催化的作用下,N2被光催化材料捕獲進而被還原實現“N2→NH3”的轉化示意圖。下列說法正確的是( )A.此方法不屬于人工固氮技術 B.由轉化示意圖可知,氮氣化學性質很活潑 C.該反應過程中有共價鍵的斷裂和形成 D.該反應的化學方程式N2+H2 2NH3△組卷:179引用:3難度:0.8
一、非單選題:共4題,共55分。
-
18.外觀與NaCl相似的亞硝酸鈉(NaNO2)可用作建筑鋼材緩蝕劑。某學習小組設計如圖裝置制備亞硝酸鈉。(夾持裝置已省略)
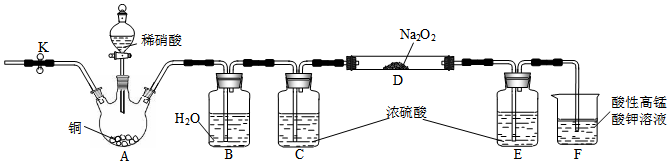
已知:2NO+Na2O2═2NaNO2,2NO2+Na2O2═2NaNO3。
(1)裝置A中發生反應的離子方程式為。
(2)反應開始時先打開止水夾K,通入氮氣至F中產生大量氣泡后再關上止水夾K。
①通入N2的目的是,若實驗時觀察到,說明通入N2未達到預期目的。
②若通入N2未達到預期目的,裝置B可除去NO中的NO2雜質,該反應的化學方程式為。
(3)實驗時裝置D中的實驗現象是。
(4)裝置C、E不可省去,省去會導致產品中混有雜質和。
(5)裝置F的作用是。組卷:116引用:5難度:0.7 -
19.(1)向某體積固定的密閉容器中加入0.3molA、0.1molC和一定量(未知)的B三種氣體,一定條件下發生反應,各物質濃度隨時間變化如圖所示。已知在反應過程中混合氣體的平均相對分子質量沒有變化。請回答:
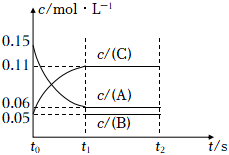
①若t1=15,則t0~t1內反應速率v(C)=,A的轉化率為;
②寫出反應的化學方程式:;
(2)工業上可以通過CO2(g)與H2(g)反應制備CH3OH(g):CO2(g)+3H2(g)?CH3OH(g)+H2O(g) ΔH<0。在一體積固定的密閉容器中投入一定量的CO和H2進行上述反應。下列敘述中能說明上述反應達到平衡狀態的是。
A.反應中CO2與CH3OH的物質的量之比為1:1
B.V正(H2)=3V逆(CH3OH)
C.混合氣體的壓強不隨時間的變化而變化
D.混合氣體的密度不再改變
(3)向恒容密閉容器中充入一定量CO2和H2,在不同催化劑作用下合成甲醇,反應進行相同時間后(均未達到化學平衡狀態),CO2的轉化率隨反應溫度的變化如圖甲所示。其中a點CO2的轉化率高于b點的原因是。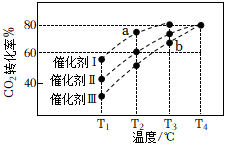
(4)燃料電池是一種高效、環境友好的供電裝置,如圖乙為CH3OH燃料電池的工作原理示意圖,a、b均為惰性電極。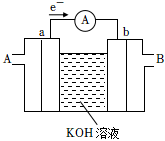
①使用時,空氣從口通入(填“A”或“B”);
②a極的電極反應為:。組卷:39引用:1難度:0.5


