2020年山東省泰安市肥城市高考化學適應性試卷(二)
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題2分,共20分.每小題只有一個選項符合題意.
-
1.化學與人類生活、生產和社會可持續發展密切相關,下列有關說法正確的是( )
A.海水淡化能解決淡水供應危機,向海水中加明礬可以使海水淡化 B.中國華為自主研發的5G芯片巴龍5000的主要材料是Si C.現代科技已經能夠拍到氫鍵的“照片”,直觀地證實了水分子間的氫鍵是一個水分子中的氫原子與另一個水分子中的氧原子間形成的化學鍵 D.用銅片制成的“納米銅”具有非常強的化學活性,在空氣中可以燃燒,說明“納米銅”的還原性比銅片更強 組卷:37引用:1難度:0.7 -
2.下列物質性質和用途都正確且相關的是( )
選項 性質 用途 A FeCl3溶液顯酸性 用于刻蝕電路板 B SO2具有氧化性 SO2常用于漂白秸稈、織物 C HF溶液具有酸性 HF溶液能在玻璃上刻圖案 D CH3CH2OH完全燃燒生成二氧化碳和水并放出大量熱量 乙醇常作清潔能源 A.A B.B C.C D.D 組卷:36引用:3難度:0.7 -
3.為研究廢舊電池的再利用,實驗室利用舊電池的銅帽(主要成分為Zn和Cu)回收Cu并制備ZnO的部分實驗過程如圖所示。下列敘述錯誤的是( )
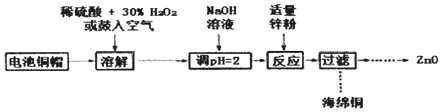
A.“溶解”操作中溶液溫度不宜過高 B.銅帽溶解后,將溶液加熱至沸騰以除去溶液中過量的氧氣或H2O2 C.與鋅粉反應的離子可能為Cu2+、H+ D.“過濾”操作后,將濾液蒸發結晶、過濾洗滌干燥后高溫灼燒即可得純凈的ZnO 組卷:90引用:6難度:0.5 -
 4.短周期主族元素W、X、Y、Z、M是W的最高價氧化物對應的水化物,常溫下,0.01mol?L-1 M溶液的pH=12,X、Y、Z的單質e、f、g在通常狀態下均為氣態,并有如圖所示的轉化關系(反應條件略去)。在雙原子單質分子中,f分子含共用電子對數最多,1個乙分子含10個電子。下列說法正確的是
4.短周期主族元素W、X、Y、Z、M是W的最高價氧化物對應的水化物,常溫下,0.01mol?L-1 M溶液的pH=12,X、Y、Z的單質e、f、g在通常狀態下均為氣態,并有如圖所示的轉化關系(反應條件略去)。在雙原子單質分子中,f分子含共用電子對數最多,1個乙分子含10個電子。下列說法正確的是
( )A.簡單離子半徑:Z>Y>W B.X能分別與W、Y、Z組成共價化合物 C.化合物丙能抑制水電離 D.X與Y元素形成的最簡單的氣態氫化物是極性分子 組卷:19引用:2難度:0.5 -
 5.Y是一種天然除草劑,其結構如圖所示,下列說法正確的是( )
5.Y是一種天然除草劑,其結構如圖所示,下列說法正確的是( )A.Y可以和Na2CO3溶液發生反應 B.Y分子中所有碳原子一定在同一平面內 C.1mol Y最多能與6mol NaOH反應 D.Y與足量的H2發生加成反應的產物含9個手性碳原子 組卷:49引用:1難度:0.5 -
6.設NA為阿伏加德羅常數的值,N表示粒子數。下列敘述正確的是( )
A.6.0g SiO2晶體中含有共價鍵的個數為0.2NA B.將1mol Cl2通入水中,則n(HClO)+n(Cl-)+n(ClO-)=2NA C.3.0g含甲醛(HCHO)的冰醋酸中含有的原子總數為0.4NA D.將CO2通過Na2O2使其質量增加ag時,反應轉移的電子數為 aNA44組卷:59引用:1難度:0.8
三、非選擇題:本題共5小題,共60分.
-
19.氮和硫的氧化物是造成大氣污染的主要物質。研究它們的反應機理,對于消除環境污染有重要意義。
(1)2NO(g)+O2(g)?2NO2(g)的基元反應如下(E為活化能):
2NO(g)N2O2(g)E1=82kJ?mol-1v=k1c2(NO)k1
N2O2(g)2NO(g)E-1=205kJ?mol-1v=k-1c(N2O2)K-1
N2O2(g)+O2(g)2NO2(g)E2=82kJ?mol-1v=k2c(N2O2)?c(O2)k2
2NO2(g)N2O2(g)+O2(g)E-2=72kJ?mol-1v=k-2c2(NO2)K-2
①2NO(g)+O2(g)?2NO2(g)△H=kJ?mol-1,平衡常數K與上述反應速率常數k1、k-1、k2、k-2的關系式為K=;
②某溫度下反應2NO(g)+O2(g)?2NO2(g)的速率常數k=8.8×10-2L2?mol-2?s-1,當反應物濃度都是0.05mol?L-1時,反應的速率是mol?L-1?s-1;若此時縮小容器的體積,使氣體壓強增大為原來的2倍,則反應速率增大為之前的倍。
(2)2SO2(g)+O2(g)?2SO3(g)反應過程中能量變化如圖1所示。在V2O5存在時,該反應的機理為:V2O5+SO2→2VO2+SO3(快)4VO2+O2→2V2O5(慢)
下列說法正確的是。(填序號)
a.反應速率主要取決于V2O5的質量
b.VO2是該反應的催化劑
c.逆反應的活化能大于198kJ?mol-1
d.增大SO2的濃度可顯著提高反應速率
(3)某研究小組研究T1℃、T2℃時,氮硫的氧化物的轉化:NO2(g)+SO2(g)?NO(g)+SO3(g)△H<0中1gP(NO2)和lgP(SO3)關系如圖2所示,實驗初始時體系中的P(NO2)和P(SO2)相等、P(NO)和P(SO3)相等。
①T1T2(填“>”、“<”或者“=”),溫度為T1時化學平衡常數Kp=。
②由平衡狀態a到b,改變的條件是。組卷:26引用:1難度:0.7 -
20.乙酰氧基胡椒酚乙酸酯(F)具有抗氧化性、抗腫瘤作用,其合成路線如圖1所示。

已知:(見圖2)
(1)A→B的反應類型為。
(2)化合物C的名稱是。
(3)化合物E中含氧官能團的名稱為。請在圖3中用*標出化合物F中的手性碳原子。
(4)寫出化合物F與足量NaOH溶液反應的化學方程式。
(5)寫出同時滿足下列條件的E的一種同分異構體的結構簡式:。
①能與FeCl3溶液發生顯色反應;
②能發生銀鏡反應;
③核磁共振氫譜顯示有4種不同化學環境的氫,其峰面積比為6:2:1:1。
(6)請以乙醛和甲苯為原料制 ,寫出相應的合成路線流程圖。(無機試劑任用,合成路線流程圖1示例)組卷:26引用:3難度:0.5
,寫出相應的合成路線流程圖。(無機試劑任用,合成路線流程圖1示例)組卷:26引用:3難度:0.5


