2015-2016學年廣東省江門市臺山市華僑中學高三(上)周測化學試卷(9.11)
發布:2024/4/20 14:35:0
一、選擇題(每小題6分,共72分)
-
1.下列說法正確的是(NA表示阿伏加德羅常數的值)( )
A.在常溫常壓下,11.2 LN2含有的分子數為0.5 NA B.在常溫常壓下,1mol氖氣含有的原子數為2NA C.71gCl2所含原子數為2NA D.在同溫同壓下,相同體積的任何氣體單質所含的原子數相同 組卷:24引用:11難度:0.7 -
2.鋼鐵發生吸氧腐蝕時,正極上發生的電極反應是( )
A.2H++2e-═H2↑ B.Fe2++2e-═Fe C.2H2O+O2+4e-═4OH- D.Fe3++e-═Fe2+ 組卷:603引用:82難度:0.9 -
3.下列離子方程式正確的是( )
A.碳酸鎂中滴加稀鹽酸:CO32-+2H+=CO2↑+H2O B.向鹽酸中滴加氨水:H++NH3?H2O=NH4++H2O C.向亞硫酸鈉溶液中滴加硝酸:SO32-+2H+=SO2↑+H2O D.向漂白粉溶液通入少量二氧化硫:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO 組卷:7引用:1難度:0.7 -
4.下列關于溶液和膠體的敘述,正確的是( )
A.溶液是電中性的,膠體是帶電的 B.一束光線分別通過溶液和膠體時,后者會出現明顯光帶,前者則沒有 C.溶液中溶質粒子的運動有規律,膠體中分散質粒子的運動無規律,即布朗運動 D.通電時,溶液中的溶質粒子不會向兩極移動,膠體的分散質粒子向某一極移動 組卷:26引用:4難度:0.9
二.非選擇題:(28分)
-
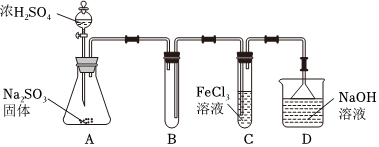 13.某研究小組用下圖裝置進行SO2 與FeCl3溶液反應的相關實驗(夾持裝置已略去).
13.某研究小組用下圖裝置進行SO2 與FeCl3溶液反應的相關實驗(夾持裝置已略去).
(1)在配制氯化鐵溶液時,需先把氯化鐵晶體溶解在中,再加水稀釋,這樣操作的目的是,操作中不需要的儀器有(填字母).
a.藥匙 b.燒杯 c.石棉網 d.玻璃棒 e.坩堝
(2)通入足量SO2時C中觀察到的現象為,
(3)根據以上現象,該小組同學認為SO2 與 FeCl3溶液發生氧化還原反應.
①寫出SO2與FeCl3溶液反應的離子方程式;
②請設計實驗方案檢驗有Fe2+生成;
③該小組同學向C試管反應后的溶液中加入硝酸酸化的BaCl2溶液,若出現白色沉淀,即可證明反應生成了.該做法SO2-4(填“合理”或“不合理”),理由是.
(4)D裝置中倒置漏斗的作用是.
(5)為了驗證SO2具有還原性,實驗中可以代替FeCl3的試劑有(填入正確選項前的字母).
a.濃H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液.組卷:167引用:5難度:0.5 -
14.廢舊鋰離子電池的正極材料(主要含有LiCoO2及少量Al、Fe等)可用于回收鈷、鋰,工藝流程如下:
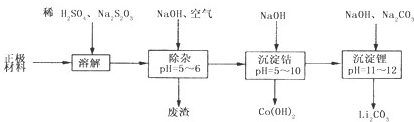
(1)在上述溶解過程中,S2O32-被氧化成SO42-,LiCoO2在溶解過程中發生反應的化學方程式為,還原產物是.
(2)在上述除雜過程中,通入空氣的作用是.廢渣的主要成分是.
(3)“沉淀鈷”和“沉淀鋰”的離子方程式分別為、.
(4)除了廢渣可以回收利用外,本工藝還可回收的副產品是.組卷:35引用:2難度:0.5


