2020-2021學年湖北省黃岡市蘄春縣高二(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共15小題,每小題3分,共45分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.我國明代《本草綱目》中收載藥物1892種,其中“燒酒”條目下寫道:“自元時始創其法,用濃酒和糟入甑,蒸令氣上…其清如水,味極濃烈,蓋酒露也.”這里所用的“法”是指( )
A.萃取 B.滲析 C.蒸餾 D.干餾 組卷:187引用:52難度:0.9 -
2.基態R原子的3p能級上只有一對成對電子,則R的最高價氧化物對應水化物的酸根離子是( )
A.RO32- B.RO3- C.RO4- D.RO42- 組卷:33引用:1難度:0.5 -
3.人類最早冶金的歷史年代曲線圖如圖所示(-1000表示公元前1000年),下列說法正確的是( )
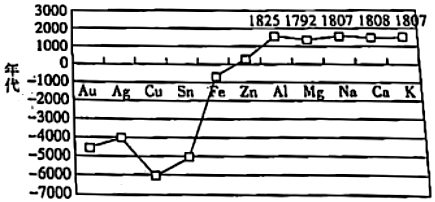
A.金屬越活潑,冶煉的年代一定越晚 B.冶煉金屬的歷史:電解氯化物比電解氧化物早 C.自然界中銅元素以游離態形式存在,故銅的冶煉年代最早 D.金屬氧化物(如Al2O3、Cu2O)也屬于金屬材料 組卷:62引用:2難度:0.8 -
4.分類法在化學發展中起到了非常重要的作用,下列說法正確的是( )
A.Mg、Al、Cu可以分別用置換法、直接加熱法和電解法冶煉得到 B.向煮沸的NaOH溶液中逐滴加入少量飽和FeCl3溶液,可制得Fe(OH)3膠體 C.酸性氧化物一定是非金屬氧化物,混合物、分散系、膠體有從屬關系 D.SiO2可與NaOH反應生成Na2SiO3和水,故SiO2屬于酸性氧化物 組卷:15引用:1難度:0.8 -
5.下列氫化物分子內共價鍵的極性由強到弱的順序正確的是( )
A.HF、H2O、CH4 B.H2O、CH4、HF C.CH4、HF、H2O D.CH4、H2O、HF 組卷:43引用:1難度:0.7 -
6.如表實驗裝置能達到相應實驗目的的是( )
實驗裝置 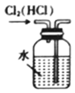

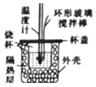

實驗目的 A.除去Cl2中的HCl B.制備并收集NO C.測定中和反應的反應熱 D.制取CO2 A.A B.B C.C D.D 組卷:3引用:1難度:0.5
二、非選擇題:本題共4小題,共55分。
-
18.亞氯酸鈉(NaClO2)是一種重要的含氯消毒劑,制備亞氯酸鈉的工藝流程如圖:

回答下列問題:
(1)亞氯酸鈉用作紙漿、紙張和各種纖維的漂白劑,是一種高效漂白劑,主要原因是亞氯酸鈉具有性。
(2)制備ClO2氣體的化學方程式為2NaClO3+H2O2+H2SO4═2ClO2↑+O2↑+Na2SO4+2H2O;制備時可用S代替H2O2,寫出該反應的離子方程式:。但“吸收”時卻不宜用S代替H2O2,理由是。
(3)可從“廢液”中回收的主要物質是(填化學式),“結晶”后經過濾即可獲得粗產品。
(4)測定某亞氯酸鈉樣品的純度:準確稱取亞氯酸鈉樣品mg,加入適量蒸餾水和過量的碘化鉀晶體,再滴入適量稀硫酸(發生反應ClO2-+4I-+4H+═2I2+Cl-+2H2O,配成250mL待測液。移取25.00mL待測液于錐形瓶中,加幾滴淀粉溶液,用cmol?L-1的Na2S2O3標準溶液進行滴定,消耗Na2S2O3標準溶液VmL(已知:I2+2S2O32-═2I-+S4O62-)。
①移取25.00mL待測液的儀器的名稱是。
②在接近滴定終點時,使用“半滴操作”可提高測定的準確度,其操作方法是將旋塞稍稍轉動,使半滴溶液懸于管口,用錐形瓶內壁將半滴溶液沾落,(請在橫線上補全操作),繼續搖動錐形瓶,觀察溶液顏色變化。
③該樣品中NaClO2的質量分數為(用含m、c、V的代數式表示);在滴定操作正確無誤的情況下,此實驗測得結果偏高,其可能的原因是。組卷:23引用:3難度:0.6 -
19.據報道,我國化學研究人員用Ni(NO3)2和Tb(CH3COO)3等合成了一個鎳的一維鏈狀配位聚合物(如圖1),對鎳配合物在磁性、電化學性質等方面的研究提出了理論指導。
請回答下列問題: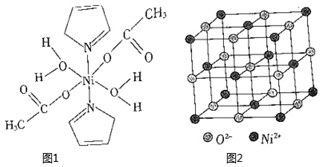
(l)基態Ni原子的基態電子排布式為,Ni在元素周期表中的位置是。
(2)C、N、O三種元素第一電離能最大的是(填元素符號),C在形成化合物時,其鍵型以共價鍵為主,其原因是。
(3)鎳的一維鏈狀配位聚合物中,碳原子的雜化方式為。已知:CH3COOH的沸點為117.9℃,HCOOCH3的沸點為32℃。CH3COOH的沸點高于HCOOCH3的沸點的主要原因是。
(4 )Ni(NO3)2的陰離子為NO3-,中心原子N原子的σ鍵電子對數為。陰離子NO3-的空間構型是。
(5)已知:氧化鎳的晶胞結構如圖2所示。
①若NA為阿伏加德羅常數的值,晶胞中最近的O2-之間的距離為a nm,則氧化鎳的密度為g?cm-3。
②某缺陷氧化鎳的組成為Ni0.95O,其中Ni元素只有+2價和+3價兩種價態,這兩種價態的離子數目之比N(Ni2+):N(Ni3+)為。組卷:7引用:2難度:0.5


